DNAは細胞のバネとしても働いている「DNAの新たな役割」を提唱
プレスリリース
国立研究開発法人科学技術振興機構
国立研究開発法人日本医療研究開発機構
概要
私たちの体を形成する細胞の核のなかには生命の設計図であるDNAが収められています。細胞および核は押されたり引っ張られたりして、絶えず物理的な力にさらされています。この力によりDNAが切れたりすると、細胞にさまざまな問題が生じます(図1)。これまで、細胞の核はその硬い殻の構造によって内部のDNAを守っていると考えられてきました。
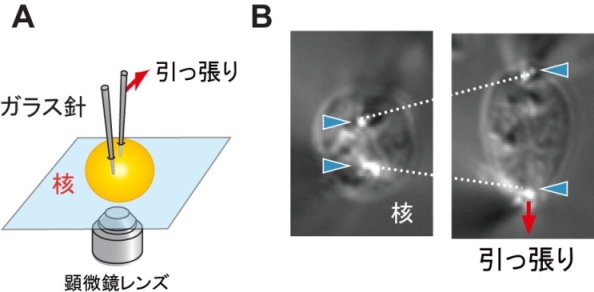
本研究では、直径が髪の毛の百分の一ほど(~1ミクロン)の細いガラス針を使ってヒト細胞の核を直接触り(図2A)、力を掛けたときの核のゆがみを観察することで、核の「強さ」を計測しました(図2B)。その結果、核は力に対抗するための「硬さ」と「弾性」を合わせ持っていることがわかりました。さらに、この弾性力は、これまで考えられてきた核の殻の構造だけでなく、収納されたDNA自体によっても生み出されていることがわかりました(図3)。これまで遺伝情報のメモリデバイスとみなされてきたDNAが、核の弾性を支えるバネの役割を演じているのです。
力が加わることによって核に生じるゆがみとそれに伴うDNAの損傷は、細胞に「死」や「がん化」など、様々な異常をもたらすと考えられています。今回の発見は、このような細胞の異常が起こるしくみの解明につながることが期待されます。
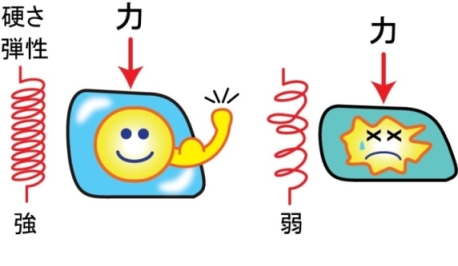 図1.細胞には絶えず力がかかっており、バネ弾性がないとつぶれてしまい(右)、細胞の機能が損なわれて異常が起きてしまう。
図1.細胞には絶えず力がかかっており、バネ弾性がないとつぶれてしまい(右)、細胞の機能が損なわれて異常が起きてしまう。
成果掲載誌
本研究成果は、平成29年4月20日正午(米国東部時間)に米国細胞生物学会誌 Molecular Biology of the Cell にハイライトとして掲載されます。
- 論文タイトル:
- Nucleosome−nucleosome interactions via histone tails and linker DNA regulate nuclear rigidity (リンカーDNAとヒストンテールを介したヌクレオソームの相互作用が細胞核の「硬さ」を制御する)
- 著者:
- Yuta Shimamoto, Sachiko Tamura, Hiroshi Masumoto, and Kazuhiro Maeshima(島本勇太、田村佐知子、増本博司、前島一博)
研究の詳細
研究の背景
本研究の成果
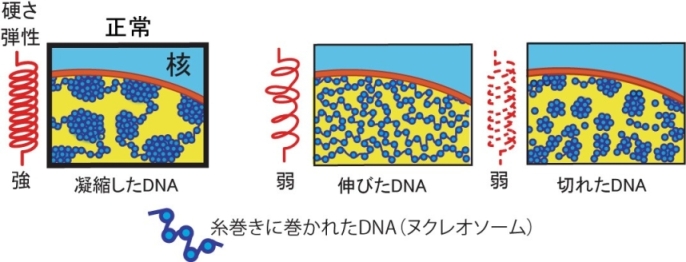
これまで、細胞核の硬さは核ラミナ(1)と呼ばれる殻の構造によって支えられているという考えが主流でしたが、本研究では、細胞核の硬さとバネ弾性が核内のDNAによって生み出されていることを明らかにしました。さらにDNAのバネ弾性がDNAのどのような構造によって生み出されているのか調べたところ、ヌクレオソーム(2)構造をとったDNAが伸びたり(図3中)、短く切れたり(図3右)するとバネ弾性が弱くなることを発見しました。このことから、DNAが不規則に凝縮し、塊をつくることで核のバネになることを突き止めました(図3左)。
この成果は、島本研究室(定量メカノバイオロジー研究室)で以前開発したガラス針を用いた力計測顕微鏡(3)(図2)と、前島研究室で確立された細胞核とDNAの折り畳みの研究手法とを組み合わせることによって達成されたものです。2つの技術を融合することによって、核のDNAの状態を変化させ(図3)、その状態が核の硬さ・バネ弾性にどのように影響するかを定量的に計測することに成功しました。
今後の期待
用語解説
- (1)核ラミナ
- 核膜の裏打ち構造で、核を支えていると考えられてきた。ラミンという線維状のたんぱく質がメッシュ構造をつくっている。
- (2)ヌクレオソーム
- 正の電荷を持った4種類のヒストンたんぱく質からできた糸巻きのような構造体。負の電荷をもったDNAが約2周巻ついて、数珠のように連なっている(図3下)。
- (3)力計測顕微鏡
- 細胞やタンパク質が出す微小な力を測ることができる装置。測りたいものに応じて、光や磁気の力を使ったり、ガラス針などを使ったりする。
研究体制と支援
本研究は、情報・システム研究機構国立遺伝学研究所・島本勇太准教授、田村佐知子テクニカルスタッフ、前島一博教授と、長崎大学・増本博司講師との共同研究です。本研究の遂行にあたり、国立研究開発法人日本医療研究開発機構(AMED)革新的先端研究開発支援事業(PRIME)「メカノバイオロジー機構の解明による革新的医療機器及び医療技術の創出」研究開発領域(研究開発総括:名古屋大学大学院 曽我部正博特任教授)(課題名「細胞核のマイクロメカニクスと機械受容メカニズムの解明」、研究代表者:島本勇太)、科学技術振興機構(JST)戦略的創造研究推進事業(CREST)「統合1細胞解析のための革新的技術基盤」(研究総括:東京大学大学院 菅野純夫教授)(研究課題名「超解像3次元ライブイメージングによるゲノムDNAの構造、エピゲノム状態、転写因子動態の経時的計測と操作」(JPMJCR15G2)、研究代表者:岡田 康志)、JSTテニュアトラック普及・定着事業、および科研費(15K14515、16H04746)の支援を受けました。
問い合わせ先
研究に関すること
情報・システム研究機構 国立遺伝学研究所 定量メカノバイオロジー研究室
准教授 島本 勇太 (しまもと ゆうた)
TEL:055-981-6784 メール:yuta.shimamoto“AT”nig.ac.jp
情報・システム研究機構 国立遺伝学研究所 生体高分子研究室
教授 前島 一博 (まえしま かずひろ)
TEL:055-981-6864 メール:kmaeshim“AT”nig.ac.jp
JST事業に関すること
科学技術振興機構 戦略研究推進部
川口 哲(かわぐち てつ)
TEL:03-3512-3524 メール:crest“AT”jst.go.jp
AMED事業に関すること
日本医療研究開発機構(AMED)基盤研究事業部 研究企画課
TEL:03-6870-2224 メール:kenkyuk-ask“AT”amed.go.jp
報道担当
情報・システム研究機構 国立遺伝学研究所 リサーチ・アドミニストレーター室
清野 浩明(せいの ひろあき)
TEL:055-981-6745(広報)5873 メール:hseino“AT”nig.ac.jp
科学技術振興機構 広報課
TEL:03-5214-8404 FAX:03-5214-8432
メール:jstkoho“AT”jst.go.jp
※メールは上記アドレス“AT”の部分を@に変えてください。
掲載日 平成29年4月21日
最終更新日 平成29年4月21日


