<図1>
研究代表者の研究室には、有機合成実験設備、細胞培養設備、動物実験設備が整備されており、ユニットPIC型核酸送達システムのためのポリマー合成から機能評価までのすべての実験を行うことができる。 ユニットPICの細胞内分布を解析するための共焦点レーザー顕微鏡(Carl Zeiss LSM710)やマウス体内におけるユニットPICの挙動を解析するためのin vivoイメージング装置(IVIS)も利用可能である。
ホーム > 平成26年度採択課題 > 高分子ナノテクノロジーを基盤とした革新的核酸医薬シーズ送達システムの創出
研究開発代表者:西山 伸宏
東京工業大学 資源化学研究所 教授

アンチセンス核酸、siRNA等のオリゴ核酸は、あらゆる疾患に対して遺伝子配列から容易に設計でき、高い特異性を有するために副作用が少なく、さらに化学合成によって製造も容易であることから次世代の医薬品として大きな可能性を秘めています。 しかしながら、これらの核酸医薬シーズを疾患治療へと展開するためには、核酸医薬シーズを標的組織に到達させ、かつ細胞内部へと送達することのできるデリバリーシステムの開発が必要不可欠となります。 現在までに、カチオン性脂質やカチオン性高分子を利用したデリバリーシステムが開発され、デリバリーが比較的容易な肝臓を標的とした一部のシステムは臨床試験へと進んでいますが、実用化にはまだ遠く、がん等の他の臓器・組織を標的にした場合には技術的課題が多く存在しているのが現状です。 このような背景において、高分子ミセル型医薬品の開発において実績を有している研究代表者は、「全身デリバリーで真に実用化が可能な核酸医薬シーズ送達システムとは、必要な機能をなるべくシンプルな構造の中に創り込んだシステムである」と考え、ポリエチレングリコール(PEG)-ポリアミノ酸ブロック共重合体とオリゴ核酸1分子から形成されるユニットPIC型核酸送達システムの開発に取り組んできました。 これまでの研究により、ユニットPIC型核酸送達システムは、明確な構造を有し、製造が極めて容易であることに加えて、siRNAのデリバリーにおいて、高い血中滞留性、固形がんへの特異的集積効果、サイズが小さいことによる優れた組織浸透性、標的分子のノックダウンに基づく優れた抗腫瘍効果、高い安全性が確認されています。 そこで本研究では、高分子ナノテクノロジーを基盤として、ユニットPICの血中滞留性および標的選択性のさらなる向上のためのポリマー設計の最適化、標的細胞による取り込み促進のための新規リガンド分子の開発、標的組織の微小環境において物理化学的性質が変化する機能性ポリマーの設計、体内における長期蓄積を回避する新規ポリマーの設計等のさまざまな要素技術の開発を行い、必要な機能をユニットPICへと組み込むことによって、真に臨床応用が可能な核酸医薬デリバリーシステムの構築を目指します。 日本発のデリバリーシステムによる難病の克服や新産業の創出に向けて、民間企業との共同研究やライセンスアウト、臨床試験に向けた国内医療機関との共同研究も活発に行って行きたいと考えています。

研究代表者の研究室には、有機合成実験設備、細胞培養設備、動物実験設備が整備されており、ユニットPIC型核酸送達システムのためのポリマー合成から機能評価までのすべての実験を行うことができる。 ユニットPICの細胞内分布を解析するための共焦点レーザー顕微鏡(Carl Zeiss LSM710)やマウス体内におけるユニットPICの挙動を解析するためのin vivoイメージング装置(IVIS)も利用可能である。
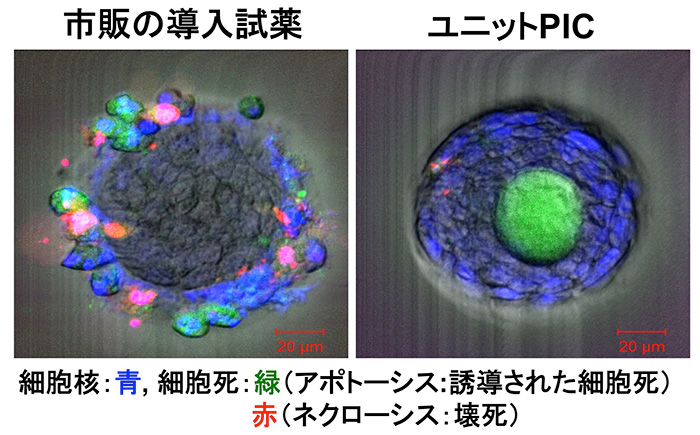
3次元培養ヒト膵臓がん(BxPC3)細胞(スフェロイド)への分裂期キナーゼに対するsiRNAの導入によるアポトーシスの誘導:市販の導入試薬では、スフェロイド表面にのみアポトーシス(緑)が誘導され、導入試薬による細胞傷害に由来するネクローシス(赤)も認められた。一方、ユニットPICでは、細胞傷害性は認められず、スフェロイド内部において効率的なアポトーシスの誘導が確認された。
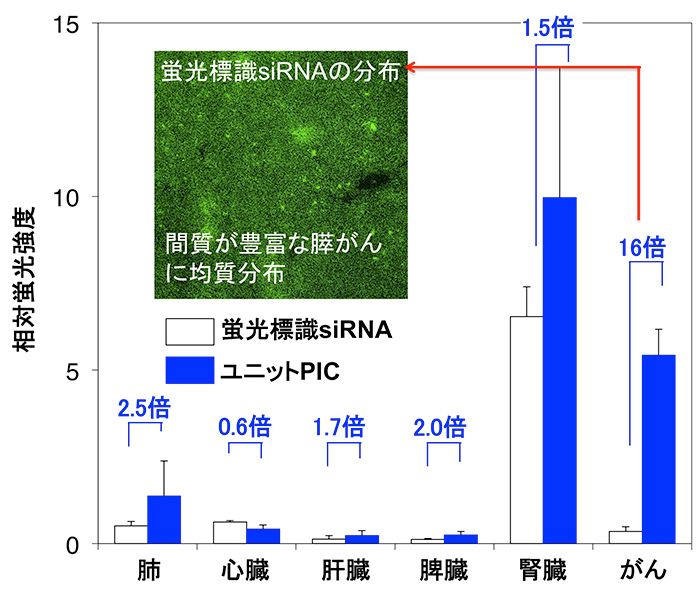
ヒト膵臓がん(BxPC3)細胞の皮下移植モデルマウスにおける蛍光標識siRNA内包ユニットPICの体内分布(経静脈内投与24時間後): ユニットPICに内包された蛍光標識siRNAは、固形がんに選択性に集積し、蛍光標識siRNA単独の16倍の集積を示した。また、ユニットPICに内包された蛍光標識siRNAは、がん組織内に均質に分布することが確認され(挿入写真)、サイズの小さいユニットPICは優れた組織浸透性を有することが確認された。