DMSOフリータイプの細胞凍結保存液をゼノアックリソース株式会社が開発―間葉系幹細胞の凍結保存に適応可能―
プレスリリース
国立研究開発法人国立成育医療研究センター
幹細胞評価基盤技術研究組合
国立研究開発法人日本医療研究開発機構
国立研究開発法人新エネルギー・産業技術総合開発機構
成果の概要
幹細胞評価基盤技術研究組合の組合員であるゼノアックリソース株式会社は、国立成育医療研究センター、産業技術総合研究所と共同でDMSO*1フリータイプの細胞凍結保存液の商品化に成功しました。本製品は間葉系幹細胞*2を始めさまざまな細胞の凍結保存に適応可能です。
本製品の製造においては、Good Manufacturing Practice(GMP)に準拠*3した製造管理及び品質管理が行われます。ケミカリーディファインド(化学的に定義された既知成分からなる)処方でXeno-フリー(ヒト以外の動物成分が含有されていない)の概念を満たしていることは勿論、これまで以上に品質の高い製品が供給できるため、バイオテクノロジーや再生医療分野で大きく貢献できるものと期待されます。
この細胞凍結保存液は、ゼノアックリソース株式会社が商品化し、平成27年12月1日に販売を開始します。
なお、この成果は、「再生医療の産業化に向けた細胞製造・加工システムの開発/ヒト間葉系幹細胞由来の再生医療製品製造システムの開発」プロジェクト(平成26年4月に新エネルギー・産業技術総合開発機構(NEDO)で採択され、平成27年度より日本医療研究開発機構(AMED)で継続中)により得られたものです。
事業の概要
本プロジェクトでは中畑 龍俊 京都大学iPS細胞研究所副所長をプログラム・スーパーバイザー(PS)とし、阿久津 英憲 国立成育医療研究センター部長をサブプロジェクトリーダー(SPL)とした間葉系グループにおいて、組合員企業と大学、研究機関が連携して目標達成を目指しています。
製品の概要
| 製品名 | 容量 | 製品コード | 希望小売価格 (税別) |
発売日 |
|---|---|---|---|---|
| STEM-CELLBANKER® DMSO Free GMP grade | 100mL | CB061 | 28000円 | 12月1日 |
| STEM-CELLBANKER® DMSO Free GMP grade | 20mL × 4 | CB063 | 28000円 | 12月1日 |
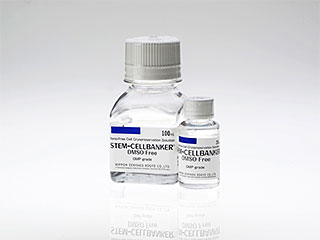
発売元:ゼノアックリソース株式会社
製造元:日本全薬工業株式会社
※本製品の国内に於ける販売はタカラバイオ株式会社と提携しています。
※本製品は医薬品ではありません。
- STEM-CELLBANKER® DMSO Free GMP gradeは、凍害防御剤としてのDMSOを使用していません。
- DMSOにより分化誘導が懸念される細胞の凍結保存、そしてDMSOの毒性がご心配なお客様のために開発されました。血清タイプ・無血清タイプに加え、お客様の選択肢が更に広がりました。
本製品の間葉系幹細胞への適用に関する成果は、阿久津英憲SPLが率いる研究グループでの共同研究成果を活用したものです。本プロジェクトにおいて、ゼノアックリソース株式会社は、細胞凍結保存に関する技術を応用し、既知成分からなるXeno-フリーの概念を満たす最適なDMSOフリータイプの凍結保存液の処方検討を行ってきました。また、研究期間中にGMP生産体制を整え、GMPに準拠した製品化を達成できるよう進めてきました。その結果、今回、予定よりも早期に生産体制および製品化の目標を達成することができました。
本成果に関する阿久津 英憲SPLのコメント
「ゼノアックリソース株式会社の凍結保存液STEM-CELLBANKER®シリーズにGMP gradeのDMSOフリー凍結保存液が開発されました。本プロジェクトでは、産業技術総合研究所や国立成育医療研究センター研究所などの複数施設において行われた評価試験で、このDMSOフリー・GMP grade凍結保存液が様々な間葉系幹細胞を良好な状態で凍結保存できることが示されました。
再生医療の発展には細胞の保存・輸送の品質管理は必須であり、世界基準の製造設備で製造された製品によりグローバルな再生医療の発展にさらに貢献できると確信しています。」
参考
- *1 DMSO
- ジメチルスルホキシド(dimethyl sulfoxide)は(CH3)2SOの分子式で表される有機化合物で、細胞凍結保存時に細胞内で氷が結晶化し、ダメージを与えるのを防ぐために添加しており、国内の細胞バンクを始め、臨床用・研究用を問わず広く使用されています。
一方で、DMSO濃度が高くなると細胞毒性を示すことも知られており、DMSOを使用しない凍結保存液の開発も望まれていました。 - *2 間葉系幹細胞
- 骨髄や脂肪など「間葉」といわれる組織由来の体性幹細胞で、軟骨、骨、脂肪、心筋、神経などへの分化能を有し、iPS/ES細胞と共に、再生医療への応用が大きく期待されている細胞です。腫瘍形成能がほとんど無いと考えられており、間葉系幹細胞を用いた多くの臨床研究が国内外で進められています。
- *3 Good Manufacturing Practice(GMP)準拠
- GMPは、医薬品および医薬部外品の品質確保を図るため、原料の受入れから最終製品の包装、出荷に至るまで、全製造工程における組織的な管理に基づく品質保証体制を確立するために定められた基準です。GMPグレード品は、新たに建設したGMP基準に適合した工場で、GMP体制の下、GMP基準に則った製造方法で製造しています。製品が環境にさらされる作業はすべてグレードA環境で実施し、調製液のバイオバーデン管理、無菌ろ過フィルターの完全性試験を行うことによって無菌性を保証しています。
お問い合わせ先
ゼノアックリソース株式会社 細胞工学研究室室長 佐瀬 孝一
Tel:024-945-2300 E-mail:saze-kohichi“AT”zenoaq.jp
国立研究開発法人 国立成育医療研究センター研究所 再生医療センター 生殖医療研究部
部長 阿久津 英憲
Tel:03-5494-7048 E-mail:akutsu-h“AT”ncchd.go.jp
幹細胞評価基盤技術研究組合 専務理事 中村 吉宏
Tel:03-5541-2790 E-mail:nakamura“AT”scetra.or.jp
国立研究開発法人 日本医療研究開発機構 戦略推進部 再生医療研究課
Tel:03-6870-2220 E-mail:saisei“AT”amed.go.jp
国立研究開発法人 新エネルギー・産業技術総合開発機構 広報部
Tel:044-520-5151 E-mail:nedo_press“AT”ml.nedo.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください
掲載日 平成27年11月25日
最終更新日 平成27年11月25日


