皮膚の健康と病気を調節する脂質の新しい役割の発見―難治性皮膚疾患の治療に向けての新しい創薬に期待―
プレスリリース
公益財団法人東京都医学総合研究所
東京都福祉保健局
国立研究開発法人科学技術振興機構
国立研究開発法人日本医療研究開発機構
(公財)東京都医学総合研究所の村上誠参事研究員、山本圭研究員らは、脂質を分解する酵素の研究から、皮膚の健康と病気を調節する新しい脂質メカニズムを発見しました。表皮角化細胞(ケラチノサイト)の酵素が新しい活性を持つ脂質を作り出し、皮膚の分化と肥厚を進めることを初めて見つけました。この成果は、乾癬や皮膚癌などの病気の新しい診断法や治療薬の開発につながると考えています。
この研究は、京都大学の椛島健治教授、千葉大学の神戸直智准教授、米国ワシントン大学のMichael Gelb教授、仏国CNRS研究所のGérard Lambeau教授らとの共同研究により、国立研究開発法人科学技術振興機構(JST)の戦略的創造研究推進事業 チーム型研究(CREST)(平成27年4月1日より、本研究課題は日本医療研究開発機構(AMED)に承継され、引き続き研究開発の支援が実施されています)および日本学術振興会科研費(新学術領域研究、基盤研究)の一環として行われました。この研究は、2015年10月5日(米国東部時間)に米国科学誌『Journal of Experimental Medicine(ジャーナル・オブ・エクスペリメンタル・メディシン)』にオンライン掲載されました。
研究の背景
脂質は皮膚にとって非常に大切な生体成分です。外界に接する皮膚表面の表皮角化細胞(ケラチノサイト)は脂質(特にセラミド)の層を作り、体内からの水分の蒸散または病原体などの侵入から体を守っています。日常、表皮角化細胞は分化と増殖を行っていますが、このサイクルが壊れると皮膚のバリアが乱れ、治療の難しい乾癬*1やかぶれ(接触性皮膚炎)*2などのアレルギーにつながります。しかし、セラミド以外の脂質が皮膚でどのような役割をしているかについては十分理解されていませんでした。村上研究員らは、リン脂質を分解する酵素(ホスホリパーゼA2*3)に関する研究を進める中で、表皮に存在する酵素によってできるユニークな脂質(リゾ型リン脂質*4)が健康や病気の調節に重要な役割を果たしていることを発見しました。
研究の概要
村上研究員らは、皮膚異常を発症するモデルマウスの皮膚の遺伝子をマイクロアレイ法(発現遺伝子解析)により比較しました。その結果、これまで機能が不明だった細胞外に分泌されるリン脂質分解酵素(PLA2G2F:分泌性ホスホリパーゼA2のひとつ)が表皮にのみ強く発現していることを見いだしました。同じことはヒトの皮膚でも起こり、乾癬患者の肥厚した表皮で発現が増加していました。そこで、この酵素の皮膚における役割をさらに解明するために、遺伝子操作したモデルマウスを作りました。
PLA2G2Fを過剰に発現させたマウスは強い皮膚異常を示し、乾癬の指標となる遺伝子の発現量が増加していました。一方、PLA2G2Fを欠損させたマウスの皮膚は一見正常に見えましたが、電子顕微鏡下で観察すると、腹部皮膚の角質が剥がれており、皮膚から体外への水分の漏出量が増加し、皮膚のバリア機能が損なわれていました。表皮角化細胞をPLA2G2F欠損マウスから取り出して試験管内で培養すると、分化の目印となる遺伝子の発現も損なわれていました。このPLA2G2F欠損マウスに実験的に乾癬やかぶれを引き起こすと、表皮の肥厚と活性化が抑えられ、病態が改善しました(図A)。さらに、実験的に皮膚癌を引き起こすと、腫瘍の増殖は劇的に抑えられました。これらの結果から、PLA2G2Fは表皮の肥厚をさらに悪化させていることが分かりました。
PLA2G2Fの作用には、この酵素が産生する脂質代謝物が関わっているはずです。そこで私たちはこの脂質を同定するために、遺伝子操作マウスの皮膚を用いて脂質の全解析を行いました。その結果、PLA2G2Fの発現量と同じ変動パターンを示す唯一の脂質代謝経路を同定しました。つまり、PLA2G2Fは表皮のリン脂質に作用し、ドコサヘキサエン酸(DHA)を持つエーテル型リン脂質*5(プラズマロージェン型ホスファチジルエタノールアミン)を、リゾ型(ドコサヘキエン酸を失ったリン脂質)に変換していることが判明しました(図B)。このリゾ型リン脂質(P-LPE)を欠損マウスに与えると、抑えられていた乾癬の症状が野生型マウスのレベルまで悪化しました。また、欠損マウスから取り出した表皮角化細胞にも同様の効果が認められました。したがって、このリゾ型リン脂質は、乾癬やかぶれの新規バイオマーカーであると同時に、新しい生理活性脂質*6であることが明らかとなりました。
これまでに私たちは、分泌性ホスホリパーゼA2分子群の生体内における役割を解明してきました(Cell Metab 2014, Nat Immunol 2013, J Exp Med 2013, J Clin Invest 2010など)。この研究は、皮膚に発現しているPLA2G2Fの機能を解明し、この酵素により作り出されたリゾ型リン脂質が生命応答の調節に関わることを示した初めての研究成果です(図C)。また、治りにくい表皮肥厚性の病気に新しい診断法・治療法を提唱するものです。
今後の展望
皮膚のPLA2G2Fやその代謝物であるリゾ型リン脂質の量は、乾癬や皮膚癌などの治りにくい皮膚疾患の診断のための新規バイオマーカーとなる可能性があります。また、この酵素が皮膚にのみ発現していることを考えると、この酵素やリゾ型リン脂質を標的とした創薬は、こうした皮膚疾患に対して新規の予防・治療法の開発につながることが期待できます。
用語解説
- *1 乾癬:
- 慢性かつ難治性の皮膚角化疾患。赤い発疹が出現し、その上に角質細胞が剥がれ落ちた白疹が出現する。白色人種に多く、日本人の罹患率は約0.1%である。表皮の増殖速度が正常時をはるかに上回り、周縁の皮膚組織に炎症を起こしながら表皮が過度に増殖し、角化の亢進によって白いカサブタ状の皮疹を多く生じる。病態形成にT細胞性の自己免疫系(特にTh17免疫応答)が関与するといわれている。マウスの皮膚に化学物質(イミキモド)を反復塗布すると、乾癬と類似した病態を誘導することができる。
- *2 かぶれ(接触性皮膚炎):
- アレルギーは古典的に大きく4つのタイプに分類され、接触性皮膚炎はIV型に分類される。抗原の反復暴露を受けることによりT細胞を中心とした免疫反応が起こり、皮膚炎を生じる。ウルシかぶれや金属アレルギーが、この代表である。マウスでは化学物質(ジニトロフルオロベンゼン)を皮膚に反復塗布することで接触性皮膚炎の病態を誘導することができる。
- *3 ホスホリパーゼA2:
- リン脂質を加水分解して脂肪酸とリゾ型リン脂質を産生する酵素群の総称。本研究では特に、細胞外に分泌されるホスホリパーゼA2の一群である分泌性ホスホリパーゼA2(sPLA2; “s”はsecretedを表わす)を取り扱っている。哺乳動物には11種類のアイソザイム(類似の構造を持つ一群の酵素タンパク質)が存在し、本研究ではこのうちIIF型分泌性ホスホリパーゼA2(PLA2G2F)を取り扱っている。
- *4 リゾ型リン脂質:
- 細胞膜を構成するリン脂質は通常2つの脂肪酸を持っている。このうちの一方が取り除かれて脂肪酸がひとつになったリン脂質をリゾ型リン脂質と呼ぶ。図Bを参照。
- *5 エーテル型リン脂質:
- リン脂質は通常、構成成分の脂肪酸とエステル結合で結合しているが、エーテル結合した脂肪酸を持つものがある。エーテル型リン脂質の中でも、図1Bに示す構造式の黄色部分に二重結合を持つもの(特にホスファチジルエタノールアミン)は、プラズマロージェンと呼ばれる。
- *6 生理活性脂質:
- 脂質メディエーターとも呼ばれ、脂肪酸から産生されるものとリゾ型リン脂質から産生されるものがある。脂肪酸由来の生理活性脂質としては、脂肪酸の一種であるアラキドン酸から生合成されるプロスタグランジンやロイコトリエンが有名であり、一般に炎症を促進する活性を持つ。一方で、エイコサペンタエン酸やドコサヘキサエン酸などの脂肪酸から産生される生理活性脂質は抗炎症作用を示す。リゾ型リン脂質由来の生理活性脂質としてはリゾホスファチジン酸(LPA)や血小板活性化因子(PAF)がよく知られている。今回同定したリゾ型リン脂質(P-LPE)は、これまでに報告のない新規のリゾ型リン脂質性の生理活性脂質である。
論文タイトル
“The role of group IIF-secreted phospholipase A2 in epidermal homeostasis and hyperplasia”
(表皮の恒常性と肥厚におけるIIF型分泌性ホスホリパーゼA2の役割)
図の解説
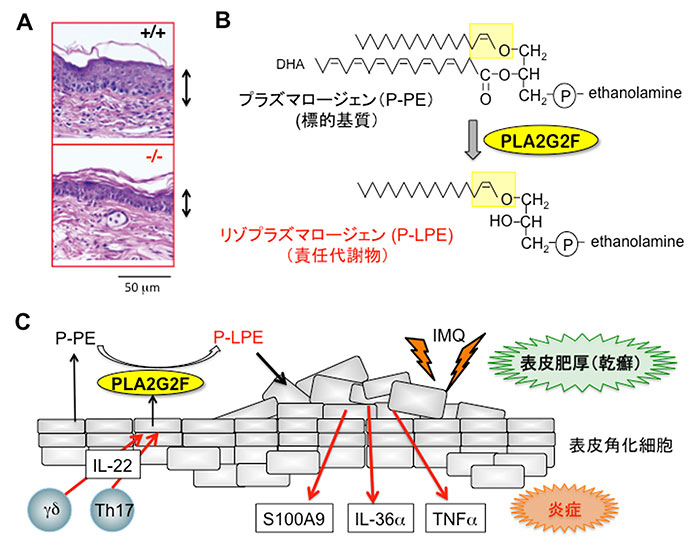
- PLA2G2Fの欠損マウス(-/-)では野生型マウス(+/+)と比べて乾癬による表皮の肥厚が起こりにくい(右端の両端矢印は表皮の厚みを示す)。
- 皮膚において、PLA2G2Fは特殊なエーテル型リン脂質(プラズマロージェン; P-PE)をリゾ型(P-LPE)に変換する。
- 表皮が肥厚する疾患(乾癬)におけるPLA2G2Fの作用機序。乾癬で増加するTh17サイトカイン(IL-22)により発現が誘導されたPLA2G2Fは、表皮角化細胞から分泌されたプラズマロージェン(P-PE)をリゾ型(P-LPE)に変換する。P-LPEは表皮角化細胞に作用して乾癬の病状(表皮の肥厚と炎症)を悪化させる。
- IMQ(イミキモド):マウスに乾癬様の皮膚炎を引き起こす薬物。
- S100A9:乾癬で発現が著しく増加するタンパク質で、炎症の増悪や感染防御に関わる。
- IL-36α:表皮に特異的なサイトカインで、乾癬で誘導され表皮肥厚に関わる。
- TNFα:表皮角化細胞や免疫細胞から産生される代表的な炎症性サイトカイン。
- γδT細胞:皮膚に常在するT細胞の一群で、Th17型サイトカイン(IL-17A, IL-22等)を産生する。
参考
本研究と並んで、米国アイオワ大学のStanley Perlman教授との共同研究により行われた分泌性ホスホリパーゼA2に関する以下の共著論文も2015年9月21日に『Journal of Experimental Medicine』に発表されました。
お問い合わせ先
リリース内容に関するお問い合わせ先
公益財団法人東京都医学総合研究所
脂質代謝プロジェクト 村上
電話:03-5316-3228
事務局研究推進課 佐久間・榎本
電話:03-5316-3109
JSTの事業に関するお問い合わせ先
川口 哲(カワグチ テツ)
科学技術振興機構 戦略研究推進部 ライフイノベーショングループ
〒102-0076 東京都千代田区五番町7 K’s五番町
Tel:03-3512-3524 Fax:03-3222-2064
E-mail:crest“AT”jst.go.jp
AMEDの事業に関するお問い合わせ先
坂本 祥純(サカモト ヨシズミ)
日本医療研究開発機構 戦略推進部研究企画課
〒100-0004 東京都千代田区大手町 1-7-1 読売新聞ビル
Tel:03-6870-2224 Fax:03-6870-2243
E-mail:kenkyuk-ask“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください
関連リンク
掲載日 平成27年10月13日
最終更新日 平成27年10月13日


