てんかん治療薬遺伝子型検査の臨床的有用性を実証―遺伝子検査により薬疹発症率を半減―
プレスリリース
理化学研究所
日本医療研究開発機構
要旨
理化学研究所(理研)生命医科学研究センターの莚田泰誠チームリーダーを中心とする共同研究グループ※は、てんかん[1]治療薬の使用における遺伝子型検査の有用性に関する臨床介入研究を行い、「HLA-A*31:01遺伝子型」を用いた薬理遺伝学検査の臨床的有用性[2]を実証しました。これは、理研と国内18医療機関、36病院※の共同研究として実施した前向き臨床研究「Genotype-Based Carbamazepine Therapy(GENCAT)study [3]」の成果です。
カルバマゼピンは、てんかん治療の第一選択薬として世界中で使われています。しかしこの薬は、薬疹(薬によって起こる皮膚や眼、口などの粘膜に現れる発疹)による副作用発症率が高いことが、医療上、大きな問題となっていました。2011年、理研はHLA-A*31:01遺伝子型が、日本人におけるカルバマゼピンによる薬疹の発症に大きく関与していることを明らかにしました注1)。そして2012年、カルバマゼピンの投与が必要とされた患者を対象とした前向き臨床研究「GENCAT study」が開始されました。
この研究では、カルバマゼピンを投与予定の日本人患者1,130名全員に、カルバマゼピンを投与する前にHLA-A*31:01遺伝子型検査を行い、遺伝子型陰性者にはカルバマゼピンを、陽性者には代替薬をそれぞれ投与しました。その結果、HLA-A*31:01遺伝子型検査により、カルバマゼピンによる薬疹の発症率が41~61%減少することが示され、HLA-A*31:01遺伝子型を用いた薬理遺伝学検査の臨床的有用性が実証されました。
今回の結果は、カルバマゼピンによる治療が必要な患者に対して、投与前に薬理遺伝学検査を行うことで、薬疹による副作用を適切に防止できることを実証しています。これは、個人に最適な治療法の確立を目指したprecision medicine[4]の実現に大きく近づく成果です。
本成果は、米国の医学雑誌『JAMA Neurology』に掲載されるのに先立ち、オンライン版(4月2日付け:日本時間4月3日)に掲載されます。
本研究は、日本医療研究開発機構(AMED)「オーダーメイド医療の実現プログラム」および文部科学省「次世代がん研究戦略推進プロジェクト がん薬物療法の個別適正化プログラム」の支援を受けて実施しました。
注1)Ozeki T, Mushiroda T, Yowang A, et al. Genome-wide association study identifies HLA-A*3101 allele as a genetic risk factor for carbamazepine-induced cutaneous adverse drug reactions in Japanese population. Hum Mol Genet 2011;20(5):1034-1041.
背景
カルバマゼピンはてんかん治療、特に部分発作における第一選択薬であり、世界中で躁病、躁うつ病の躁状態、統合失調症の興奮状態、三叉神経痛の治療にも使われています。しかし、カルバマゼピンは、薬疹(薬によって起こる皮膚や眼、口などの粘膜に現れる発疹)による副作用発症率が3.7~13%と非常に高く注2)、臨床において、カルバマゼピンの投与が必要な患者を治療する上で大きな問題となっています。
これまで、薬疹が起こりやすい患者を事前に予測する方法がないため、医療現場では、カルバマゼピンを投与後に薬疹が出現した場合は、直ちにカルバマゼピンを中止するなどの対応がとられていました。しかし、一部の患者は薬疹が重症化し、皮膚粘膜眼症候群(スティーブンス・ジョンソン症候群、SJS)、中毒性表皮壊死融解症(TEN)、薬剤性過敏性症候群をきたし、死亡または重篤な後遺症が残る症例もありました。厚生労働省へ報告された薬剤副作用を集計した報告注3)では、年間にSJS-TENが602例発症し、そのうち、8.7%(52.4例/年)が死亡、5.3%(31.6例/年)が後遺症ありまたは未回復であり、カルバマゼピンはそれらの発症例における推定原因医薬品の第3位となっています。
2011年、理研統合生命医科学研究センター(現 生命医科学研究センター)は、カルバマゼピンによる薬疹発症例を用いたゲノムワイド関連解析を行い、HLA遺伝子[5]の一つ、HLA-A遺伝子のHLA-A*31:01遺伝子型を持つ日本人の患者は、同型を持っていない患者に比べてカルバマゼピンによる薬疹が9.5倍起こりやすいことを報告しました。同年、その結果は、カルバマゼピンの添付文書にも記載されました。しかし、HLA-A*31:01遺伝子型検査の臨床的有用性が証明されていないため、HLA-A*31:01遺伝子型検査は保険収載されておらず、国内の医療機関ではカルバマゼピンを投与する患者にHLA-A*31:01遺伝子型検査を実施することができません。
このため、理研は全国の18医療機関、36病院と共同研究グループを立ち上げ、てんかん治療薬カルバマゼピンの遺伝子型検査の有用性に関する前向き臨床研究「Genotype-Based Carbamazepine Therapy (GENCAT) study」を、2012年に開始しました。
注2)Kramlinger KG, Phillips KA, Post RM. Rash complicating carbamazepine treatment. J Clin Psychopharmacol 1994;14(6):408-413; Arif H, Buchsbaum R, Weintraub D, et al. Comparison and predictors of rash associated with 15 antiepileptic drugs. Neurology 2007;68(2):1701-1709; McCormack M, Alfirevic A, Bourgeois S, et al. HLA-A*31:01 and carbamazepine-induced hypersensitivity reactions in Europeans. N Engl J Med 2011;364(12):1134-1143; Shirzadi M, Alvestad S, Hovdal H, et al. Comparison of carbamazepine rash in multiple sclerosis and epilepsy. Acta Neurol Scand 2012;125(1):60-63.
注3)医薬品医療機器総合機構『医薬品・医療機器等安全性情報』(No.290、2012年4月)
研究手法と成果
GENCAT studyでは、医療機関においてカルバマゼピンの投与が必要と考えられた日本人患者1,130名に、本研究に対する文書での同意を得た後、HLA-A*31:01遺伝子型検査を実施しました。そして、遺伝子型検査の結果が陰性の場合はカルバマゼピンを投与し、遺伝子型検査結果が陽性の場合はカルバマゼピン以外の代替薬をそれぞれ投与し、その後8週間、カルバマゼピンによる薬疹が発症するかどうかを追跡しました(図1)。これは、日本で初めて実施された薬理遺伝学検査による臨床介入研究です。
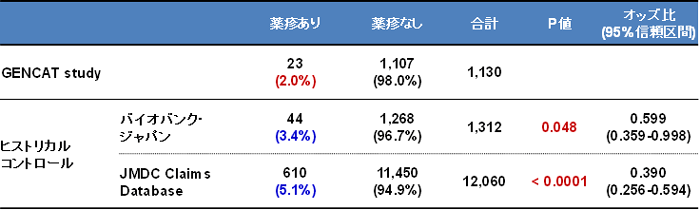
2012年1月から2014年11月までの間、日本人患者1,130名のうち、198名(17.5%)がHLA-A*31:01遺伝子型検査が陽性でした。8週間の追跡期間中にカルバマゼピンによる薬疹の発症を23例(2.0%)に認めました。このうち4例で入院での治療が必要となりましたが、重篤な副作用であるSJS-TENは1例も発症しませんでした(バイオバンク・ジャパン[6]におけるSJS-TENの発症は1,312名中3例)。
この薬疹発症率をバイオバンク・ジャパンの薬疹発症率(3.4%)と比べたところ、薬疹発症率が59%へと有意に低下していることが示されました(P値[7]=0.048)。さらに、株式会社日本医療データセンターが有する健康保険組合レセプトデータ(JMDC Claims Database)における薬疹発症率(5.1%)と比較したところ、同様に薬疹発症率が39%へと 有意に低下していることが示されました(P値<0.0001)(表1)。すなわち、カルバマゼピンによる薬疹の発症率が41~61%減少することが分かりました。
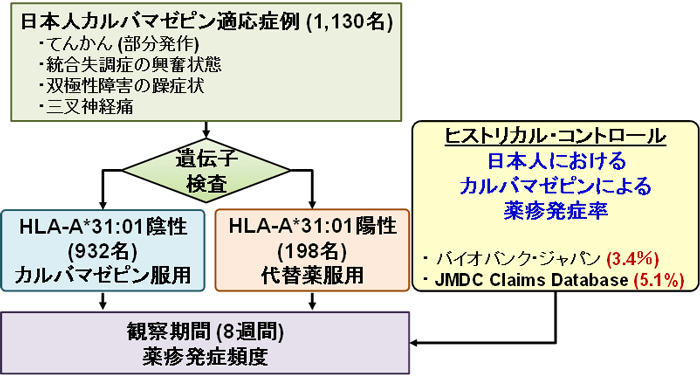
図1 GENCAT studyの概要
本研究の結果より、カルバマゼピンを投与する前にHLA-A*31:01遺伝子型検査を行い、その結果に基づいてカルバマゼピンを投与するかどうかを決定することが、カルバマゼピンによる薬疹の適切な予防法となることが証明され、HLA-A*31:01遺伝子型を用いた薬理遺伝学検査の臨床的有用性も実証されました。
今後の期待
本成果により、カルバマゼピンの投与が必要な患者にHLA-A*31:01の遺伝子検査を行うことで、カルバマゼピンによる薬疹のリスクを軽減できることが実証されました。これは、個人に最適なてんかん治療の確立を目指した、precision medicineの実現に向けた、大きな前進です。
将来、HLA-A*31:01遺伝子型検査が日本で保険収載された場合、カルバマゼピンによる薬疹発症率が減るとともに、重篤な副作用であるSJS-TENによる死亡や後遺症を適切に予防できると期待できます。
論文情報
- タイトル
- Association of HLA-A*31:01 screening with the incidence of carbamazepine-induced cutaneous adverse reactions in a Japanese population
- 著者名
- Taisei Mushiroda, Yukitoshi Takahashi, Teiichi Onuma, Yoshiaki Yamamoto, Tetsumasa Kamei, Tohru Hoshida, Katsuya Takeuchi, Kotaro Otsuka, Mitsutoshi Okazaki, Masako Watanabe, Kosuke Kanemoto, Tomohiro Ohshima, Atsushi Watanabe, Shiro Minami, Kayoko Saito, Hisashi Tanii, Yasushi Shimo, Minoru Hara, Shinji Saitoh, Toshihiko Kinoshita, Masaki Kato, Naoto Yamada, Naoki Akamatsu, Toshihiko Fukuchi, Shigenobu Ishida, Shingo Yasumoto, Atsushi Takahashi, Takeshi Ozeki, Takahisa Furuta, Yoshiro Saito, Nobuyuki Izumida, Yoko Kano, Tetsuo Shiohara, Michiaki Kubo, for the GENCAT Study Group
- 雑誌
- JAMA Neurology
- DOI
- 10.1001/jamaneurol.2018.0278
補足説明
- [1] てんかん
- さまざまな原因によって引き起こされる慢性の脳疾患。大脳の神経細胞の過剰な放電(興奮)によって繰り返し引き起こされる反復性の発作を特徴とし、変異に富む臨床症状や検査所見を伴う。発症率は人口の0.5~1%である。なかでも発作がある程度の長さ以上続く状態、または短い発作の場合でも繰り返し起こって、その間の意識の回復がないものをてんかん重積状態と呼び、生命に危機が及ぶ可能性がある。
- [2] 薬理遺伝学検査の臨床的有用性
- 薬理遺伝学研究は、特定の患者における薬効や副作用などの薬物応答性に関連する遺伝因子を見いだし、個人個人に合った薬を適切に使い分けることを目指す研究分野である。2002年に発見されたエイズ治療薬アバカビルの薬疹と関連するHLA-B*57:01遺伝子型については、2008年に米国のPREDICT-1試験において、HLA-B*57:01遺伝学的検査の臨床的有用性がランダム化比較試験により検討され、遺伝子型検査の導入により薬疹の発症率が約50%に減少することが示された。また、台湾人で見つかった、カルバマゼピンによるSJS-TEN関連遺伝子のHLA-B*15:02遺伝子型検査では、HLA-B*15:02陽性患者にカルバマゼピン以外の薬を服用した場合、SJS-TEN患者の発生が全くみられなかったことが2011年に報告されている。これらの臨床試験の結果を受けて、米国や台湾では、アバカビルやカルバマゼピンによる治療を開始する前に遺伝子型検査を行うことが、標準治療として患者に提供されている。
なお、日本医学会「医療における遺伝学的検査・診断に関するガイドライン(2011年2月)」では、単一遺伝子疾患、多因子疾患、薬物等の効果・副作用・代謝、個人識別に関わる遺伝学的検査等、ゲノムおよびミトコンドリア内の原則的に生涯変化しない、その個体が生来的に保有する遺伝学的情報を明らかにする検査をヒト遺伝学的検査と呼ぶ。遺伝学的検査は、分析的妥当性(精度管理がきちんとしていて再現性が高いこと)、臨床的妥当性(検査結果の意味付けが十分にされていること)、臨床的有用性(診断がつけられることにより、疾患の見通しについての情報が得られたり、予防法や治療法に結びついたりするような臨床上のメリットがあること)などを確認した上で、有用と考えられる場合に実施することとなっている。 - [3] 前向き臨床研究「Genotype-Based Carbamazepine Therapy(GENCAT)study」
- HLA-A*31:01の遺伝子検査によるてんかん治療薬の使い分けの臨床的有用性を実証するために、2012年に開始した臨床研究。国内の18医療機関・36病院が参画した。参加した患者全員に遺伝子検査の結果に基づいて、てんかん治療薬の使い分けをし、追跡調査をすることにより、報告されている日本人におけるカルバマゼピンによる薬疹発症率を比較した。このような研究デザインを前向き(プロスペクティブ)臨床研究という。なお、今回の臨床研究では、株式会社理研ジェネシスおよび理研が共同開発した、小型遺伝子解析システム「Quimple」を病院内に設置し、遺伝子型解析を行った。
株式会社理研ジェネシスは、理研ゲノム医科学研究センター(現 生命医科学センター)が培った遺伝子解析技術を基盤として、株式会社理研ベンチャーキャピタル(有馬朗人社長)と凸版印刷の共同出資によって2007年10月15日に設立。理研との技術連携を図りながら、遺伝子解析の受託解析事業、診断薬・試薬事業、周辺サービス事業などを推進し、Precision Medicineを実現化することによって個々人の生活向上を図ることを目標としている。 - [4] Precision medicine
- 「精密医療」と訳され、個人の遺伝子情報などを含むオミックス・データの解析に基づいて、患者を層別化し、そのサブグループごとの治療や予防(先制医療)の確立を目指す「個人の詳細な情報をもとにした医療」を意味する。
- [5] HLA遺伝子
- ヒト白血球型抗原(human leukocyte antigen:HLA)を決定する遺伝子群。HLA遺伝子には多くの種類が存在し、さらにそれぞれの遺伝子が数十種類の異なるタイプを持つ。HLAは免疫に関係が深く、多くの疾患の発症や副作用の発現リスク因子であることが報告されている。
- [6] バイオバンク・ジャパン
- 日本人集団27万人を対象とした、世界最大級の疾患バイオバンク。オーダーメイド医療の実現プログラムを通じて実施され、ゲノムDNAや血清サンプルを臨床情報と共に収集し、研究者へのデータ提供や分譲を行っている。
- [7] P値
- ある試験において、二つの群の間の差が偶然生じる可能性を示す指標。例えば、「P値が0.05である」とは、その結果を偶然生じることが100回に5回あることを意味する。すなわち、P値が小さいほど、二群間の差が生じている可能性が高い
発表者・機関窓口
発表者
理化学研究所 生命医科学研究センター ファーマコゲノミクス研究チーム
チームリーダー 莚田 泰誠(むしろだ たいせい)
(旧 統合生命医科学研究センター ファーマコゲノミクス研究グループ グループディレクター)
機関窓口
理化学研究所 広報室 報道担当
TEL:048-467-9272 FAX:048-462-4715
E-mail:ex-press”AT"riken.jp
AMED事業に関するお問い合わせ先
日本医療研究開発機構(AMED)
基盤研究事業部 バイオバンク課
TEL:03-6870-2228
E-mail:kiban-kenkyu”AT"amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
※共同研究グループ
- 理化学研究所 統合生命医科学研究センター
-
- 副センター長 久保 充明(くぼ みちあき)
(旧 統合生命医科学研究センター) - ファーマコゲノミクス研究チーム
チームリーダー 莚田 泰誠(むしろだ たいせい)
(旧 統合生命医科学研究センター ファーマコゲノミクス研究グループ グループディレクター)
- 副センター長 久保 充明(くぼ みちあき)
- ※GENCAT study参加医療機関および代表者(18医療機関、36病院)
- 愛知医科大学
-
- 兼本 浩祐(かねもと こうすけ)、大島 智弘(おおしま ともひろ)
- 岩手医科大学
-
- 武内 克也(たけうち かつや)、大塚 耕太郎(おおつか こうたろう)
- 関西医科大学
-
- 木下 利彦(きのした としひこ)、加藤 正樹(かとう まさき)
- 久留米大学
-
- 石田 重信(いしだ しげのぶ)、安元 眞吾(やすもと しんご)
- 国立精神・神経医療研究センター
-
- 岡崎 光俊(おかざき みつとし)、渡邉 雅子(わたなべ まさこ)
- 産業医科大学
-
- 赤松 直樹(あかまつ なおき)
- 滋賀医科大学
-
- 山田 尚登(やまだ なおと)
- 静岡てんかん・神経医療センター
-
- 高橋 幸利(たかはし ゆきとし)、山本 吉章(やまもと よしあき)
- 順天堂大学
-
- 下 泰司 (しも やすし)
- 徳洲会病院グループ
-
- 亀井 徹正(かめい てつまさ)
- すずかけクリニック
-
- 福智 寿彦(ふくち としひこ)
- 東京女子医科大学 遺伝子医療センター
-
- 斎藤 加代子(さいとう かよこ)
- 名古屋市立大学
-
- 齋藤 伸治(さいとう しんじ)
- 奈良医療センター
-
- 星田 徹 (ほしだ とおる)
- 日本医科大学付属病院
-
- 渡邉 淳(わたなべ あつし)、南 史朗(みなみ しろう)
- 原クリニック
-
- 原 實 (はら みのる)
- 三重大学大学院
-
- 谷井 久志(たにい ひさし)
- むさしの国分寺クリニック
-
- 大沼 悌一(おおぬま ていいち)
- その他の共同研究者氏名
- 杏林大学 医学部
-
- 塩原 哲夫(しおはら てつお)、狩野 葉子(かの ようこ)
- 浜松医科大学 臨床研究管理センター
-
- 古田 隆久(ふるた たかひさ)
- 国立医薬品食品衛生研究所
-
- 斎藤 嘉朗(さいとう よしろう)
- 国立社会保障・人口問題研究所
-
- 泉田 信行(いずみだ のぶゆき)
関連リンク
掲載日 平成30年4月3日
最終更新日 平成30年4月3日


