体の“かたち”づくりに重要なシグナルを発見!
プレスリリース
金沢大学
日本医療研究開発機構
金沢大学ベンチャービジネスラボラトリーの家崎高志博士研究員、金沢大学医薬保健研究域薬学系の金田勝幸教授、檜井栄一准教授らの研究グループは、京都大学ウイルス・再生医科学研究所の大野睦人教授、北畠真助教、金沢医科大学の石垣靖人教授、中京学院大学の眞部孝幸教授らとの共同研究により、私たちの体の“かたち”づくりに重要なシグナルと新しい分子メカニズムを発見しました。
私たちの体は、さまざまな要因が複雑に絡み合って精巧に“かたち”づくられています。骨格はその“かたち”づくりの最も基本的な構造です。骨格の形成に重要なシグナルはこれまでいくつか明らかになっていましたが、ライフスタイルに起因する栄養環境シグナルが、どのように骨格の形成に関与しているかについては明らかになっていませんでした。
本研究グループは、マウスジェネティクス(※1)と生化学的解析を組み合わせることにより、栄養環境シグナルを統合する Mechanistic target of rapamycin(mTOR)(※2)という因子が、骨格の形成に重要な役割を果たしていることを発見し、その詳細な分子メカニズムを明らかにしました。
本成果は、「私たちの体はどのように“かたち”づくられて、どのように維持されているのか」という疑問に対して新たな概念を提供するとともに、“かたち”の形成異常や、その恒常性維持の破綻によって引き起こされるさまざまな骨系統疾患に対する新しい知見と解決法を提供し、アンメット・メディカル・ニーズ(※3)の解消に貢献することが期待されます。
本研究成果は、米国学術雑誌『Stem Cell Reports』に掲載されます。(オンライン版公開日:日本時間 2018年6月29日午前1時)
研究の背景
骨格は、私たちの体の“かたち”づくりの最も基本的な構造です。間葉系幹細胞(※4)の凝集と軟骨細胞の分化は、脊椎や大腿骨などの長管骨の形成においてとても重要な工程です。本研究グループはこれまでに、グルコースやアミノ酸などの栄養環境シグナルが骨格の形成やその恒常性の維持に重要な役割を果たしていることを明らかにしてきました。しかしながら、栄養環境シグナルがどのようにして骨格の形成を調節しているのかについては、ほとんど明らかになっていませんでした。
研究成果の概要
mTORC1は、さまざまなシグナルを統合して細胞機能を調節する働きを持つmTOR複合体です。本研究グループは、栄養環境シグナルによる骨格形成の調節やその恒常性の維持に、mTORシグナルが関与しているかどうかを明らかにすることを試みました。
まず、間葉系前駆細胞特異的なmTORC1不活性化マウスを作製してみたところ、手足がほとんど形成されないという劇的な表現型を示しました(図1(中央)矢印)。さらに、軟骨細胞特異的なmTORC1不活性化マウスを作製してみると、手足の形成不全だけでなく、脊椎の形成異常も確認されました(図1(右)矢印)。このことから、mTORC1シグナルは骨格の形成にとても重要であることが明らかになりました。
次に、「どうしてmTORC1を不活性化すると,手足や脊椎の形成に異常がみられるのか」という疑問を解決することを試みました。そこで、mTORC1不活性化細胞においてさまざまな因子の発現を調べました。その結果,Sox9(※5)のmRNA(※6)発現量には変化はなかったものの、タンパク質の発現量が著しく減少していることが分かりました。さらに詳細な解析を行ったところ,mTORC1不活性化細胞ではポリソーム (※7)においてSox9のRNA量が著しく減少しており、Sox9のRNA翻訳が抑制されていることが分かりました。また、その翻訳制御に4E-BPs(※8)経路が関与していることも明らかになりました(図2)。
以上のことから、栄養環境シグナルを統合するmTORC1シグナルは、4E-BPs経路を介してSox9のRNA翻訳を調節することで、骨格形成に重要な役割を果たしていることが明らかになりました。
研究成果の意義・今後の展開
本研究成果は、軟骨無形成症や脊椎側弯(そくわん)症など、骨格形成の異常やその恒常性維持の破綻によって引き起こされるさまざまな骨系統疾患に対する予防・治療法の開発に新しい知見を提供し、アンメット・メディカル・ニーズの解消に貢献することが期待されます。
参考図
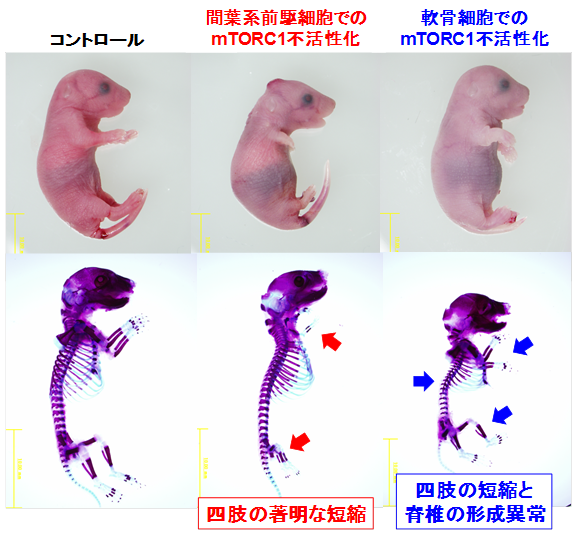
図1 胎生18.5日目の胎児の骨格標本
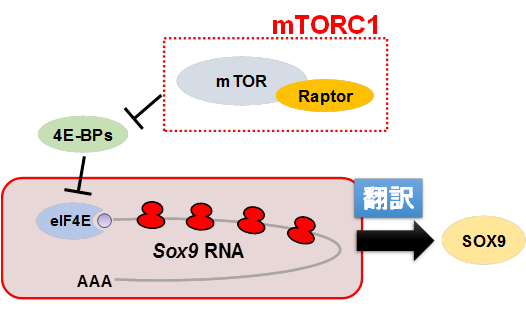
図2 mTORC1/4E-BPs経路によるSox9のRNA翻訳調節
用語解説
- ※1 マウスジェネティクス
- 遺伝子を操作したねずみ(マウス)を用いた実験。
- ※2 Mechanistic target of rapamycin(mTOR)
- 細胞の成長、増殖、生存、分化などのさまざまな機能を調節する酵素。複数のタンパク質による複合体(complex)を形成し、その複合体はmTORCと呼ばれる。
- ※3 アンメット・メディカル・ニーズ
- 未だ有効な治療方法が確立されていない疾病に対する医療への要望。
- ※4 間葉系幹細胞
- 骨、軟骨、脂肪、筋などの細胞に分化する能力を持つ細胞。再生医療への応用が期待されている。
- ※5 Sox9
- Soxと呼ばれる、骨格の形成に中心的な役割を果たしている遺伝子グループの一つ。Sox遺伝子の9番目。
- ※6 mRNA
- たんぱく質に翻訳されうる塩基配列情報と構造を持った分子で、細胞中のタンパク質合成部位であるリボソームにDNAの情報を伝える役割を持つ。分子生物学などでは、mRNAの情報に基づいて、細胞などでタンパク質が合成される反応を「翻訳」という。
- ※7 ポリソーム
- 翻訳の場であるリボソームがmRNAによって複数個つながれたもの。
- ※8 4E-BPs
- 翻訳開始因子であるeIF4Eと複合体を形成することで、翻訳を抑制する機能を持つ。
掲載論文
- 雑誌名:
- Stem Cell Reports
- 論文名:
- Translational control of Sox9 RNA by mTORC1 contributes to skeletogenesis
(mTORC1はSox9のRNA翻訳調節を介して骨格形成を制御する) - 著者名:
- Takashi Iezaki, Tetsuhiro Horie, Kazuya Fukasawa, Makoto Kitabatake, Yuka Nakamura, Gyujin Park, Yuki Onishi, Kakeru Ozaki, Takashi Kanayama, Manami Hiraiwa, Yuka Kitaguchi, Katsuyuki, Kaneda, Takayuki Manabe, Yasuhito Ishigaki, Mutsuhito Ohno and Eiichi Hinoi
(家崎高志、堀江哲寛、深澤和也、北畠真、中村有香、朴奎珍、大西勇気、尾崎翔、金山天志、平岩茉奈美、北口裕香、金田勝幸、眞部孝幸、石垣靖人、大野睦人、檜井栄一)
本研究は、日本学術振興会科研費 基盤研究B(一般)「幹細胞ニッチのmTORシグナルによる造血機能制御:白血病治療展開への基礎研究」(檜井栄一)、基盤研究B(特設)「栄養環境センサーを分子基軸とした脊椎側弯症に対する発症・進行予測技術の開発」(檜井栄一)、新学術領域研究(研究領域提案型)「メカノセンサーとしての間葉系幹細胞」(檜井栄一)、国立研究開発法人日本医療研究開発機構(AMED)難治性疾患実用化研究事業「肋骨異常を伴う先天性側弯症の発症機序の解明」(研究開発代表者:檜井栄一)、京都大学ウイルス感染症・生命科学先端融合的共同研究拠点の支援を受けて行ったものです。
本件に関するお問い合わせ先
研究に関すること
金沢大学 医薬保健研究域薬学系
准教授 檜井 栄一(ひのい えいいち)
TEL:076-234-4472
E-mail:hinoi”AT”p.kanazawa-u.ac.jp
AMEDの事業に関すること
国立研究開発法人日本医療研究開発機構戦略推進部 難病研究課
東京都千代田区大手町1-7-1
TEL:03-6870-2223
E-mail:nambyo-info”AT”amed.go.jp
広報に関すること
金沢大学 総務部広報室戦略企画係
舘 正裕樹(たち まさゆき)
TEL:076-264-5024
E-mail:koho"AT"adm.kanazawa-u.ac.jp
金沢大学 医薬保健系事務部薬学・がん研支援課企画総務係
黒崎 めぐみ(くろさき めぐみ)
TEL:076-234-6822
E-mail:y-somu”AT”adm.kanazawa-u.ac.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
関連リンク
掲載日 平成30年6月29日
最終更新日 平成30年6月29日


