TYK2遺伝子のレアバリアントが関節リウマチ発症を抑制―特定のタンパク質ドメインを標的とした治療法の開発へ―
プレスリリース
理化学研究所
東京大学
日本医療研究開発機構
理化学研究所(理研)生命医科学研究センター基盤技術開発研究チームの茂木朋貴リサーチアソシエイト(研究当時、現 東京大学大学院農学生命科学研究科 特任研究員)、桃沢幸秀チームリーダー、自己免疫疾患研究チームの高地雄太副チームリーダー、東京大学大学院新領域創成科学研究科メディカル情報生命専攻クリニカルシークエンス分野の松田浩一教授らの共同研究グループ※は、日本人約6,000人分のDNAを解析し、アミノ酸変化を伴う低頻度の遺伝子バリアント[1](=レアバリアント[2])がTYK2遺伝子[3]上の特定の領域(ドメイン)に存在している場合に、それが関節リウマチの発症を抑制することを発見しました。
本研究成果は、関節リウマチの発症メカニズムのさらなる解明やTYK2遺伝子ドメインの選択的調節による新たな治療法の開発に貢献すると期待できます。
今回、共同研究グループは、バイオバンク・ジャパン[4]で収集された関節リウマチ患者2,322人とリウマチ患者でない人(対照群)4,517人のDNAを用いて、98遺伝子上にあるレアバリアントの解析を行いました。その結果、TYK2遺伝子上にアミノ酸配列に影響を及ぼすレアバリアントを保有すると2.08倍関節リウマチを発症しにくいこと、これらのレアバリアントはタンパク質機能に関わる二つのドメイン上に特に多く存在することが分かりました。また、これらのドメインの代表的な遺伝子バリアントの機能をそれぞれ調べたところ、異なったサイトカイン[5]シグナルの変化が示されました。これらの結果は、一つの遺伝子であっても特定のドメインについて解析することで、より詳しいメカニズムを明らかにできるとともに、特定のドメインを制御する新たな治療法開発の可能性を提示するものです。
本研究は、英国の科学雑誌『Annals of the Rheumatic Diseases』の掲載に先立ち、オンライン版(5月22日付け)に掲載されました。
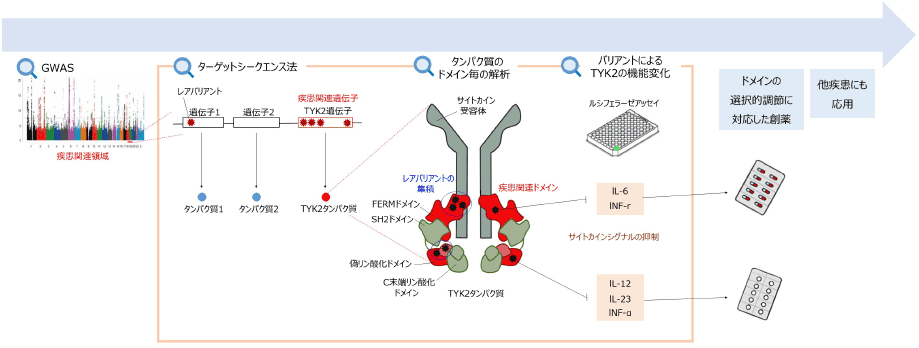
図 今回のレアバリアント探査によって得られたドメインごとの機能の違いと創薬への流れ
※GWASの図は注2より引用図の説明
- *共同研究グループ
- 理化学研究所
- 生命医科学研究センター 基盤技術開発研究チーム
- リサーチアソシエイト(研究当時) 茂木 朋貴(もてぎ ともき)
(現 客員研究員、東京大学大学院 農学生命科学研究科 特任研究員) - チームリーダー 桃沢 幸秀(ももざわ ゆきひで)
- リサーチアソシエイト(研究当時) 茂木 朋貴(もてぎ ともき)
- 自己免疫疾患研究チーム
- 副チームリーダー 高地 雄太(こうち ゆうた)
- チームリーダー 山本 一彦(やまもと かずひこ)
- 生命医科学研究センター
- 副センター長(研究当時) 久保 充明(くぼ みちあき)
- 東京大学大学院 新領域創成科学研究科
- メディカル情報生命専攻 クリニカルシークエンス分野
- 教授 松田 浩一 (まつだ こういち)
※研究支援
本研究は、日本医療研究開発機構(AMED)のオーダーメイド医療の実現プログラム「疾患関連遺伝子等の探索を効率化するための遺伝子多型情報の高度化(研究開発代表者:久保 充明)」の支援のもと行われました。
背景
自己免疫疾患[6]の一つである関節リウマチは、関節の炎症と破壊を生じる疾患で、日本人の約1%が罹患していることが知られています注1)。2003年に生物学的製剤の使用が認可されたことから、この疾患の予後は大きく改善しました。しかし現在の生物学的製剤では治療が困難な場合もあり、より良い治療法を開発するには、発症メカニズムをさらに詳しく調べる必要があります。
関節リウマチでは遺伝的要因が発症に関与することがよく知られており、ゲノムワイド関連解析(GWAS)[7]によって、発症に関わる頻度の高い遺伝子バリアントが100個以上同定されています。この遺伝子バリアントを持つ人は、持たない人に比べ、1.1~1.5倍程度、関節リウマチにかかりやすいことが分かっています注2)。
一方で、人口の5%以下にしか存在しないレアバリアントはGWASでの解析が難しいものの、疾患発症に対してより強い影響を示す可能性があります。このレアバリアントを同定することは、より詳しい発症メカニズム解明の起点となり、新たな治療ターゲットの開発につながると考えられます。
- 注1)
- Hisashi Yamanaka, Naonobu Sugiyama, Eisuke Inoue, Atsuo Taniguchi, Shigeki Momohara., Estimates of the prevalence of and current treatment practices for rheumatoid arthritis in Japan using reimbursement data from health insurance societies and the IORRA cohort (I).Modern Rheumatology2015, 24, 33-40.
- 注2)
- Yukinori Okada, Di Wu, Gosia Trynka, Towfique Raj, Chikashi Terao, Katsunori Ikari, Yuta Kochi, et al., Genetics of rheumatoid arthritis contributes to biology and drug discovery. Nature 2014, 506, 376-381
研究手法と成果
共同研究グループは、バイオバンク・ジャパン(バイオバンク・ジャパンのHP)によって収集された関節リウマチ患者の疾患群2,322人と対照群4,517人のサンプルについて、既に大規模GWASによって関節リウマチ発症との関連が示唆されている98遺伝子の全翻訳領域である176,335塩基を対象に、理研生命医科学研究センター基盤技術開発研究チームが開発したターゲットシークエンス法[8]を用いてレアバリアントの解析を行いました。遺伝子ごとのレアバリアントの割合を調べた結果、対照群ではTYK2遺伝子上にアミノ酸配列に影響を及ぼすレアバリアントが多く保有されており(疾患群:8.3%、対照群:14.0%、P=3.94×10-12)、遺伝子バリアントを持つことで2.08倍関節リウマチを発症しにくいことが分かりました。
さらに、TYK2タンパク質を構成する四つの領域(ドメイン)に着目して解析したところ、FERMドメイン[3]と偽リン酸化ドメイン[3]においても、対照群ではレアバリアントをより多く保有することが明らかとなりました。その割合は、FERMドメインにおいて疾患群の3.2%、対照群で4.8%、偽リン酸化ドメインでは疾患群の4.0%、対照群で7.4%であり(図1)、FERMドメインに遺伝子バリアントがあると1.52倍、偽リン酸化ドメインに遺伝子バリアントがあると1.92倍関節リウマチを発症しにくいことが明らかになりました。
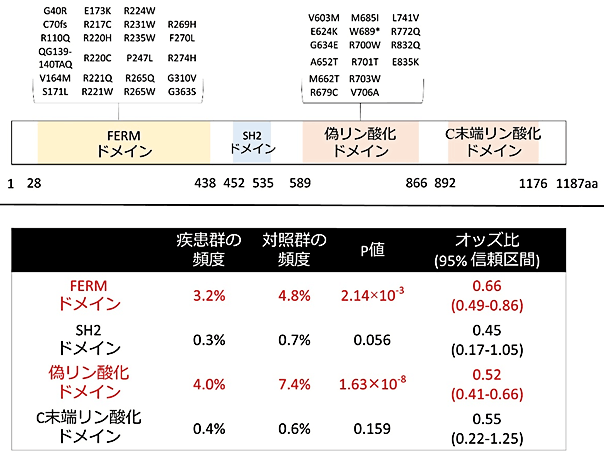
図1 TYK2タンパク質の各ドメインにおける変異とドメインごとのP値およびオッズ比
下段:TYK2におけるレアバリアントの蓄積をドメインごとに解析した表。赤字で示したFERMドメインと偽リン酸化ドメインへ遺伝子バリアントの蓄積が統計的に有意な差が認められた。P値は、偶然にそのようなことが起こる確率のことで、統計学的有意差を示す指標。数値が小さいほど偶然では起こりえないことを表す。オッズ比は、ある事象の起こりやすさについて二つの群で比較したときの違いを示す統計学的尺度の一つ。
次に、これらドメインに存在するレアバリアントが、どのようにTYK2遺伝子の機能に影響を及ぼすのかを評価しました。まず、HepG2とHEK-239FTという細胞株を用いて、これらのTYK2遺伝子に各ドメインの代表的な遺伝子バリアントであるR231W(FERMドメイン)、R703W(偽リン酸化ドメイン)を導入しました。そして、TYK2に作用するサイトカインのシグナル変化を、ルシフェラーゼアッセイ[9]によって測定しました。 その結果、R231Wでは特にインターロイキン-6(IL-6)、インターフェロン-ガンマ(INF-γ)によるシグナル変化が抑制され(図2B,C)、R703WではIL-12、IL-23、INF-αによるシグナル変化が抑制されることが分かりました(図2A, D, E)。これらのタンパク質は炎症に寄与するサイトカイン[5]として知られており、TYK2遺伝子の変異によって関節リウマチの発症が抑制されるのは、これら炎症にかかわるサイトカインシグナルの抑制による可能性が示されました。
また、このメカニズムに関わっているサイトカインシグナルはドメインごとに異なっており、TYK2による関節リウマチ発症の抑制には、INF-αやINF-γIL-6やIL-12、IL-23が強く関わっている可能性が示されました。
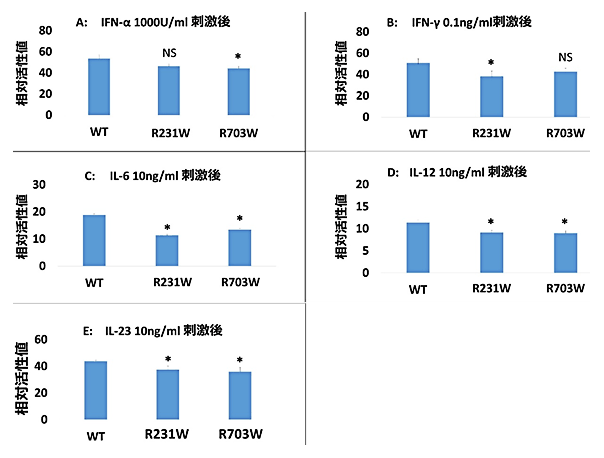
図2 TYK2の各ドメインの遺伝子バリアントによるサイトカイン反応の違い
今後の期待
今回の研究により、TYK2遺伝子上に関節リウマチ発症を抑制するレアバリアントが存在することが明らかとなりました。また、そのレアバリアントは、TYK2タンパク質の特定のドメインに集積しており、これらドメインの選択的調節による新たな関節リウマチの治療法の開発につながる可能性も示しています。
また、本研究で示された手法は、他の疾患でも同様に適用することで、遺伝子内のドメインごとの詳細なメカニズム解明につながる可能性があります。
論文情報
- タイトル
- Identification of rare coding variants in TYK2 protective for rheumatoid arthritis in the Japanese population and their effects on cytokine signaling
- 著者名
- Tomoki Motegi, Yuta Kochi, Koichi Matsuda, Michiaki Kubo, Kazuhiko Yamamoto, Yukihide Momozawa
- 雑誌
- Annals of the Rheumatic Diseases
- DOI
- 10.1136/annrheumdis-2019-215062
補足説明
- [1]遺伝子バリアント
- ヒトゲノムは約30億の塩基対から構成されるが、個々人を比較するとその塩基配列には違いがあり、それを遺伝子バリアントと呼ぶ。遺伝子バリアントにより、病気のかかりやすさや医薬品への反応にも違いが生じる。
- [2]レアバリアント
- 一般人口の約5%未満にしか存在しない遺伝子バリアント。疾患発症に対してより強い影響を与えている可能性があり、研究が進められている。
- [3]TYK2遺伝子、FERMドメイン、偽リン酸化ドメイン
- TYK2は非受容体型チロシンキナーゼの一つで、多くのサイトカインシグナルの伝達に関わる。TYK2の機能を完全に喪失している人は、高IgE症候群という免疫不全症を発症することがある。四つの領域(ドメイン)に分かれており、このうちFERMドメインは受容体との安定的な結合の維持に関わり、偽リン酸化ドメインはリン酸化ドメインの活性化に関与している。
- [4]バイオバンク・ジャパン
- 日本人集団27万人を対象とした、世界最大級の疾患バイオバンク。オーダーメイド医療の実現プログラムを通じて実施され、ゲノムDNAや血清サンプルを臨床情報と共に収集し、研究者へ分譲を行っている。2003年から東京大学医科学研究所内に設置されている。
- [5]サイトカイン、炎症性サイトカイン
- 細胞間での情報交換を担うタンパク質をサイトカインと呼び、サイトカインによって引き起こされるシグナル伝達機構をサイトカインシグナルと呼ぶ。この中で生体内における炎症反応を引き起こすサイトカインを炎症性サイトカインといい、代表的なものにTNF-αやIL-6などがある。
- [6]自己免疫疾患
- 何らかの免疫異常によって自分の体や組織を異物のように認識し、自己抗体や自己に反応するリンパ球を作り、自分の体を攻撃する疾患のこと。代表的なものに関節リウマチがある。
- [7]ゲノムワイド関連解析(GWAS)
- 疾患の感受性遺伝子を見つける代表的な方法。ヒトゲノムを網羅した数100万~1,000万の一塩基多型を対象に、対象サンプル群における疾患との関係を評価できる。2002年に世界で初めて理化学研究所で実施された手法であり、以後世界中で精力的に実施されている。GWASはGenome-Wide Association Studyの略。
- [8]ターゲットシークエンス法
- ゲノムDNAの特定の領域だけを解析する手法。数千人規模の数十遺伝子の解析を高速かつ高精度に行うため、ゲノムの複数の領域を同時に増幅するマルチプレックスポリメラーゼ連鎖反応(PCR:Polymerase Chain Reaction)を応用することで、大規模かつ安価にDNAの配列を決定することができる。
- [9]ルシフェラーゼアッセイ
- 変化を測定したい遺伝子を蛍光を発する遺伝子に置き換えることによって、蛍光の強さから遺伝子の発現状態を高感度で調べられる手法。今回はサイトカインシグナルの応答配列をルシフェラーゼ遺伝子で置き換えることによって、TYK2遺伝子のレアバリアントがどのようにサイトカインシグナルへ影響を与えているのかを調べている。
発表者・機関窓口
発表者
理化学研究所
生命医科学研究センター 基盤技術開発研究チーム
リサーチアソシエイト(研究当時) 茂木 朋貴(もてぎ ともき)
(現 客員研究員、東京大学大学院 農学生命科学研究科 特任研究員)
チームリーダー 桃沢 幸秀(ももざわ ゆきひで)
東京大学大学院 新領域創成科学研究科
メディカル情報生命専攻 クリニカルシークエンス分野
教授 松田 浩一(まつだ こういち)
機関窓口
理化学研究所 広報室 報道担当
TEL:048-467-9272 FAX:048-462-4715
E-mail:ex-press"AT"riken.jp
東京大学大学院新領域創成科学研究科 広報室
TEL:04-7136-5450
E-mail:info"AT"edu.u-tokyo.ac.jp
AMED事業に関するお問い合わせ先
日本医療研究開発機構(AMED)
基盤研究事業部 バイオバンク課
TEl:03-6870-2228
E-mail:order-made"AT"amed.go.jp
※上記の"AT"は@に置き換えてください。
関連リンク
掲載日 令和元年6月13日
最終更新日 令和元年6月13日


