昆虫ホルモンの生合成を撹乱する蚊の発育阻害剤の発見―環境に優しい農薬の開発に向けて―
プレスリリース
国立大学法人筑波大学
学校法人東京薬科大学
国立研究開発法人理化学研究所
国立研究開発法人日本医療研究開発機構
地球上で最も多くのヒトを殺す生物は、蚊です。現在、マラリアやデング熱など、蚊が媒介する重篤な感染症による死者は、世界中で年間70万人にも上ります。これらの感染症に対する防衛策として、蚊を殺したり、あるいは蚊の成長を阻害する薬剤の使用は欠かせません。しかしながら、既存の殺蚊剤に対して抵抗性を示す蚊の出現が確認されています。そのため、単一の薬剤に過剰に頼るのではなく、作用機序の異なる複数の薬剤をローテーションして使用することで、薬剤抵抗性の出現を回避する戦略が不可欠です。
害虫に対する高い殺虫能や成長阻害能を示しながら、昆虫以外の生物に対する作用がない薬剤として、昆虫特有の生命現象を撹乱する「昆虫成長制御剤」があります。その一つとして、昆虫の脱皮と変態を司る昆虫ステロイドホルモン「エクジステロイド」の働きを撹乱する薬剤が注目されています。
本研究チームは、エクジステロイド生合成に必要な酵素「Noppera-bo(略称Nobo)注1)」に焦点を当て、デング熱、黄熱、ジカウイルス感染症を媒介するネッタイシマカ由来のNoppera-boの活性を阻害する薬剤を探索しました。その結果、植物の二次代謝物としてよく知られるフラボノイド化合物であるデスメチルグリシテインが極めて有効であることを発見し、さらにX線結晶構造解析注2)によって分子レベルでの作用機序の解明に成功しました。加えて、デスメチルグリシテインが、ネッタイシマカ幼虫の発育を阻害することも見いだしました。
今回の研究成果により、環境負荷が少なく効果の高い殺蚊剤の開発が期待されます。
研究代表者
東京薬科大学 生命科学部 藤川 雄太 助教
理化学研究所 生命機能科学研究センター 制御分子設計研究チーム 本間 光貴 チームリーダー
研究の背景
国際保健機関(WHO)や国連教育科学文化機関(UNESCO)の推計によると、マラリアやデング熱など、蚊が媒介する重篤な感染症による死者は世界中で年間70万人にも上ります。
蚊によって媒介される感染症に対する防衛策の一つは、殺虫剤の使用です。しかしながら、既存殺蚊剤に対して抵抗性を示す蚊の出現が確認されており、その有効性は永続的ではありません。そのため、単一の薬剤に過剰に頼るのではなく、作用機序の異なる複数の薬剤をローテーションして使用することで、薬剤抵抗性の出現を回避する戦略が不可欠です。それには、化学構造や作用機序が異なる薬剤を、継続的に開発することが求められます。
害虫に対する高い殺虫能や成長阻害能を示しつつ、昆虫以外の生物に対する副作用がない薬剤として、昆虫特有の生命現象を撹乱する「昆虫成長制御剤」があります。その一つとして、昆虫の脱皮と変態を司る昆虫ステロイドホルモン「エクジステロイド」の働きを撹乱する薬剤が古くから注目されています。エクジステロイドの生合成を阻害する方法も考えられますが、その実現のためにはエクジステロイド生合成酵素注3)の同定が必要です。
本研究チームでは、これまでに、Noppera-boと名づけられた生合成酵素(タンパク質)を同定しています(参考図A)。Noboは、進化的に、蚊を含むハエ目昆虫とチョウ目昆虫のみに保存されており、特定の昆虫のみに殺虫効果を示す選択的殺虫剤への応用にも好適と考えられることから、その酵素活性を阻害する薬剤の探索を進めてきました。また、これに伴い、1万種類の化合物を1日で探索できる技術を確立しています。
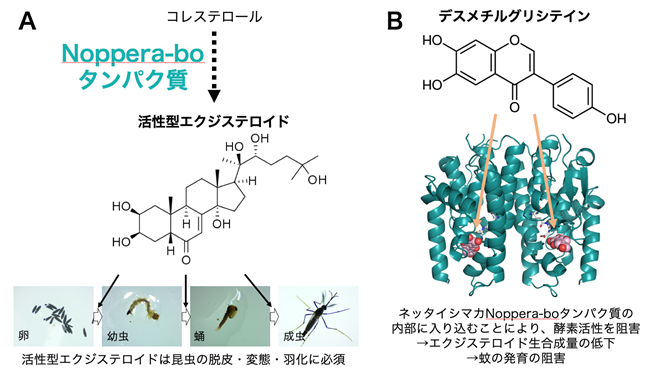
- Noppera-boは、食餌から摂取したコレステロールからエクジステロイドを生合成する過程に関与する。活性型のエクジステロイドや、昆虫の脱皮や変態、そして羽化に必須である。
- 本研究で見出したデスメチルグリシテインというフラボノイド化合物は、ネッタイシマカNoppera-boタンパク質の内部に入り込み、酵素活性を阻害する。その結果、エクジステロイド生合成量が低下し、蚊の発育が阻害されると考えられる。
研究内容と成果
本研究では、デング熱、黄熱、ジカウイルス感染症などを媒介するネッタイシマカのNobo(以下AeNobo)を阻害する化合物を探索しました。上述の探索技術を活用し、東京大学創薬機構が保有する9,600種類の化合物ライブラリーの中からAeNobo阻害活性を網羅的に探索し、植物の二次代謝産物注4)としてよく知られているフラボノイド化合物を同定しました。また、市販品として容易に入手できた複数のフラボノイド化合物についても検討したところ、試験した半数以上のフラボノイド化合物にAeNobo阻害活性が認められました。
次に、高エネルギー加速機研究機構の放射光実験施設フォトンファクトリーを使用したX線結晶構造解析によって、AeNoboタンパク質とフラボノイド化合物が分子レベルでどのように相互作用するのかを検討しました。その結果、試験したフラボノイド化合物のうち、ゲニステイン(genistein)とダイゼイン(daidzein)という2種類について、AeNoboとのタンパク質-分子複合体構造を解明することに成功しました。そして、それらのいずれについても、AeNoboタンパク質を構成するアミノ酸のうち、113番目のアスパラギン酸残基との間で形成される水素結合や、39番目のフェニルアラニン残基との間で形成される分子間の引力が、フラボノイド化合物の阻害活性の発揮に重要であることを見いだしました。これらの相互作用様式は、分子動力学シミュレーション注5)による計算科学手法によっても支持されました。
さらに、AeNoboとの水素結合や引力をより強めることができるフラボノイド化合物を探索したところ、デスメチルグリシテイン(正式名称4′,6,7-トリヒドロキシイソフラボン)という化合物が、非常に強いAeNobo阻害活性を持つことが明らかになりました(参考図B)。これを用いてネッタイシマカの若齢幼虫を処理したところ、0.001%程度という低い濃度でも、幼虫発育を顕著に阻害できる活性があることが分かりました。
ゲニステインやダイゼインに蚊の幼虫に対する発育阻害効果があることは、以前から知られていましたが、その阻害効果がどのような分子メカニズムによってもたらされているのかは、分かっていませんでした。本研究により、その作用機序の一端が初めて解明されました。
なお、ゲニステインやダイゼインは、哺乳類の女性ホルモン様の活性を持っています。女性ホルモン様活性物質は内分泌撹乱物質(いわゆる「環境ホルモン」)になる可能性があるため、殺幼虫活性があったとしても野外に散布することはできません。その点、デスメチルグリシテインは女性ホルモン様活性を持たず、環境調和型昆虫成長制御剤として優れているといえます。
今後の展開
今回、エクジステロイド生合成を阻害する化合物が、ネッタイシマカの幼虫発育を阻害する昆虫成長制御剤となり得ることが初めて示されました。一方で、これらの化合物の活性は、すでに用いられている昆虫成長制御剤や殺蚊剤と比べるとまだ低く、デスメチルグリシテインをベースに、より高い活性を有する化合物の開発や、別の化学構造を持つ高活性化合物の探索を継続する必要があります。本研究チームでは、今後、こうした化合物についても、今回と同様の手法を用いた研究を進める予定であり、これにより、実用的な昆虫成長制御剤の開発につながることが期待されます。
用語解説
- 注1)Noppera-bo
- ハエ目昆虫とチョウ目昆虫で必須の役割を果たすエクジステロイド生合成酵素の一つ。グルタチオンS-転移酵素と呼ばれる一群のタンパク質ファミリーに属する。Noppera-boの名前の由来は、このタンパク質の機能が完全に失われたショウジョウバエでは、本来胚で発達するべき表皮の構造が形成されずに「ツルツル」の見た目になるため。
- 注2)X線結晶構造解析
- 結晶中の原子および分子の配置を決定する解析のこと。結晶にX線ビームを当てた際に生じる回折の情報に基づいて、結晶の構造を決定することができる。生命科学においては、結晶化させたタンパク質をX線結晶構造解析に用いることで、タンパク質の3次元の形状や、タンパク質と低分子化合物との相互作用を分子レベルで解明することができる。
- 注3)生合成酵素
- 生物が、その構成成分となる生体分子を、食物などから得た原材料を元に作り出す過程を「生合成」といい、生合成酵素は、生合成に必要な化学反応を触媒するタンパク質を指す。コレステロールから活性型エクジステロイドを生合成するためには、少なくとも9種類の酵素が必要であると考えられている。
- 注4)二次代謝産物
- 生物の体に存在する物質は、さまざまな化学反応を経て多様な物質へと変化する。この変化の過程を代謝という。生体内の代謝された物質のうち、生物体を構成維持する上で必要な物質を一次代謝産物、生存に必ずしも必須ではない物質を二次代謝産物と呼ぶ。微生物や植物は多様な二次代謝産物を産生することが知られており、これらの中には医薬品をはじめ有益な物質が多くある。
- 注5)分子動力学シミュレーション
- 原子ならびに分子の物理的な動きのコンピューターシミュレーション手法。原子や分子の相互作用を古典力学におけるニュートンの運動方程式を数値的に解析することにより、空間中における原子や分子の位置の時間的変化(動的変化)をシミュレーションすることができる。
研究資金
本研究は、日本医療研究開発機構(AMED)創薬等ライフサイエンス研究支援基盤事業(BINDS)(課題番号JP21am0101071、JP21am0101086、JP21am0101113、JP21am0101114;支援番号1290、2145、2528、2966)、日本学術振興会科学研究費助成事業 挑戦的萌芽研究「エクジステロイド生合成に関わる新規酵素に着目した昆虫発育制御剤スクリーニング戦略」(研究費番号15K14719、研究期間:2015~2017年度)、挑戦的研究(萌芽)「構造生物学的着想に基づく昆虫グルタチオンS-転移酵素Noboの内在性基質の同定」(研究費番号18K19163、研究期間2018~2019年度)、基盤研究(A)「微生物を介した植物の間接誘導防衛機構の解明にもとづく次世代昆虫制御物質の創出」(研究費番号17H01472、研究機関2017~2020年度)、令和3年度群馬大学生体調節研究所・内分泌・代謝学共同研究拠点、文部科学省私立大学研究ブランディング事業、および高エネルギー加速器研究機構大学院生研究フェローシップ(研究期間:2018~2020年度)の支援により実施されました。
掲載論文
- 題名
- Molecular action of larvicidal flavonoids on ecdysteroidogenic glutathione S-transferase Noppera-bo in Aedes aegypt
- (ネッタイシマカのエクジステロイド生合成に関与するグルタチオンS-転移酵素Noppera-boに作用するフラボノイドの殺幼虫活性の分子作用)
- 著者名
- Kazue Inaba(稲葉 和恵、筑波大学 大学院生命環境科学研究科 博士後期課程(当時))、Kana Ebihara(海老原 佳奈、筑波大学 大学院理工情報生命学術院 博士後期課程)、Miki Senda(千田 美紀、高エネルギー加速器研究 機構物質科学研究所 助教)、Ryunosuke Yoshino(吉野 龍ノ介、筑波大学 医学医療系 助教)、Chisako Sakuma(佐久間知佐子、東京慈恵会医科大学 医学部 助教)、Kotaro Koiwai(小祝 孝太郎、高エネルギー加速器研究 機構物質科学研究所 研究員(当時))、Daisuke Takaya(髙谷 大輔、理化学研究所 生命機能科学研究センター 研究員)、Chiduru Watanabe(渡邉 千鶴、理化学研究所 生命機能科学研究センター 研究員)、Akira Watanabe(渡邊 瑛、筑波大学 大学院理工情報生命学術院 修士課程)、Yusuke Kawashima(川嶋 裕介、星薬科大学 薬学部 特任助手(当時))、Kaori Fukuzawa(福澤 薫、星薬科大学 薬学部 准教授)、Riyo Imamura(今村 理世、東京大学 創薬機構 特任講師)、Hirotatsu Kojima(小島 宏建、東京大学 創薬機構 特任教授)、Takayoshi Okabe(岡部 隆義、東京大学 創薬機構 特任教授)、Nozomi Uemura(上村 望、国立感染症研究所 昆虫医科学部 研究員)、Shinji Kasai(葛西 真治、国立感染症研究所 昆虫医科学部 部長)、Hirotaka Kanuka(嘉糠 洋陸、東京慈恵会医科大学 医学部 教授)、Takashi Nishimura(西村 隆史、群馬大学 生体調節研究所 教授)、Kodai Watanabe(渡邉幸大、東京薬科大学 生命科学部 修士課程(当時))、Hideshi Inoue(井上 英史、東京薬科大学 生命科学部 教授)、Yuuta Fujikawa(藤川 雄太、東京薬科大学 生命科学部 助教)、Teruki Honma(本間 光貴、理化学研究所 生命機能科学研究センター チームリーダー)、Takatsugu Hirokawa(広川 貴次、筑波大学 医学医療系 教授)、Toshiya Senda(千田 俊哉、高エネルギー加速器研究機構物質科学研究所 教授)、Ryusuke Niwa(丹羽 隆介、筑波大学 生存ダイナミクス研究センター 教授、高エネルギー加速器研究機構 物質科学研究所 客員教授)
- 掲載誌
- BMC Biology
- 掲載日
- 2022年2月17日
- DOI
- 10.1186/s12915-022-01233-2
お問合わせ先
研究に関すること
丹羽 隆介(にわ りゅうすけ)
筑波大学 生存ダイナミクス研究センター 教授
TEL:029-853-7342
E-mail:ryusuke-niwa"AT"umin.ac.jp
Niwa Lab Tsukuba
取材・報道に関すること
筑波大学広報室
TEL:029-853-2040
E-mail:kohositu"AT"un.tsukuba.ac.jp
東京薬科大学広報課
TEL:042-676-6711
E-mail:kouhouka"AT"toyaku.ac.jp
理化学研究所広報室 報道担当
E-mail:ex-press"AT"riken.jp
AMED事業に関すること
日本医療研究開発機構(AMED)
創薬等ライフサイエンス研究支援基盤事業(BINDS)
創薬事業部 医薬品研究開発課
TEL:03-6870-2219
E-mail:20-DDLSG-16"AT"amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
関連リンク
掲載日 令和4年2月17日
最終更新日 令和4年2月17日


