発症早期の筋萎縮性側索硬化症(ALS)患者さんを対象とした高用量メチルコバラミン第3相試験(JETALS)のご報告―症状の進行抑制効果が示されました―
プレスリリース
徳島大学
日本医療研究開発機構
報道概要
徳島大学 梶龍兒特命教授(主任研究者)、徳島大学大学院医歯薬学研究部医学域臨床神経科学分野 和泉唯信教授(治験調整医師)らの研究チームは、発症早期の筋萎縮性側索硬化症(ALS)の患者に対する高用量メチルコバラミンの有効性、安全性を検証する目的で「高用量メチルコバラミンの筋萎縮性側索硬化症に対する第Ⅲ相試験-医師主導治験-」(Japan Early-stage Trial of Ultrahigh-Dose Methylcobalamin for ALS: 以下、JETALS)を行いました。本治験は徳島大学病院、千葉大学医学部附属病院脳神経内科(桑原聡教授:治験調整医師)など全国25施設で実施されました。
活性型ビタミンB12であるメチルコバラミンは、基礎研究において高用量を投与することによりALSに対して神経保護的な作用を持つことが知られていました。2006年から2014年にエーザイ社が実施した発症3年以内のALS患者を対象に実施された第Ⅱ/Ⅲ相試験では、全登録者を対象とした評価においては主要評価項目に対するメチルコバラミンの有効性を示すことができませんでしたが、発症から1年未満に治験登録された被験者を対象とした評価においては、メチルコバラミン50mgの週2回筋肉内投与は、プラセボ注1と比較して有意に生存期間を約600日も延長、症状の進行を抑制する効果が示唆されていました(部分解析注2)。
第Ⅱ/Ⅲ相試験の部分解析で得られた結果を再検証するため、2017年より発症1年未満のALS患者を対象にJETALSを開始しました。本治験では、第Ⅱ/Ⅲ相試験の部分解析と同様に、メチルコバラミン50mgはプラセボと比較して有意に症状の進行を抑制し、発症早期ALS患者に対する高用量メチルコバラミンの有効性、安全性が改めて確認されました。
これまでの治療薬として、症状の進行に対する抑制効果は明確でないものの生存期間を約90日延長するリルゾール(経口薬)と、経過中の機能評価スケールを改善するものの生存期間への影響は確定していないエダラボン(点滴注射薬)がありましたが、高用量メチルコバラミンは、これまでに実施された臨床試験の結果から発症早期のALS患者においてリルゾールよりも長い生存期間の延長が期待され、エダラボンよりも大きな症状の進行抑制効果が示された画期的な治療法として、今後の保険収載が期待されます。
背景
ALSは、運動ニューロン注3が変性して筋萎縮と筋力低下を来す進行性の疾患で、個人差はあるものの発症後2~5年で死亡または人工呼吸器の装着に至ります。これまでにリルゾール(経口薬)、エダラボン(点滴注射薬)が保険収載されていますが効果は限定的であり、新たな治療薬の開発が求められています。
活性型ビタミンB12であるメチルコバラミンは、低用量において「末梢性神経障害」と「ビタミンB12欠乏による巨赤芽球性貧血」に対して保険適用されている薬剤です。研究チームは基礎研究において高用量メチルコバラミンに神経保護作用があることを見出し、少数の患者による臨床研究で、高用量メチルコバラミンが神経伝導検査における複合筋活動電位を改善させることを確認しました。この結果をもとにエーザイ社が発症3年未満のALS患者を対象とした第Ⅱ/Ⅲ相試験を全国51施設で実施し、373人のALS患者(プラセボ群 124例、メチルコバラミン 25mg群 124例及び50mg群 125例)に対して、最長182週にわたり治験薬の週2回筋肉内投与を実施しました。結果として、主要評価項目であるイベント(非侵襲的呼吸補助装置の終日装着、侵襲的呼吸補助装置の装着又は死亡)の発生率50%までの期間、治療開始から182週までのALSFRS-R注4の合計点数の変化量において、25mg群及び50mg群はプラセボ群を上回る傾向は認められたものの、優越性を示すことができませんでした。しかし、ALS発症から治験開始日までの期間が1年未満の部分集団(プラセボ群 48例,25mg群 54例及び50mg群 42例)では、50mg群はプラセボ群と比較してイベント発生までの期間を約600日延長し、治療16週時点でALSFRS-R合計点数の低下を約45%抑制する結果が得られました。
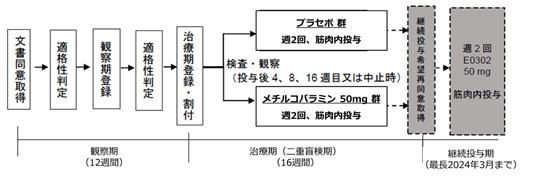
第Ⅱ/Ⅲ相試験の部分解析において、発症早期のALS患者に対する高用量メチルコバラミンの生存期間延長効果と進行抑制効果が示唆されたため、我々は発症1年未満のALS患者を対象として高用量メチルコバラミンの有効性・安全性を再検証するため、上述のJETALSを新たに計画しました。JETALSは多施設共同、ランダム化、プラセボ対照、二重盲検並行群間比較試験であり、2017年11月より全国25施設で実施されました(図1、2)。本治験では発症早期のALS患者を効率的に組み入れるため、診断基準として従来の改訂El Escorial基準よりも診断感度に優れたupdated Awaji基準(2007年に徳島大学が提唱したAwaji基準の改定版)を世界で初めて採用しました。主要評価項目は治療開始から16週までのALSFRS-R合計点数の変化量であり、被験者は16週間にわたり週2回、治験薬(プラセボまたはメチルコバラミン50mg)の筋肉内投与を受けました。

研究結果
治験開始から約2年間で目標の128例を上回る130例が登録され、このうち129例(プラセボ群 64例,メチルコバラミン群 65例)が解析対象となり、126例(プラセボ群 63例、メチルコバラミン群 63例)が16週間の治療期間を完了しました。
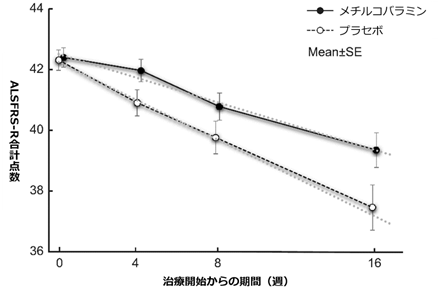
結果として、高用量メチルコバラミンはプラセボと比較し、治療16週時点でALSFRS-R合計点数の低下を約43%抑制する効果を示しました(図3)。この結果は第Ⅱ/Ⅲ相試験の部分解析結果と同様であり、発症早期ALS患者に対する高用量メチルコバラミンの有効性が再現されました。また、本研究の被験者の約90%はリルゾールを併用しており、リルゾール単独治療とリルゾールと高用量メチルコバラミンの併用療法の比較では、併用治療で有意に症状進行が抑制されていることがわかりました。
安全性について、有害事象注5およびの副作用注6の発生率はメチルコバラミン群で約62%、約8%、プラセボ群で約66%、約2%であり、両群に差はなく、高用量メチルコバラミンの高い安全性が確認されました。
まとめ
本研究において発症早期のALS患者に対して、高用量メチルコバラミンは高い有効性、安全性、忍容性を持つことがわかりました。以上の結果は国際的に著名な科学雑誌JAMA Neurologyに掲載されました。
論文情報
- 掲載誌
- JAMA Neurology
- タイトル
- Efficacy and Safety of Ultra-High Dose Methylcobalamin in Early-Stage Amyotrophic Lateral Sclerosis: A Randomized Clinical Trial
- 著者名
- Ryosuke Oki, Yuishin Izumi*, Koji Fujita, Ryosuke Miyamoto, Hiroyuki Nodera, Yasutaka Sato, Satoshi Sakaguchi, Hiroshi Nokihara, Kazuaki Kanai, Taiji Tsunemi, Nobutaka Hattori, Yuki Hatanaka, Masahiro Sonoo, Naoki Atsuta, Gen Sobue, Toshio Shimizu, Kazumoto Shibuya, Ken Ikeda, Osamu Kano, Kazuto Nishinaka, Yasuhiro Kojima, Masaya Oda, Kiyonobu Komai, Hitoshi Kikuchi, Nobuo Kohara, Makoto Urushitani, Yoshiaki Nakayama, Hidefumi Ito, Makiko Nagai, Kazutoshi Nishiyama, Daisuke Kuzume, Shun Shimohama, Takayoshi Shimohata, Koji Abe, Tomohiko Ishihara, Osamu Onodera, Sagiri Isose, Nobuyuki Araki, Mitsuya Morita, Kazuyuki Noda, Tatsushi Toda, Hirofumi Maruyama, Hirokazu Furuya, Satoshi Teramukai, Tatsuo Kagimura, Kensuke Noma, Hiroaki Yanagawa, Satoshi Kuwabara, Ryuji Kaji, for JETALS collaborators.
- (*責任著者)
- DOI
- 10.1001/jamaneurol.2022.0901
本研究への支援
本研究は、下記機関より支援を受けて実施されました。
- 日本医療研究開発機構(AMED)難治性疾患実用化研究事業の研究課題「大量メチルコバラミン筋注によるALSの治療薬開発研究」(主任研究者 梶龍兒;2017~2020年度)
- 厚生労働科学研究費補助金 難治性疾患等政策研究事業(難治性疾患政策研究事業)「神経変性疾患領域における基盤的調査研究班」(研究代表者 中島健二)(2017年度~)
- エーザイ株式会社(2017~2019年度:治験薬提供、2020年度~:治験薬提供、研究費助成)
用語説明
- (注1)プラセボ
- メチルコバラミンと見た目の区別はつかないが、有効成分であるメチルコバラミンが含まれていないもの。
- (注2)部分解析
- 治験の全参加者うち、男女別、年齢階級別、重症度別など、特定の解析対象の集団を抜き出して層別し、その集団での治療効果や安全性などを解析すること。
- (注3)運動ニューロン
- 身体の筋肉を動かすための神経細胞。
- (注4)ALSFRS-R
- ALS機能評価スケール改訂版(ALS functional rating scale-revised)の略号で国際的に用いられている。ALS患者の日常生活を評価する尺度であり、スコアは48点満点で、重症であるほど点数が低い。
- (注5)有害事象
- 薬を投与された患者に生じたあらゆる好ましくない徴候、症状、または病気。
- (注6)副作用
- 薬によって患者に生じた好ましくない徴候、症状、または病気。
お問い合わせ先
研究成果(治験)に関する問合せ先
徳島大学病院治験調整事務局
TEL:088-633-9658
E-mail:chousei763"AT"umin.ac.jp
報道に関する問合せ先
徳島大学蔵本事務部医学部総務課総務係
TEL:088-633-9116
E-mail:isysoumu1k"AT"tokushima-u.ac.jp
AMED事業に関する問合せ先
日本医療研究開発機構
創薬事業部創薬企画・評価課
難治性疾患実用化研究事業担当
TEL:03-6870-2226
E-mail:nambyo-r"AT"amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
関連リンク
掲載日 令和4年5月10日
最終更新日 令和4年5月10日


