リキッドバイオプシーによる脳腫瘍の診断モデルを作成―脳腫瘍の早期発見・早期治療への介入による予後の改善に期待―
成果情報
国立研究開発法人国立がん研究センター
学校法人東京医科大学
国立研究開発法人日本医療研究開発機構
脳腫瘍1)は脳に発生する原発性脳腫瘍と他部位のがんの脳転移による転移性脳腫瘍に分類されます。原発性脳腫瘍は約150種類に分類され、悪性脳腫瘍として悪性神経膠腫(グリオーマ)、中枢神経系原発悪性リンパ腫、良性脳腫瘍として髄膜腫、神経鞘腫が代表的な原発性脳腫瘍となります。また、悪性神経膠腫の中で最も悪性度の高い膠芽腫は、手術に加えて放射線治療と化学療法を行っても1.5~2年で半数の患者が命を落とす非常に予後の悪い病気です。
脳腫瘍は無症状の状態で発見されることは少なく、多くの場合は手足の動きにくさ、言葉のしゃべりにくさ、ふらつき、けいれん発作などの神経症状を契機に、CTやMRIなどの画像検査で診断されます。そのため診断された時点で既に腫瘍が進行していることが多く、脳腫瘍の早期発見が可能な簡便かつ有用な診断マーカーの開発は、脳腫瘍の治療成績や神経症状の改善に急務の課題です。また、脳腫瘍は脳内に発生するため手術による摘出がリスクを伴う場合もあり、血液を用いた診断ができると、手術を回避し速やかに放射線治療や化学療法を開始できるメリットがあります。
国立研究開発法人国立がん研究センター(理事長:中釜 斉、東京都中央区)と東京医科大学(学長:林 由起子/東京都新宿区)の研究チームは、通常はCTやMRIなどの画像検査で診断される脳腫瘍について、血液を用いたリキッドバイオプシー2)による診断モデルの作成に成功しました。血液を用いて簡便かつ高い精度で脳腫瘍を診断できると、健康診断などで脳腫瘍を早期に発見することができ、その結果、早期治療の開始につながり予後の改善が期待できます。
本研究では、脳腫瘍の中でも発生頻度が高い悪性神経膠腫(こうしゅ)(グリオーマ)をはじめとするさまざまな脳腫瘍について、血液(血清)中のマイクロRNA3)を用いて高い精度(感度95%、特異度4)97%)で鑑別する診断モデルを作成しました。更に、悪性脳腫瘍の中でも類似の画像所見を呈することがある膠芽腫(こうがしゅ)、転移性脳腫瘍、中枢神経系原発悪性リンパ腫についても診断モデルの作成を試み、血液による診断の可能性が示唆されました。
通常は画像検査で診断される悪性脳腫瘍が微量な血液検査で診断できる可能性を示した点で、本研究は大きな意義があると考えます。更に精度をあげて、血液検査で悪性脳腫瘍の診断ができるようになれば、脳腫瘍の早期発見や、リスクがある脳外科手術を行わなくても放射線治療や抗がん剤治療を速やかに開始することができます。今後更に検証を重ねて、悪性脳腫瘍の早期発見と治療成績の向上に寄与することが期待されます。
本研究は、国立研究開発法人日本医療研究開発機構の次世代治療・診断実現のための創薬基盤技術開発事業「体液中マイクロRNA測定技術基盤開発プロジェクト」の支援を受け行ったものであり、研究成果は米国医師会雑誌(JAMA)系列のオープンアクセスジャーナル「JAMA Network Open」に12月6日(米国中部時間)付で掲載されました。
研究開発のポイント
- 過去最多の数で脳腫瘍を有する方と有さない方(脳腫瘍266例、対象314例)について、血液(血清)中のマイクロRNAの網羅的な解析を行った。
- 発生頻度が高い悪性神経膠腫(こうしゅ)の患者で有意に変化する複数のマイクロRNAを同定し、それらの組み合わせにより悪性神経膠腫を含むさまざまな脳腫瘍を、血液により高精度に検出できる診断モデルの作成に成功した。
- 類似した画像所見を呈する膠芽(こうが)腫、転移性脳腫瘍、中枢神経系原発悪性リンパ腫を鑑別するマイクロRNAによる診断モデルを作成し、血液による診断の可能性を示した。
- 脳腫瘍の診断に向けた血液スクリーニングの実現は、脳腫瘍の早期発見・早期治療への介入による予後の改善が期待できるとともに、リキッドバイオプシーを用いた低侵襲な脳腫瘍の診断や治療効果のモニタリングの実現に大きな前進をもたらす成果である。
研究概要
本研究では、脳腫瘍を有する方266例と有さない方314例、計580例の血液(血清)中のマイクロRNAを網羅的に解析しました。特に発生頻度が高い悪性神経膠腫の鑑別を目指すため、悪性神経膠腫157例、悪性神経膠腫以外の脳腫瘍109例に分けて解析しました。
その結果、悪性神経膠腫で有意に変化する複数のマイクロRNAを同定し、そのうち3種のマイクロRNAを組み合わせることで悪性神経膠腫を判別できる判別式(グリオーマ判別式:「Glioma Index」)を作成しました。
解析対象例を探索群と検証群の2つに分け、このグリオーマ判別式の精度を検証した結果、悪性神経膠腫の患者全体の95%を正しくがんであると判別することができ(図1)、診断精度が極めて高い(感度95%、特異度97%)診断モデルの作成に成功したことを確認しました。
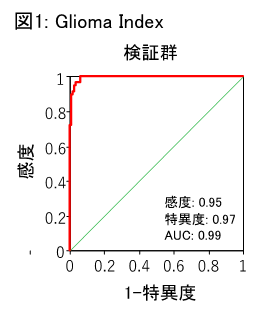
また、悪性神経膠腫の組織型と悪性度(グレード)別の検証においても、グレードII星細胞腫(せいさいぼうしゅ)100%、グレードII乏突起膠腫100%, グレードIII星細胞腫 90%, グレードII乏突起(ぼうとっき)膠腫(こうしゅ)100%, 膠芽腫(こうがしゅ)93%の患者群を陽性と診断でき、グレードIIの患者群においても高い精度で陽性と診断することができました(図2)。
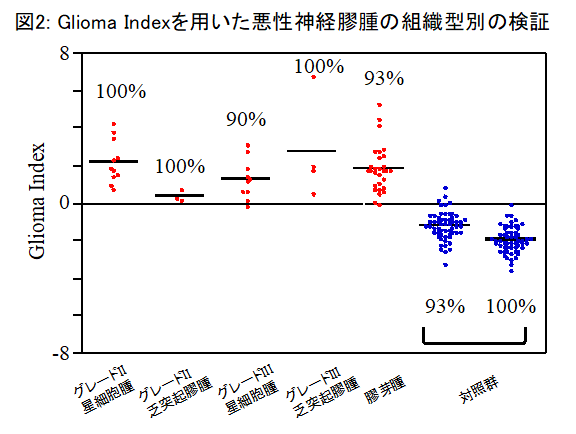
更に、このグリオーマ判別式は悪性神経膠腫以外の脳腫瘍109例の検証において、上衣腫(じょういしゅ)・毛様(もうよう)細胞性星細胞腫(さいぼうせいせいさいぼうしゅ)などの腫瘍100%、中枢神経系原発悪性リンパ腫93%、転移性脳腫瘍89%、髄膜腫・神経鞘腫(しょうしゅ)91%、頭部外傷・脳梗塞100%の患者群を陽性と診断する一方で、2例の脊髄の神経鞘腫はいずれも陰性と診断し、このグリオーマ判別式は悪性神経膠腫を含む脳腫瘍の診断に役立つ可能性が考えられました(図3)。
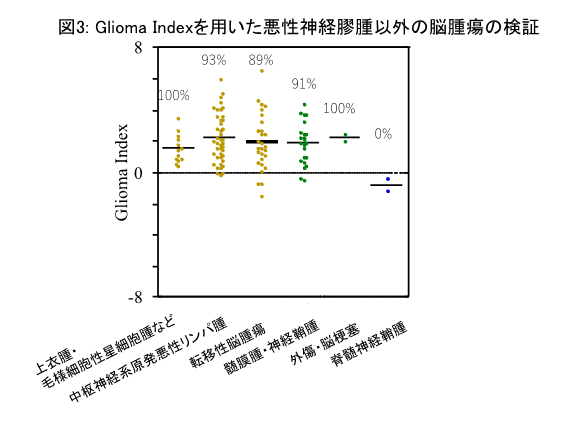
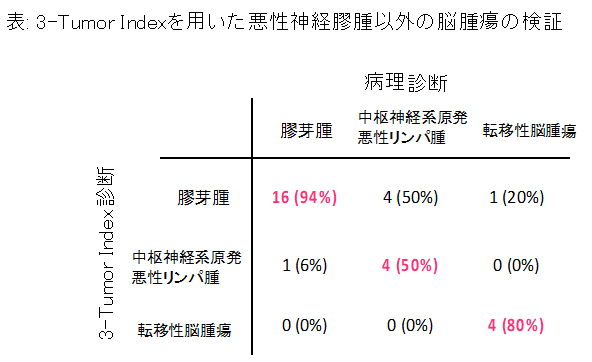
次に、膠芽腫、中枢神経系原発悪性リンパ腫、転移性脳腫瘍は頻度の高い脳腫瘍であり、画像所見からは時々この3つの腫瘍の区別がつきにくい場合があるため、グリオーマ判別式と同様の統計学的手法を用いてこの3種類の腫瘍を判別するマイクロRNAの組み合わせ判別式(3種類の脳腫瘍の判別式:「3-Tumor Index」)を作成しました。組み合わせ判別式は48種類のマイクロRNAで構成され、解析対象例を探索群と検証群の2つに分け精度を検証した結果、同モデルは膠芽腫の94%、中枢神経系原発悪性リンパ腫の50%、転移性脳腫瘍の80%を正しく判別しました。この結果により、中枢神経系原発悪性リンパ腫の診断精度は低いものの、膠芽腫や転移性脳腫瘍はマイクロRNAを用いて診断できる可能性が示されました(表)。
今後の展望
本研究により作成された血液を用いたリキッドバイオプシーの診断モデルは、過去に類を見ない極めて高い診断精度であり、かつその精度を血液からの情報のみで実現できたことは、大変意義の大きい成果です。今後、本研究成果を前向きの臨床研究で更に検証および最適化を重ねることで、脳腫瘍の早期診断の確立に向けて大きな前進が期待できます。
用語解説
- 1)脳腫瘍
- 脳腫瘍分類等については、下記「国立研究開発法人国立がん研究センター 希少がんセンター」のウェブページを参照ください。
- 2)リキッドバイオプシー
- 血液などの体液サンプルを使って診断や治療効果予測を行う技術。
- 3)マイクロRNA
- microRNA(miRNA)は21-25塩基(nt)長の1本鎖RNA分子であり真核生物において遺伝子の転写後発現調節に関与する。 ヒトゲノムには1000以上のmiRNAがコードされていると考えられている。
- 4)感度、特異度
- 感度と特異度は、診断技術の信頼性を示す指標で、病気に罹っている人を検査したとき正しく病気と判定する(陽性)確率を感度、逆に、特定の病気に罹っていない人を検査したとき正しく病気でないと判定する(陰性)確率を特異度と呼ぶ。陽性判定のしきい値を下げれば検査の感度を上げ患者の発見率を高めることができるが、その場合、特異度は下がり正常の方を患者と誤る偽陽性が増えることになる。一方、陽性判定のしきい値を上げれば検査の感度を下げ、患者の発見率は下がり、患者を正常の方と誤る偽陰性が増えることになる。正確な診断を実現するには、特異度を高く維持したまま感度を高める技術革新が必要となる。
共同研究者
本研究は、以下の施設を含む、研究グループによる取り組みの成果です。また、研究に使用した血清は、国立がん研究センターバイオバンク、横浜みのるクリニック等から提供いただきました。試料提供にご協力・ご賛同してくださった患者・家族の皆様へも深く御礼を申し上げます。引き続き、生体試料を用いた研究に対するご理解とご支援をお願いいたします。
- 国立がん研究センター
中央病院 脳脊髄腫瘍科 医員 大野 誠 (筆頭著者)
中央病院 消化管内科 医長、バイオバンク・トランスレーショナルリサーチ支援室 室長 加藤健
研究所 特任研究員 松崎潤太郎 - 東京医科大学 医学総合研究所 分子細胞治療部門 教授 落谷孝広(責任著者)
- 横浜みのるクリニック
- 東レ株式会社
- 株式会社ダイナコム
発表論文
- 雑誌名:
- JAMA Network Open
- タイトル:
- Assessment of the Diagnostic Utility of Serum MicroRNA Classification in Patients with Diffuse Glioma
- 著者:
- Makoto Ohno, Juntaro Matsuzaki, Junpei Kawauchi, Yoshiaki Aoki, Junichiro Miura, Satoko Takizawa, Ken Kato, Hiromi Sakamoto, Yuko Matsushita, Masamichi Takahashi, Yasuji Miyakita, Koichi Ichimura, Yoshitaka Narita, Takahiro Ochiya
- URL:
- https://jamanetwork.com/journals/jamanetworkopen/fullarticle/2757252
お問い合わせ先
内容に関するお問い合わせ
国立研究開発法人国立がん研究センター
企画戦略局 広報企画室
電話番号:03-3542-2511(代表) FAX:03-3542-2545
Eメール:ncc-admin“AT”ncc.go.jp
学校法人東京医科大学
総務部 広報・社会連携推進課
電話番号:03-3351-6141(代表) FAX:03-6302-0289
Eメール:d-koho“AT”tokyo-med.ac.jp
AMEDの事業に関するお問い合わせ
国立研究開発法人日本医療研究開発機構
創薬戦略部 医薬品研究課
次世代治療・診断実現のための創薬基盤技術開発事業担当
〒100-0004 東京都千代田区大手町1-7-1
電話番号:03-6870-2219 FAX:03-6870-2244
Eメール:jisedai-med“AT”amed.go.jp
※Eメールは上記アドレス“AT”の部分を@に変えてください。
関連リンク
掲載日 令和2年1月27日
最終更新日 令和2年1月27日


