非侵襲力測定法が明らかにした分子モーターの協同輸送?神経疾患研究の新しい測定法として期待?
プレスリリース
国立大学法人 東北大学大学院工学研究科
国立大学法人 東北大学学際科学フロンティア研究所
国立研究開発法人 日本医療研究開発機構
発表のポイント
- 神経細胞内で、物質は小胞にパッキングされ分子モーターによって運ばれるが、物質輸送の障害はアルツハイマー病などの神経疾患の原因になる。
- 小胞に働く力を非侵襲に測定した結果、お神輿を大勢で運ぶように、1つの小胞は複数の分子モーターに協同で運ばれることが分かった。
- 非侵襲力測定注1により、小胞輸送を担う分子モーターの減少がシナプス形成の異常に繋がることを突き止めた。
- 非侵襲力測定は神経変性疾患の物理的原因を探る新しいツールである。
概要
神経細胞内で物質は小胞にパッキングされ、分子モーターによって輸送されます。人手不足による宅配便の停滞が社会問題であるのと同様に、私たちの体内でも分子モーターの障害による小胞の輸送停滞はアルツハイマー病などの神経疾患の原因になります。東北大学大学院工学研究科の林久美子助教、東北大学学際科学フロンティア研究所の丹羽伸介助教らは、細胞を傷つけない非侵襲力測定法(図1)を用いて、生きている線虫内で小胞(シナプスの材料)に働く力を見積もることに成功しました。その結果、お神輿を大勢で運ぶように、1つの小胞を複数の分子モーターが協同で運ぶこと(図2)、運び手である分子モーターの減少が輸送力を弱め(図3)シナプス形成の異常に繋がることを突き止めました。非侵襲力測定法は神経疾患研究の新しいツールとして期待されています。
この成果は2018年1月19日16時(日本時間)以降に英国王立化学会が発行する学術誌PCCP(Physical Chemistry Chemical Physics)のオンライン版で公開されました。
研究内容
私たちの体を構成している細胞の中では、人間社会のように様々なタンパク質が役割分担して働いています。例えば細胞内は道路である微小管が張り巡らされ交通網が発達しており、物質は小胞としてパッキングされ、宅配便役のキネシンやダイニンといった分子モーターに輸送されています。特に神経細胞の長い軸索ではさながら高速道路のように宅急便が行き交っています。
人手不足による宅配便の停滞が社会問題であるのと同様に、運び手である分子モーターの障害はアルツハイマー病、パーキンソン病、ハンチントン病といった様々な神経疾患の原因になります。小胞輸送の計測はこれらの疾患の理解や新しい治療法の開発に必須の技術ですが、傷つきやすく複雑な環境を持つ細胞内では力測定などの物理計測が困難であるため、小胞輸送の計測は進んでおらず、細胞を傷つけない非侵襲な細胞内の力測定技術が必要とされてきました。特に細胞の力刺激や力学応答を研究対象とするメカノバイオロジーという分野でこのような技術が研究されています。
溶媒中で小さな粒子は熱ゆらぎ等の効果でゆらぎます。物理法則から、このようなゆらぐ運動はエネルギーと関係します。林助教らはこの物理法則に着目し小胞に働く力を小胞の重心位置のゆらぐ運動から見積もることに成功しました(図1, 参考情報1)。
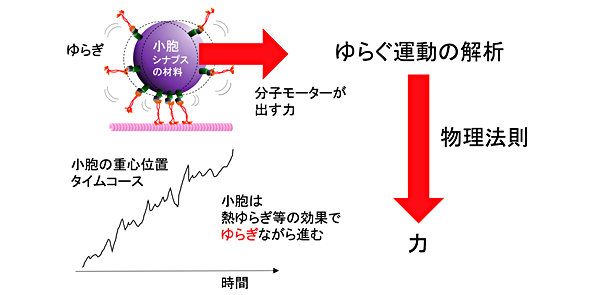
図1:ゆらぎを利用した非侵襲な力測定法(参考情報1)の概念図
細胞に外力を印加する侵襲測定と異なり、ゆらぎは小胞の蛍光イメージングから非侵襲に得られます。小胞のゆらぎ測定の結果、力分布に複数のピークが現れ、これは小胞輸送に複数の力発生ユニットが存在することを意味します。力発生は分子モーターが行うので、小胞は複数の分子モーターに協同で輸送されていることになります。人間社会でも大きな神輿は大勢で運びますが、同様に、神経細胞では1つの小胞を複数の分子モーターが協同で運ぶことで安定した効率の良い輸送を実現していると考えられます(図2)。
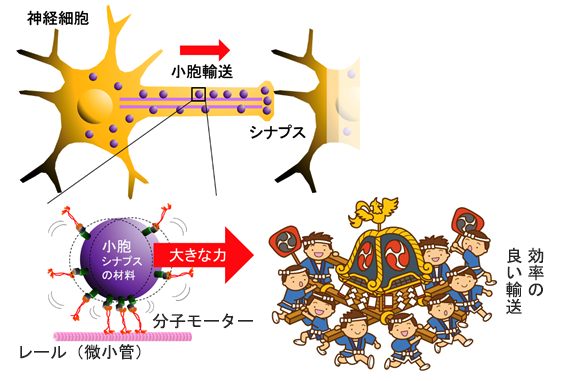
図2:神経細胞内で、複数の分子モーターによる小胞の協同輸送が、安定で効率の良い輸送を実現する。
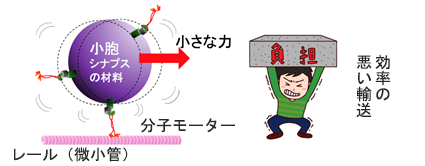
図3:分子モーターの減少による輸送力の低下
非侵襲性が特徴である「ゆらぎによる力測定法」は生きたままの個体に用いることが可能です。林助教と丹羽助教らは、この力測定法を生きている線虫内のシナプス形成位置の異常の解明に役立てました。シナプス形成の異常はアルツハイマー病の発症に密接に関係しています。以前の研究でARL-8というタンパク質が神経細胞においてシナプスの材料の輸送を制御していることが報告されていたが(参考情報2)、ARL-8が分子モーターに及ぼす影響を直接測定することは出来ませんでした。今回の測定の結果、ARL-8欠損線虫でシナプスの材料を運ぶ分子モーター数が減少したことを突き止めました(図4)。ARL-8欠損によるシナプス形成位置の変化という神経科学的な問題を力や分子モーター数などの物理的パラメータから定量的に議論することが可能になりました。
神経疾患で原因タンパク質の同定が進む中、小胞輸送障害の物理的原因はあまり調べられていませんでしたが、非侵襲力測定を用いて物理的原因を明らかにすることにより、疾患メカニズム解明に役立つと期待されます。
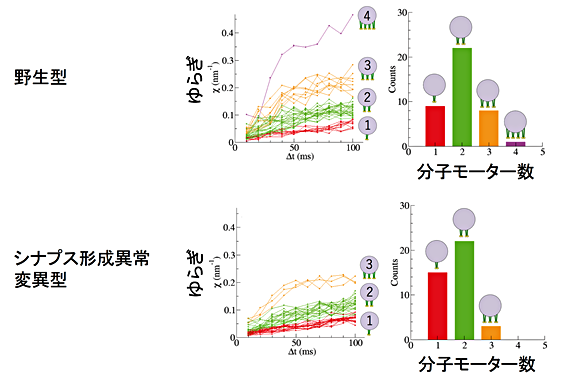
図4:ゆらぎを特徴付ける量χは力に比例。χの値は分子モーター数を反映し、とびとびの値をとる。変異型で分子モーター数は減少。
本研究は、東北大学の林久美子助教、丹羽伸介助教を始めとした共同研究グループによって、国立研究開発法人日本医療研究開発機構(AMED)の革新的先端研究開発支援事業(PRIME)「メカノバイオロジー機構の解明による革新的医療機器及び医療技術の創出」研究開発領域における研究開発課題「ゆらぎを利用した低侵襲な力測定による神経細胞オルガネラ輸送の解明」(研究開発代表者:林 久美子)ならびに文部科学省科学研究費補助金新学術領域研究「理論と実験の協奏による柔らかな分子系の機能の科学」の一環として行われました。
用語説明
- 注1 非侵襲力測定法:
- 細胞を引っ張るなどの外力を加えずに、力を測定する方法。傷付きやすい細胞での力測定で必要とされる。
論文情報
- Title:
- “Non-invasive force measurement reveals the number of active kinesins on a synaptic vesicle precursor in axonal transport regulated by ARL-8”
- Authors:
- Kumiko Hayashi*, Shin Hasegawa, Takashi Sagawa, Sohei Tasaki and Shinsuke Niwa*
- タイトル:
- ARL-8が制御するシナプス小胞前駆体輸送のキネシン分子数:非侵襲力測定法の応用
- 著者名:
- 林久美子、長谷川慎、佐川貴志、田崎創平、丹羽伸介
- 掲載誌:
- Physical Chemistry Chemical Physics
参考情報
- K.Hayashi et al., biorxiv doi:
- S. Niwa et al., Cell Report 16, p2129-2141 (2016)
お問い合わせ先
研究に関すること
東北大学大学院工学研究科
助教 林 久美子
電話番号:022-795-7955
E-mail:kumiko"AT"camp.apph.tohoku.ac.jp
東北大学学際科学フロンティア研究所/大学院生命科学研究科
助教 丹羽 伸介
電話番号:022-217-6195
E-mail:shinsuke.niwa.c8"AT"tohoku.ac.jp
報道に関すること
東北大学工学研究科情報広報室
担当 馬場 博子
電話番号:022-795-5898
E-mail:eng-pr"AT"grp.tohoku.ac.jp
AMED事業に関すること
国立研究開発法人日本医療研究開発機構(AMED)
基盤研究事業部 研究企画課
電話番号:03-6870-2224
E-mail:kenkyuk-ask"AT"amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
掲載日 平成30年1月19日
最終更新日 平成30年1月19日


