筋肉が嗅覚ニューロンに影響を与え体の温度耐性を調節―RNA分解酵素がアポトーシス分子を介してシナプスを刈り込む―
プレスリリース
甲南大学
日本医療研究開発機構
甲南大学理工学部の久原篤教授、宇治澤知代元研究員、太田茜研究員らの研究チームは、ヒトにおいて詳細な役割が未知であるENDOU(エンドウ)と呼ばれるRNA分解酵素が、寿命や温度耐性、産卵数や神経シナプスの刈り込み注1)など、多様な生命現象に関与していることを線虫の解析から明らかにしました。
特に、温度耐性において、ヒトのENDOUに相当する線虫のENDU-2が筋肉で働くことで、頭部の1対の嗅覚ニューロン(ADL)の活動を変化させ、体全体の温度耐性を変化させることがわかりました。さらに、ADL嗅覚ニューロンが温度に応答すること、ADL嗅覚ニューロンの中でもENDU-2が神経活動を調節すること発見しました。
生命の温度に対する適応は、生存していくために非常に重要な生体メカニズムです。そのため、温度適応メカニズムの解明は、温度が関わる疾患の原因解明だけでなく、温暖化や局所的な寒冷化による生物の存続など多くの分野で望まれています。
研究チームは、シンプルな実験動物である線虫C.エレガンス注2)の低温耐性を解析してきました。本研究から、筋肉がENDU-2を介して頭部の嗅覚ニューロンに働きかけ、温度耐性を調節すること、さらに、ENDU-2 は神経細胞内でも、プログラム細胞死(アポトーシス)を誘導する遺伝子の発現を調節し、シナプスの数を適切に刈り込んでいました。これらの現象が組み合わさり、温度耐性が調節されていました。
これまでにヒトと線虫で共通する生体調節メカニズムが多数発見されているため、線虫のENDU-2 が関わる生体現象や温度耐性の仕組みは、ヒトの温度耐性の仕組みや、温度が関わる疾病の原因解明などにも役立つ可能性があると期待されます。
本研究の成果は、2018年8月13日15時(米国東部標準時(夏時間))に、米国科学アカデミー紀要「Proceedings of the National Academy of Sciences of USA(PNAS)」のオンライン速報版で公開されます。
研究の背景と経緯
温度は生体反応に直接影響を及ぼす重要な環境情報です。そのため、温度に対する適切な応答は、生命が生存していくために非常に重要な生体メカニズムです。生体機能において、急激な温度変化は大きな負担がかかり、例えばヒトの場合、急激な温度変化で脳卒中や心疾患を引き起こしやすくなります。温度適応機構は多くの生物に保存されている生体メカニズムと考えられ、その仕組みを明らかとすることは多方面から望まれています。しかし、温度適応は体内の多数の細胞からなるネットワークの情報処理の結果であるため、その仕組みの解明には多大な時間を要すると考えられます。例えば、ヒトの体は約37兆の細胞で構成されており、その細胞間ネットワークは複雑です。さらに、生体調節の中枢である脳は、約1000億個の神経細胞で構成されているため、その神経ネットワークは非常に複雑です。これらのことが、温度適応を含む生体内の情報処理の解析の大きなハードルとなっています。
本研究チームは、959個の細胞からなるシンプルなモデル実験動物である線虫「C.エレガンス」を使い、温度適応メカニズムの解明を目指してきました。これまでに、低温耐性現象(図1)の解析から、頭部にある1対の感覚神経細胞(温度受容ニューロン)が温度を受容し、この神経細胞がインスリンを分泌して腸に情報を伝え、腸が温度耐性を制御することを発見しています(Ohta, Ujisawa et al.,Nature commun, 2014)。また、腸の下流で精子が関与し、精子が温度受容ニューロンの神経活動に影響をフィードバック制御することも見つかっています(Sonoda et al., Cell reports, 2016)(図2)。
また、温度耐性に関わる新しい分子(遺伝子)として、ENDU-2と呼ばれる分子(遺伝子)が、低温耐性に関与する可能性が示唆されていました(Ohta, Ujisawa et al., Nature commun, 2014)。
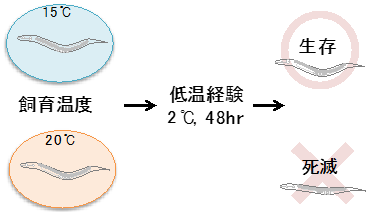
図1 線虫の温度に対する適応(低温耐性)
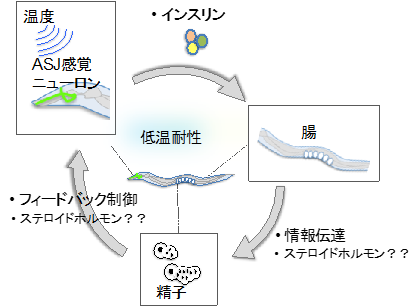
図2 既知の温度適応の生体ネットワーク
研究の内容
ヒトにおいて個体レベルでの詳細な役割が未知であったENDOU(エンドウ)と呼ばれるRNA分解酵素に着目し、その線虫ホモログであるENDU-2について解析をすすめました。ENDU-2の機能を生化学的に解析した結果、RNA注3)を分解する酵素であるエンドリボヌクレアーゼであることがわかりました。
そこで、ENDU-2が欠損した変異体線虫(endu-2変異体)について、どのような異常を示すか調べたところ、寿命や温度耐性、産卵数などに異常が見つかりました。また、温度耐性に関しては、25℃飼育後に2℃に置かれても生存できる低温耐性の上昇が見られましたが、このendu-2変異体の異常は、既知の低温耐性に関わる細胞でendu-2遺伝子を発現させても回復しませんでした。
ところが、endu-2変異体の様々な細胞にendu-2遺伝子を導入していったところ、嫌いな化学物質を感知する頭部のADLと呼ばれる1対の「嗅覚ニューロン」または「筋肉細胞」でendu-2遺伝子を発現させるた時に変異体の異常が回復しました。
そこで、ADLニューロンが、化学物質だけでなく温度にも応答するかを、カルシウムイメージング法という光技術で測定したところ、ADLニューロンは温度に反応することが見つかりました。
さらに、endu-2変異体では、ADLニューロンの温度応答性が低下していました。予想外にも、この異常は、「ADLニューロン」または「筋肉細胞」でendu-2遺伝子を発現させることで回復しました。
つまり、(1)筋肉がADLニューロンを調節し体の温度耐性を調節すること(図3)、(2)ADLの中でもENDU-2が働き温度耐性を調節していることが分かりました(図3)。
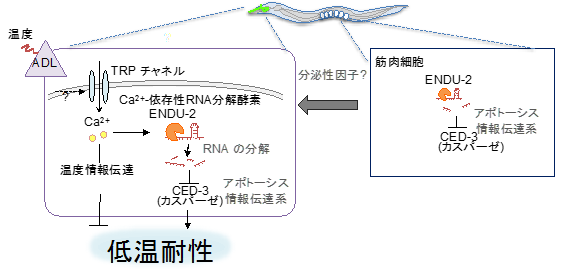
図3 ENDU-2を介した筋肉による頭部のADL感覚ニューロンの調節とADL内の抑制性の調節
ENDU-2によって発現制御を受ける転写産物候補を探索するために、野生株とendu-2変異体の体内RNAの種類と量を、次世代シークエンサーを使ったRNAシークエンシング注4)解析により比較しました。その結果、endu-2変異体では、プログラム細胞死(アポトーシス) 注5)を誘導することで知られるカスパーゼ注6) (CED-3)の遺伝子の発現量が変化していました。
過去の解析から、カスパーゼがニューロン内のシナプス注7)の数を正に制御していることが知られていたため、endu-2変異体についてもニューロンの中のシナプスの数を測定しました。その結果、endu-2変異体ではシナプスの数が増加していました。つまり、ENDU-2はCED-3の量を調節することで、シナプスの数を抑制的に調節していました(図4)。
以上のように、ENDU-2は、(1)筋肉による頭部のADL嗅覚ニューロンの調整と、(2)ニューロン内のシナプスの数の調節という、2つの役割を持つことで、温度耐性を調節していることが示唆されました(図5)。
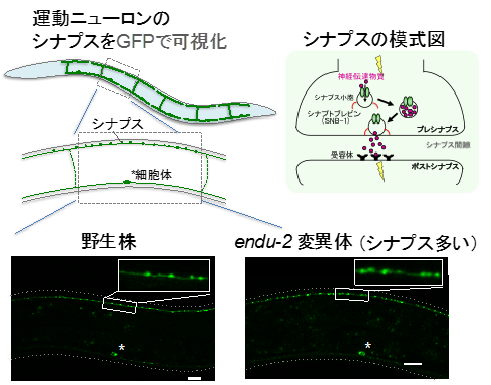
図4 endu-2変異体ではシナプスの数が多い
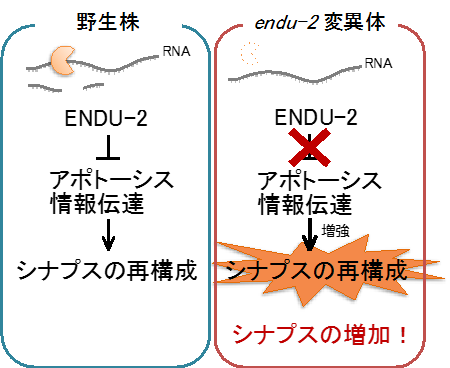
図5 ENDU-2がアポトーシス情報伝達系を抑制しシナプスの数を調節
今後の展開
温度に対する適応能力は、その重要性から多くの生物で保存されています。さらに、線虫のENDU-2に相当する分子がヒトにも存在しています。これまでにヒトと線虫の間に共通する生体調節メカニズムが多数見つかっていることから、本研究で得られた線虫におけるENDU-2を介した生体現象や温度耐性の仕組みは、ヒトの温度適応の仕組みや、温度が関わる疾病の原因解明などにも役立つ可能性があると期待されます。
研究支援
本研究は、日本医療研究開発機構(AMED)革新的先端研究開発支援事業(PRIME)「メカノバイオロジー機構の解明による革新的医療機器及び医療技術の創出」研究開発領域における研究開発課題「新規温度センサー分子の単離とそれを用いた応用技術の創出」(研究開発代表者:久原篤)、文部科学省科学研究補助金 新学術領域(研究領域提案型)「温度を基軸とした生命現象の統合的理解」研究領域における研究課題「TRPチャネルおよび膜脂質による温度センシング機構の解明」(研究代表者:富永真琴、研究分担者:久原篤)の研究費によって行われました。
用語解説
- 注1)シナプスの刈り込み
- シナプス刈り込みとは、動物が生後から成熟個体になるまでに、必要なシナプスだけが残り、不要なシナプスは除去される現象である。成熟個体への発生段階の神経回路における普遍的現象と考えられている。
- 注2)C.エレガンス
- 土壌に生息する非寄生性の線虫で、正式名称はカエノラブディティス・エレガンス。古くから分子遺伝学的解析に使用されている。1998年には多細胞生物で初めて全ゲノムDNAの解読が終了した。ヒトの遺伝子数と同等に約2万個の遺伝子を持ち、類似の遺伝子も多い。
- 注3)RNA
- 細胞内では新たなタンパク質を作るために、核内に高度に保存されたDNA情報から、一度RNAへと転写が行われる。その転写配列を元にタンパク質が合成される。
- 注4)RNAシークエンシング
- サンプルから取り出したsmall RNAを含む全転写物を、次世代シークエンサーを用いて遺伝子配列情報を高速で読み取り、定量化する方法。
- 注5)アポトーシス
- プログラム細胞死とも呼ばれ、あらかじめ遺伝子内に細胞死を起こすことがプログラムされており、不要になった細胞が自ら死ぬこと。ヒトでは、胎児の水かきがアポトーシスにより消去されることが知られている。
- 注6)カスパーゼ
- アポトーシス誘導を実行させる分子であり、蛋白質の断片化をおこなう。線虫のアポトーシスシグナル経路ではCED-3が知られている。
- 注7)シナプス
- シナプスは、神経細胞間等に形成される、神経情報伝達に関わる接合部位とその構造として知られている。神経伝達物質が分泌されるシナプス前細胞と、それを受け取るシナプス前細胞からなる。
掲載論文名
“Endoribonuclease ENDU-2 regulates multiple traits including cold tolerance via cell autonomous and nonautonomous controls in Caenorhabditis elegans”
(C.エレガンスにおいてRNA分解酵素 ENDU-2は低温耐性を含む複数の現象を細胞自律的かつ非自律的に制御する)
米国科学アカデミー紀要「Proceedings of the National Academy of Sciences of USA(PNAS)
発表者
宇治澤 知代(ウジサワ トモヨ)(研究実施時の所属:甲南大学理工学部 研究員)
*太田 茜(オオタ アカネ)(日本学術振興会特別研究員PD、甲南大学特別研究員)
Tatsuya Ii(University of Alaska Anchorage, Researcher)
水口 洋平(ミナクチ ヨウヘイ)(国立遺伝学研究所、研究員)
豊田 敦(トヨダ アツシ)(国立遺伝学研究所、特任教授)
Miki Ii(University of Alaska Anchorage, Assistant Professor)
*久原 篤(クハラ アツシ)(甲南大学理工学部、教授)
*責任著者
お問い合わせ先
本研究内容に関すること
久原 篤(クハラ アツシ)(本研究論文の責任著者)
甲南大学 理工学部 教授
〒658-8501 兵庫県神戸市東灘区岡本8-9-1 甲南大学理工学部(14号館3F 久原研)
TEL:078-435-2512 FAX:078-435-2539
E-mail:kuhara"AT"konan-u.ac.jp
研究室ホームページ: http://kuharan.com/index.html
太田 茜(オオタ アカネ)(本研究論文の責任著者)
日本学術振興会 特別研究員PD/甲南大学特別研究員
〒658-8501 兵庫県神戸市東灘区岡本8-9-1 甲南大学理工学部(14号館3F 久原研)
TEL:078-435-2512 FAX:078-435-2539
E-mail:aohta"AT"center.konan-u.ac.jp
宇治澤 知代(ウジサワ トモヨ)(本研究論文の筆頭著者)
現職:自然科学研究機構 生命創成探究センター 博士研究員
〒〒444-8787 愛知県岡崎市明大寺町東山5-1 山手2号館6階西
TEL:0564-59-5286 FAX:0564-59-5285
E-mail:ujisawa"AT"nips.ac.jp
広報に関すること
羽田 和幸(ハネダ カズユキ)
甲南学園 広報部
〒658-8501 兵庫県神戸市東灘区岡本8-9-1
TEL:078-435-2314 FAX:078-435-2546
E-mail: kouhou"AT"adm.konan-u.ac.jp
AMED事業に関すること
国立研究開発法人日本医療研究開発機構(AMED)
基盤研究事業部 研究企画課
TEL:03-6870-2224 FAX:03-6870-2246
E-mail:kenkyuk-ask"AT"amed.go.jp
※E-mailは上記アドレス”AT”の部分を@に変えてください。
掲載日 平成30年8月14日
最終更新日 平成30年8月14日


