汗孔角化症の発症メカニズムを解明―日本人の400人に1人が生まれつき発症素因を持つことが明らかに―
プレスリリース
慶應義塾大学
国立成育医療研究センター
日本医療研究開発機構
慶應義塾大学医学部皮膚科学教室の久保亮治(くぼあきはる)准教授、国立成育医療研究センター周産期病態研究部の中林一彦室長らの共同研究グループは、汗孔角化症(かんこうかっかしょう)という皮膚病になる生まれつきの素因を、日本人の400人に1人が持っていることを明らかにしました。さらに、そのような人では、紫外線などにより後天的に皮膚の細胞のゲノムが変化すると、汗孔角化症の症状が全身の皮膚に多発することが分かりました。
汗孔角化症は、直径数mm~数cmの大きさで、赤や茶色の、円形または環状の形をした、平たく少しだけ盛り上がったできもの(皮疹)が、全身の皮膚に多発する病気です。皮疹からは皮膚癌ができやすいことが知られています。子どもの身体の一部分の皮膚に集中して皮疹ができる「線状汗孔角化症」と、大人になってから腕や足を中心に全身に皮疹ができる「播種状表在性光線性汗孔角化症」などがあります。
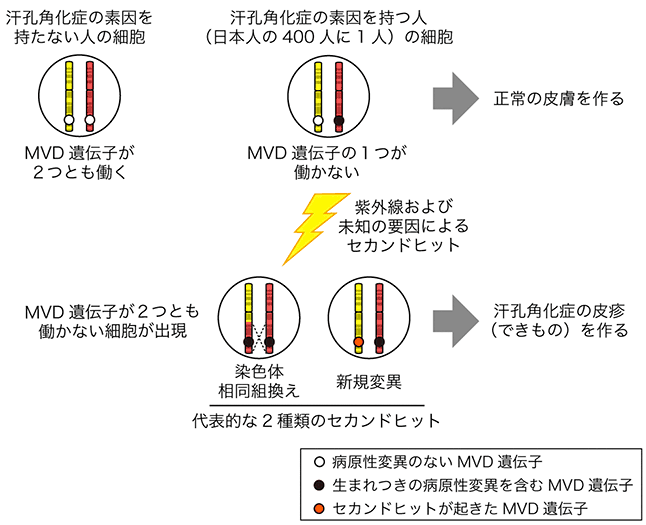
汗孔角化症を発症する人は、MVD(注1)やMVK(注2)などの遺伝子に、生まれつきの変化(遺伝子変異)を1つ持っていることが分かっていました。ヒトの細胞は遺伝子を2つずつ持っているので、遺伝子の片方が変化して働かなくても、もう片方がスペアとして働き、通常は何も問題は起きません。なぜ、遺伝子の片方だけに変化を持つ人が汗孔角化症を発症するのか、その仕組みはこれまで全く分かっていませんでした。
今回の研究から、(1)日本人のおよそ400人に1人は、MVDという遺伝子に生まれつきの変化があり、汗孔角化症になる素因を持つこと、(2)ゲノムに生じた後天的な変化(以下、セカンドヒット)によって、MVDという遺伝子が2つとも働かなくなった細胞が、汗孔角化症の皮疹を作ること、(3)セカンドヒットが胎児期に一度だけ生じると「線状汗孔角化症」になり、大人の皮膚のあちらこちらで何度も生じると、「播種状表在性光線性汗孔角化症」になることが分かりました。
今回の研究成果は、汗孔角化症から皮膚癌になるメカニズムの解明や、汗孔角化症の予防法・治療法の開発につながることが期待されます。
本研究成果は、2019年8月26日(グリニッジ標準時)に米国研究皮膚科学会の学術誌『Journal of Investigative Dermatology』(オンライン版)に掲載されました。
研究の背景
汗孔角化症は、1893年にVittorio Mibelliによって初めて記載された皮膚病で(Mibelli, G Ital Mal Ven, 1893)、さまざまな異なるタイプがあることが知られています。皮膚科の日常の診療において、しばしば診察する機会のある病気です。親子や兄弟がともに発症することがあることから、生まれつきの遺伝的な要因があることが予想されていました。
2015年に中国の研究グループから、汗孔角化症になる人の多くは、メバロン酸経路(注3)の酵素をコードする複数の遺伝子(MVDやMVKを含む複数の遺伝子)のいずれかに生まれつきの変化を持つことが報告されました(Zhang et al, eLife 2015)。しかし、この変化を持つ人が、なぜ汗孔角化症になるのか、その仕組みはこれまで全く分かっていませんでした。
研究の概要と成果
今回、慶應義塾大学医学部皮膚科学教室の久保亮治准教授を中心とした、同百寿総合研究センター、同臨床遺伝学センター、国立成育医療研究センター・周産期病態研究部の共同研究グループは、子どものうちから身体の一部の皮膚に集中して症状が現れる「線状汗孔角化症」と、大人になってから全身の皮膚に症状が現れる「播種状表在性光線性汗孔角化症」という、2つのタイプの汗孔角化症に着目して、解析を行いました。
「線状汗孔角化症」2名、「播種状表在性光線性汗孔角化症」7名、合計9名に採血検査と皮膚のできもの(皮疹)の生検検査を行い、それぞれの細胞の遺伝子を調べました。その結果、9名のうち7名が、2つあるMVD遺伝子の片方に、746番目のC(シトシン)がT(チミン)へと塩基が置き換えられる変化(c.746T>C)を生まれつき持っていたことが分かりました。残りの2名のうち1名はMVD遺伝子の片方に、もう1名はMVK遺伝子の片方に、比較的まれな変化を生まれつき持っていました。
MVD遺伝子のc.746T>Cという変化は、中国の研究からも報告されており、病気の原因となる変化と考えられます。東北メディカル・メガバンクの日本人ゲノムデータベースを調べたところ、およそ日本人の400人に1人が、この変化を生まれつき持っており、汗孔角化症になる素因を持つことが分かりました。
ヒトの細胞は遺伝子を2つずつ有しているので、片方が変化して働かなくても、もう片方がスペアとして働き、通常は何も問題は起きません。なぜ、片方の遺伝子にしか変化を持たない人が汗孔角化症になるのか、その仕組みはこれまでまったくわかっていませんでした。
研究グループが9名の血液の細胞、症状のない皮膚の細胞、症状のある皮膚の細胞を比較した結果、症状のある皮膚の細胞でだけ、スペアとして働くはずのもう片方の遺伝子が、後天的に変化してしまっていることが分かりました。つまり、後天的な変化(以下、セカンドヒット)により、MVDまたはMVKのいずれかの遺伝子が2つとも働かなくなった細胞が、汗孔角化症の皮疹を作っていたことが示されました。
セカンドヒットは主に2つの仕組みによって生じていました(図1)。最も多かったのは、染色体の途中からテロメア末端までが片親由来となる染色体の変化でした。この変化により、生まれつき片方の遺伝子にあった変化が、もう片方の遺伝子にもコピーされてしまい、遺伝子が2つとも働かなくなっていました(図1)。このような染色体の変化は、体細胞における染色体相同組換え(注4)により生じると考えられていますが、その誘因はまだよく分かっていません。次に多かったのは、遺伝子の暗号がCからTへと書き換えられてしまう遺伝子の変異でした。これは主に紫外線によって引き起こされることが分かっています。
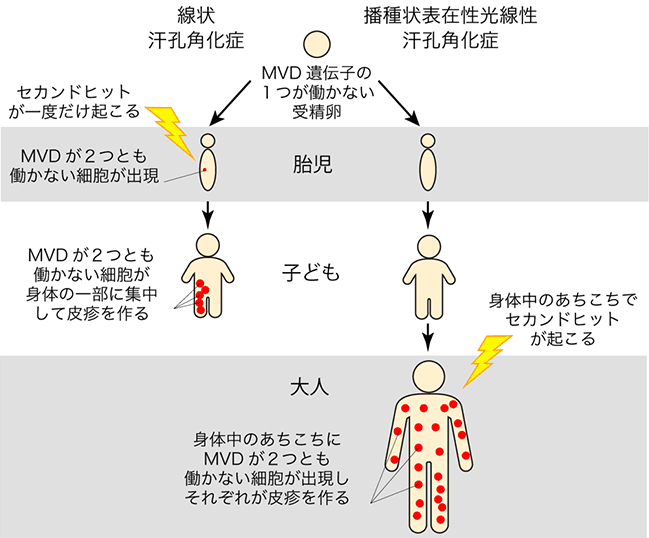
子どものうちに発症した「線状汗孔角化症」では、別々の皮疹が全て同一のセカンドヒットによる変化を持っていました。つまり、胎児期にセカンドヒットが起こった1つの細胞が、身体が作られていく過程で増殖して拡がった結果、身体の一部に線状に分布する汗孔角化症の皮疹ができたと考えられました(図2)。
一方、大人になってから発症した「播種状表在性光線性汗孔角化症」では、身体中に散らばる1つ1つの皮疹は、それぞれ別々のセカンドヒットによる変化を持っていました。つまり、大人になってから、皮膚のあちこちで別々にセカンドヒットが起こり、セカンドヒットが起こったそれぞれの細胞が増殖して皮疹を作ったと考えられました(図2)。
研究の意義・今後の展開
今回の研究から、日本人の400人に1人という、これまで考えられていたよりもずっと多くの人が、汗孔角化症になる生まれつきの素因を持つことが分かりました。さらに、汗孔角化症を発症させるセカンドヒットの仕組みが明らかになり、セカンドヒットが胎児期に生じるか、大人になってから生じるかによって、異なる2種類の汗孔角化症になることが分かりました。本成果は、汗孔角化症の予防法や治療法の開発につながると考えられます。さらに今後、セカンドヒットが起こった細胞が増殖する仕組みを解き明かし、この病気から皮膚癌が生じる仕組みを解き明かすことで、皮膚癌の治療を目指す研究を加速させることが期待されます。
特記事項
本研究は国立研究開発法人日本医療研究開発機構(AMED)の臨床ゲノム情報統合データベース整備事業「希少・難治性疾患領域における臨床ゲノムデータストレージの整備に関する研究」、難治性疾患実用化研究事業「未診断疾患イニシアチブ(Initiative on Rare and Undiagnosed Disease(IRUD)):希少未診断疾患に対する診断プログラムの開発に関する研究」およびマルホ株式会社との共同研究費の支援を受けて行われました。
論文
- タイトル:
- Clonal expansion of second-hit cells with somatic recombinations or C>T transitions form porokeratosis in MVD or MVK mutant heterozygotes
- タイトル和訳:
- MVDまたはMVKに遺伝子変異をヘテロ接合で持つ人では、体細胞における染色体相同組換え、またはCからTへの点突然変異によるセカンドヒットが生じた細胞がクローン増殖することにより、汗孔角化症が生じる
- 著者名:
- 久保亮治,佐々木貴史、鈴木寿人、塩濱愛子、青木里美、佐藤尚武、藤田春美、小野紀子、梅垣知子、河合智子、中林一彦、秦健一郎、山田大資、松原洋一、小崎健次郎、天谷雅行
- 掲載誌:
- Journal of Investigative Dermatology(オンライン版)
- DOI:
- https://doi.org/10.1016/j.jid.2019.05.020
共同研究グループ
- 慶應義塾大学医学部皮膚科学教室
- 久保 亮治准教授、小野 紀子助教、梅垣 知子講師(非常勤)、青木 里美、佐藤 尚武、 天谷 雅行教授
- 慶應義塾大学医学部コーセー寄附講座
- 塩濱 愛子特任助教、藤田 春美特任助教
- 慶應義塾大学医学部百寿総合研究センター
- 佐々木 貴史専任講師
- 慶應義塾大学医学部臨床遺伝学センター
- 鈴木 寿人特任講師、小崎 健次郎教授
- 国立成育医療研究センター・周産期病態研究部
- 中林 一彦室長、河合 智子室長、秦 健一郎部長、嘉村 浩美技術員、
- 国立成育医療研究センター 研究所
- 松原 洋一研究所長
用語解説
- (注1):MVD:
- メバロン酸経路の酵素の1つであるジホスホメバロン酸デカルボキシラーゼ(mevalonate pyrophosphate decarboxylase)をコードする遺伝子。
- (注2):MVK:
- メバロン酸経路の酵素の1つであるメバロン酸キナーゼ(mevalonate kinase)をコードする遺伝子。
- (注3):メバロン酸経路:
- コレステロールやステロイド、タンパク質の翻訳後修飾に用いられる脂質などを合成するための材料をアセチルCoAから作り出す経路。
- (注4):体細胞における染色体相同組換え:
- 父親由来の染色体と母親由来の染色体の間で組換えが起こることで、染色体全体の長さは変わらないまま、途中までは父親由来、途中からは母親由来という、ハイブリッドになった染色体が生まれる現象。
お問い合わせ先
本発表資料のお問い合わせ先
慶應義塾大学医学部 皮膚科学教室
准教授 久保 亮治(くぼ あきはる)
TEL:03-5363-3823 FAX:03-3352 -6880
E-mail:akiharu“AT”keio.jp
本リリースの発信元
慶應義塾大学信濃町キャンパス総務課
鈴木・山崎
〒160-8582 東京都新宿区信濃町35
TEL:03-5363-3611 FAX:03-5363-3612
E-mail:med-koho“AT”adst.keio.ac.jp
国立成育医療研究センター 企画戦略局 広報企画室
村上・近藤
TEL:03-3416-0181(内線 7783・7249)
E-mail:koho“AT”ncchd.go.jp
AMED事業に関するお問い合わせ先
国立研究開発法人 日本医療研究開発機構 (AMED)
基盤研究事業部 バイオバンク課
TEL:03-6870-2228
E-mail:genome-db“AT”amed.go.jp
戦略推進部 難病研究課
TEL:03-6870-2223
E-mail:nambyo-info“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
掲載日 令和元年8月26日
最終更新日 令和元年8月26日


