難治性の傷を治す人工タンパク質を開発―産官学連携で医師主導治験を経て企業治験へ―
プレスリリース
国立大学法人京都大学
三洋化成工業株式会社
国立研究開発法人日本医療研究開発機構
概要
京都大学大学院医学研究科形成外科学講座 野田和男 助教らと三洋化成工業株式会社(本社:京都市東山区、社長:安藤孝夫)は共同研究を行い、慢性創傷を治療する目的で、国立研究開発法人日本医療研究開発機構(AMED)医療分野研究成果展開事業 産学連携医療イノベーション創出プログラム(ACT-M)等の支援のもとに、新規治療材料シルクエラスチンスポンジを開発しました。
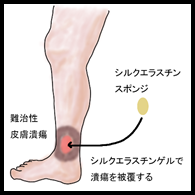
近年、糖尿病患者の増加あるいは高齢化に伴い、糖尿病性皮膚潰瘍等に代表される治りにくい創傷(慢性創傷)の増加が問題となっています。慢性創傷ではさまざまな原因で治癒が遅れ、細菌に感染し、更に治癒が遅れる悪循環になります。今回開発した新規治療材料は人工タンパク質シルクエラスチンで作製されており、感染しやすい慢性創傷に対しても有効な材料であることを動物実験等で確認しました。その後、京都大学医学部附属病院で2018年2月から12月まで、下腿難治性皮膚潰瘍を対象として、シルクエラスチンスポンジを用いた医師主導治験を行い、本材料の安全性を確認しました。
なお、この医師主導治験の成果を受けて、AMED医工連携事業化推進事業にて2020年1月から2022年3月までの開発期間(予定)にて、研究開発課題「革新的タンパク質シルクエラスチンを用いた創傷治癒材の開発及び事業化」として三洋化成工業株式会社が中心となり京都大学と広陵化学工業株式会社とともに、本材料の有効性を確認する目的の企業治験を実施し、4年以内に本材料を新規医療機器として承認を得ることを目標に事業化に向けた開発を推進します。

背景
やけどやケガ、皮膚がんの切除などで皮膚が欠損した場合、傷を治す力があれば、通常の治療で治ります。しかし、傷を治す力がない傷(難治性皮膚潰瘍)では、治るのに長い時間がかかる、あるいは治らないことが問題になります。難治性皮膚潰瘍の原因としては糖尿病、静脈還流うっ滞、膠原病等があります。難治性皮膚潰瘍を治すためには、傷を乾燥させず(湿潤を保ち)、かつ細菌感染を起こさないように、毎日傷を洗い、傷を治す軟膏を使用したり、被覆材を貼り替える必要があります。数日間そのまま交換しなければ、細菌が増えて感染が起こります。
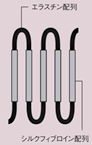
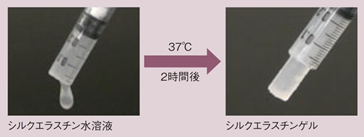
シルクエラスチンは、シルクフィブロイン※1の部分配列とエラスチン※2の部分配列とを組み合わせ、遺伝子組み換え技術によって作製された人工タンパク質です(図1)。シルクエラスチン水溶液は37度に温めるとタンパク質の構造が変化し、水分を含んだ状態で固まる(ゲル化する)という特徴があります(図2)。このシルクエラスチンの特徴を利用して、傷を治す材料(創傷治癒材)の開発を行ったところ、動物実験において、シルクエラスチンゲルが細菌感染を助長せず、傷を治す力を増強する(創傷治癒を促進する)ことを発見しました。
研究手法・成果
動物実験の結果では、感染しやすい傷に対して、シルクエラスチン水溶液を創傷治癒材として使用すると、感染を助長せず創傷の治癒を促進する効果がみられたため、実際の難治性皮膚潰瘍に対して臨床使用することを計画しました。使いやすいように、シルクエラスチンをスポンジ形状に加工したシルクエラスチンスポンジを作製しました。シルクエラスチンスポンジを皮膚の傷に貼付すると、傷から出る体液によりシルクエラスチンスポンジが溶解し、溶解したシルクエラスチン溶液が傷の表面でゲル化し、創傷の治癒を促進する効果があることを動物実験で確認しました。
そこで、シルクエラスチンスポンジを用いた医師主導治験を計画しました。治験の目的は、シルクエラスチンスポンジの安全性を確認することです。治験は2018年2月から12月まで、6例に対して行いました。その結果、重篤な、重症度の高い有害事象は起こらず、治験機器の不具合も認めなかったため、シルクエラスチンスポンジの安全性が確認されました。この結果を元に、有効性を検証する企業治験を行う方針となりました。
波及効果、今後の予定
今回の医師主導治験は、シルクエラスチンスポンジの安全性確認、課題の抽出、有効性の評価指標の確立を目的としており、いずれも達成することができました。ヒトに対する初の使用経験となった本治験のデータをもとに、今後の企業治験を計画し、さらなる知見を深める予定です。2020年度中に企業治験を開始し、将来的には医療機器としての承認を目指しています。
医師主導治験の結果を踏まえて、日本医療研究開発機構(AMED)の以下の事業にて事業化に向けた開発を推進します。詳細は以下のとおりです。
- 事業名 :
- 平成31 年(令和元年)度 医工連携事業化推進事業
- 課題名 :
- 革新的タンパク質シルクエラスチンを用いた創傷治癒材の開発及び事業化
- 研究者 :
- 三洋化成工業株式会社、国立大学法人京都大学、広陵化学工業株式会社
- 期間 :
- 2020年1月~2022年3月(予定)
- 計画 :
- 医師主導治験をベースとした企業治験の実施
ユーザビリティ性の高い製品形態の設計(容器や包装資材の設計等)
商用生産に向けた量産化検討(スケールアップ検討や収率向上検討等)
研究プロジェクトについて
- 1)医師主導治験
- 研究体制
- 京都大学大学院医学研究科形成外科学
- 京都大学医学部附属病院臨床研究総合センター
- 三洋化成工業株式会社
- 研究開発資金
- 国立研究開発法人日本医療研究開発機構(AMED)産学連携医療イノベーション創出プログラム(ACT-M)「機能性タンパク質シルクエラスチンを用いた新規医療材料の開発および臨床研究」
- 2017年10月~2019年3月
- 2)企業治験、事業化
- 研究開発体制
- 三洋化成工業株式会社
- 京都大学大学院医学研究科 形成外科学
- 京都大学ウィルス・再生医科学研究所 生体材料学
- 広陵化学工業株式会社
- 研究開発資金
- 国立研究開発法人日本医療研究開発機構(AMED) 医工連携事業化推進事業
- 「革新的タンパク質シルクエラスチンを用いた創傷治癒材の開発及び事業化」
- 2020年1月~2022年3月(予定)
用語解説
- *1 シルクフィブロイン:
- カイコが産生する繊維状のタンパク質であり、シルクの原料になる。
- *2 エラスチン:
- 弾性線維のを構成する主要なタンパク質。皮膚や肺、動脈が伸縮するのは弾性線維の働きによる。
お問い合わせ先
シルクエラスチンに関して
三洋化成工業株式会社 メディア・IR部
〒605-0995 京都市東山区一橋野本町11-1
TEL:075-541-4312
E-mail:pr-group“AT”sanyo-chemical.group
AMEDの事業に関して
国立研究開発法人日本医療研究開発機構(AMED) 産学連携部(産学連携課、医療機器研究課)
〒100-0004 東京都千代田区大手町1-7-1
TEL:03-6870-2214
E-mail:sangaku-i“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
関連リンク
- 三洋化成によるACT-M採択に関するプレスリリース
「『機能性タンパク質シルクエラスチンを用いた新規医療材料の開発および臨床研究』がAMED産学連携医療イノベーション創出プログラム(ACT-M)に採択」 - 三洋化成と京都大学による医師主導試験開始に関するプレスリリース
「下腿難治性皮膚潰瘍を対象としたシルクエラスチンスポンジを用いた医師主導治験を開始」 - 「UMIN臨床試験登録システム」における本治験情報
- 産学連携医療イノベーション創出プログラム・基本スキーム(ACT-M)/セットアップスキーム(ACT-MS)(医療分野研究成果展開事業)
- 産学連携医療イノベーション創出プログラム・基本スキーム(ACT-M)/セットアップスキーム(ACT-MS)(医療分野研究成果展開事業)採択課題一覧
掲載日 令和2年1月21日
最終更新日 令和2年1月21日


