下腿難治性皮膚潰瘍を対象としたシルクエラスチンスポンジを用いた医師主導治験を開始
プレスリリース
京都大学医学部附属病院
三洋化成工業株式会社
国立研究開発法人日本医療研究開発機構
ポイント
京都大学医学部附属病院において下腿難治性皮膚潰瘍を対象としたシルクエラスチンスポンジを用いた新たな治療法の医師主導治験を開始しました。
概要
京都大学医学部附属病院は下腿難治性皮膚潰瘍を対象としたシルクエラスチンスポンジを用いた医師主導治験を平成30年2月から開始しました(図1)。京都大学大学院医学研究科形成外科学(教授:鈴木茂彦、客員研究員:河合勝也)、三洋化成工業株式会社(本社:京都市東山区、社長:安藤孝夫、以下「三洋化成」)を中心とした共同研究による成果です。
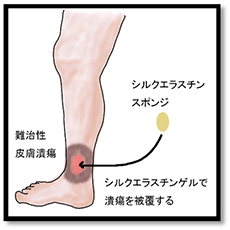
図1. 下腿難治性皮膚潰瘍に対するシルクエラスチンスポンジを用いた治験治療
京都大学形成外科学講座では三洋化成との共同研究として、2009年よりシルクエラスチンを用いた皮膚潰瘍に対する基礎的研究を開始し、シルクエラスチンが創傷治癒を促進する効果があることを見出しました。この結果をもとに、2013年より国立研究開発法人科学技術振興機構(JST)「研究成果最適展開支援プログラム(A-STEP)」、2015年より国立研究開発法人日本医療研究開発機構(AMED)「橋渡し研究加速ネットワークプログラム」の支援を受けて研究を加速させ、その後2016年10月よりAMEDの「産学連携医療イノベーション創出プログラム(ACT-M)」の支援を受けています。
これらの成果をもとに平成30年1月4日に独立行政法人医薬品医療機器総合機構に治験届を提出しました。
背景
皮膚潰瘍(皮膚の欠損、傷)が生じた場合、軟膏や被覆材を使って潰瘍が治るまで処置を行います。しかし、なかなか治らない場合もあり、難治性皮膚潰瘍と呼ばれます。難治性皮膚潰瘍の原因としては、糖尿病、動脈や静脈の障害、膠原病などがあります。難治性皮膚潰瘍の治療方法として皮膚移植などが行われますが、皮膚が生着しないこともあります。難治性皮膚潰瘍を治すためには、適度な湿潤環境を維持し、また細菌感染などの増悪因子を助長させない治療が求められますが、そのためには毎日の処置が必要になります。
シルクエラスチンは、ヒト由来のエラスチン*1)と天然由来のシルクフィブロイン*2)を部分的に組み合わせ、遺伝子組み換え技術によって作製された人工タンパク質です(図2)。
*1)皮膚などの弾性線維を構成するタンパク質,*2)シルク(絹)を構成するタンパク質
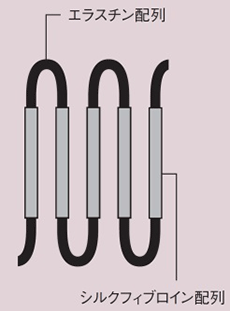
図2.シルクエラスチンの構造
シルクフィブロイン部分とエラスチン部分が交互に連結したタンパク質です。
シルクエラスチン水溶液は37度に温めるとタンパク質の構造が変化し、水分を含んだ状態で固まる(ゲル化する)という特徴があります(写真1)。この特徴を利用して創傷治癒材としての開発研究を行い、シルクエラスチンが難治性皮膚潰瘍の治癒を促進する材料であることを動物実験で確認しました。動物実験では、皮膚潰瘍部で一度固まったシルクエラスチンゲルは2週間程度維持され、適度な湿潤環境を維持し、また細菌感染を助長しませんでした。このような特徴を持った創傷治癒材が実用化できれば、毎日処置する必要がなくなり、負担が軽くなると考えています。

写真1.シルクエラスチン水溶液のゲル化
シルクエラスチンを水に溶かして、体温付近(37℃前後)で加温するとゲル化します。
今回の治験機器であるシルクエラスチンスポンジ(写真2)は、シルクエラスチンをスポンジ形状に加工したものです。シルクエラスチンスポンジを創傷面に投与することで、創傷面からの体液によりシルクエラスチンが溶解します。その後、体液を含むシルクエラスチン溶液が、創傷面に密着してゲル化することで創傷治癒促進効果が生まれると考えています(図3)。

写真2.シルクエラスチンスポンジ
三洋化成の界面活性制御技術を活用して、シルクエラスチンをスポンジ形状に加工できます。
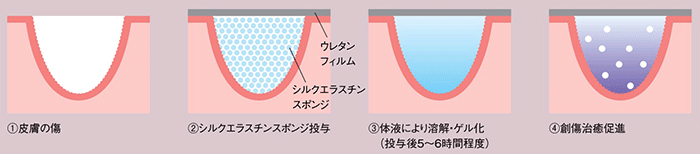
図3.シルクエラスチンスポンジを用いた傷の治療
皮膚の傷にシルクエラスチンスポンジをのせ、その上にウレタンフィルムを貼付します。その後、体液によってシルクエラスチンスポンジが溶解し、体温によってゲル化します。 ゲル化したシルクエラスチンは、傷に密着して創傷治癒を促進します。
治験概要
- 治験名:
- 下腿難治性皮膚潰瘍を対象としたシルクエラスチンスポンジ貼付による安全性評価に関する探索的臨床試験
- 治験の目的:
- 通常の治療では治癒が期待できない下腿難治性皮膚潰瘍を対象に、シルクエラスチンスポンジ貼付による治療を行ない、その安全性を確認する。
- 自ら治験を実施する者:
- 京都大学医学部附属病院 形成外科 野田和男
- 「UMIN臨床試験登録システム」における本治験情報:
今後の予定
三洋化成では、医師主導治験の結果を受けて企業治験を行ない、医療機器として承認を目指します。
お問い合わせ先
医師主導治験に関して
京都大学医学部附属病院 形成外科
TEL 075-751-3613
E-mail ecrus_office"AT"kuhp.kyoto-u.ac.jp
シルクエラスチンに関して
三洋化成工業株式会社 広報部
〒605-0995 京都市東山区一橋野本町11-1
TEL 075-541-4312
E-mail pr-group"AT"sanyo-chemical.com
事業に関して
国立研究開発法人日本医療研究開発機構(AMED)
産学連携部 産学連携課
〒100-0004 東京都千代田区大手町1-7-1
TEL 03-6870-2214
E-mail sangaku-i"AT"amed.go.jp
※E-mailは上記アドレス"AT"の部分を@に変えてください。
関連リンク
掲載日 平成30年2月5日
最終更新日 平成30年2月5日


