新たなC型肝炎ウイルス感染予防ワクチンの開発
プレスリリース
国立大学法人京都大学
国立感染症研究所
国立研究開発法人日本医療研究開発機構
国立感染症研究所
国立研究開発法人日本医療研究開発機構
ポイント
- C型肝炎ウイルス(HCV)は慢性肝炎を引き起こし、肝硬変や肝癌の原因となるウイルスとして知られているが、有効なワクチンは未だ実用化されていない。
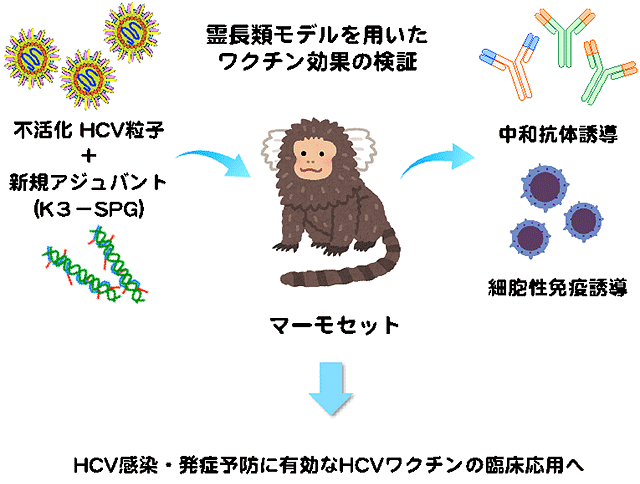
- 本研究では不活化HCV粒子ワクチンを強力な補助剤(アジュバント)であるK3-SPGとともにマーモセットに接種することで、感染・発症予防に有効な中和抗体と細胞性免疫の両方を効率良く誘導できることを明らかにした。
- 今後、不活化HCV粒子の大量合成技術やワクチン接種プロトコルの最適化を通じて、早期のHCVワクチン実用化を目指す。
概要
明里宏文(あかり ひろふみ)京都大学霊長類研究所 教授らは、加藤孝宣(かとう たかのぶ)国立感染症研究所 室長らと共同で有望なHCVワクチンの開発に成功しました。この研究グループでは、2005年に報告された培養細胞によるHCV増殖システムの技術を応用してHCV粒子を大量に培養し、その不活化HCVワクチンについて検討を進めてきました。今回の研究では、不活化HCV粒子をワクチン投与時の免疫反応を高める補強剤(以下、アジュバント)であるK3-SPGとともに小型霊長類モデルであるコモンマーモセットに接種したところ、感染・発症予防に有効な中和抗体と細胞性免疫の両方を効率良く誘導できることを初めて明らかにしました。本研究の成果により、培養細胞で作製された不活化HCV粒子は、強力な新規アジュバントであるK3-SPGとともに接種することで有効かつ安全なHCVワクチンとして使用できる可能性が示されました。
研究の背景
C型肝炎ウイルス(HCV)は慢性肝炎を引き起こし、肝硬変や肝癌の原因となるウイルスとして知られています。近年、HCVの複製を阻害する直接作用型抗ウイルス薬(Direct Acting Antivirals; DAAs)が開発され、C型慢性肝炎の治癒率は向上してきました。しかしDAAsを用いた治療は高額な医療費がかかり治癒後も再感染のリスクがあること、海外では今もなお発展途上国において感染拡大が見られることから、感染・発症予防が可能なHCVワクチンの開発が依然として求められています。
HCVワクチンの開発は、これまで世界中の研究グループ試みてきましたが実用化されていません。HCVのエンベロープタンパク質を抗原として用いたワクチンは、マウス、モルモット、チンパンジー等のモデルにおいて中和抗体を誘導できることが報告されており、既に第一相臨床試験が行われています。またHCV抗原を発現させるウイルスベクターを用いたワクチンでは、細胞性免疫の誘導も報告されています。しかし感染・発症予防に必要とされている、中和抗体および細胞性免疫の両方を同時に誘導できるワクチンは開発されていません。
HCVワクチンの開発は、これまで世界中の研究グループ試みてきましたが実用化されていません。HCVのエンベロープタンパク質を抗原として用いたワクチンは、マウス、モルモット、チンパンジー等のモデルにおいて中和抗体を誘導できることが報告されており、既に第一相臨床試験が行われています。またHCV抗原を発現させるウイルスベクターを用いたワクチンでは、細胞性免疫の誘導も報告されています。しかし感染・発症予防に必要とされている、中和抗体および細胞性免疫の両方を同時に誘導できるワクチンは開発されていません。
研究の内容
本研究グループは2005年に世界で初めて報告された培養細胞によるHCV増殖システムを応用して、HCV粒子を大量に培養・精製し不活化したHCVワクチンの有効性について検討を進めてきました。その結果、不活化HCV粒子を新規アジュバントであるK3-SPGとともに小型霊長類モデルであるコモンマーモセットに接種したところ、感染阻止に有効な中和抗体と細胞性免疫の両方を効率良く誘導できることを初めて明らかにしました。
ワクチン抗原の作製
培養細胞内で効率的な増殖が可能なHCV J6/JFH-1株(遺伝子型2a)を用い、HuH-7細胞に感染させ培養を行うことで、大量のHCV粒子を調製しました。得られたHCV粒子は限外濾過膜とショ糖密度勾配超遠心で濃縮と精製を行い、UV照射で不活化しました。
霊長類モデルを用いたワクチン接種実験
ワクチン評価実験において、不活化 HCV粒子およびK3-SPG接種群と、不活化 HCV粒子およびAlum接種群の2群に分けて、コモンマーモセットにて比較検討を行いました。それぞれの接種群は2週おきに2回もしくは3回のワクチン接種を行い、抗体および細胞性免疫の誘導能について検討しました。また臓器障害など有害事象がないかどうか観察し、安全性についての検証を行いました。
その結果、不活化HCV粒子+K3-SPG群では、不活化HCV粒子+Alum群と比較して高い活性を有する中和抗体が誘導されることがわかりました。重要なことに、不活化HCV粒子+K3-SPG群で誘導される中和抗体は、ワクチンとして使用した遺伝子型2aだけでなく他の遺伝子型のHCV株の感染性を阻止しました。さらに不活化HCV粒子+K3-SPG群では、不活化HCV粒子+Alum群と比較して高いレベルの細胞性免疫応答も見られました。なお、いずれの接種群においてもワクチンやアジュバントによる有害事象は認められませんでした。以上の実験結果より、不活化HCV粒子およびK3-SPGアジュバントを組み合わせたワクチンは、HCV感染阻止に有効な中和抗体と細胞性免疫の両方を効率良く、かつ安全に誘導できることを初めて明らかにしました。
その結果、不活化HCV粒子+K3-SPG群では、不活化HCV粒子+Alum群と比較して高い活性を有する中和抗体が誘導されることがわかりました。重要なことに、不活化HCV粒子+K3-SPG群で誘導される中和抗体は、ワクチンとして使用した遺伝子型2aだけでなく他の遺伝子型のHCV株の感染性を阻止しました。さらに不活化HCV粒子+K3-SPG群では、不活化HCV粒子+Alum群と比較して高いレベルの細胞性免疫応答も見られました。なお、いずれの接種群においてもワクチンやアジュバントによる有害事象は認められませんでした。以上の実験結果より、不活化HCV粒子およびK3-SPGアジュバントを組み合わせたワクチンは、HCV感染阻止に有効な中和抗体と細胞性免疫の両方を効率良く、かつ安全に誘導できることを初めて明らかにしました。
今後の展開
本研究の成果により、培養細胞で作製された不活化HCV粒子は、強力な新規アジュバントであるK3-SPGとともに接種することで有効かつ安全なHCVワクチンとして使用できる可能性が示されました。今後、不活化HCV粒子の大量合成技術やワクチン接種プロトコルの最適化を通じて、早期のHCVワクチン実用化を目指したいと考えています。
用語解説
- (※1)K3-SPG:
- 医薬基盤・健康・栄養研究所において開発された強力な新規アジュバントで、CpG配列を持つ合成核酸をシゾフィランと結合させたもの
- (※2)Alum:
- これまで多くのワクチンで用いられているアジュバント
研究助成
本研究は厚生労働省科学研究費補助金、創薬基盤推進研究事業(H23-政策探索-一般-002)および国立研究開発法人 日本医療研究開発機構 委託費、創薬基盤推進研究事業(15ak0101002h0005)の助成にて行われました。
共同研究機関
京都大学霊長類研究所、京都大学ウイルス・再生医科学研究所、国立感染症研究所、東レ株式会社医薬研究所、医薬基盤・健康・栄養研究所、大阪大学免疫学フロンティア研究センター
論文情報
- タイトル:
- Induction of Humoral and Cellular Immunity by Immunization with Hepatitis C Virus Particle Vaccine in a Non-human Primate Model.
- 著者:
- Yokokawa H, Higashino A, Suzuki S, Moriyama M, Nakamura N, Suzuki T, Suzuki R, Ishii K, Kobiyama K, Ishii KJ, Wakita T, Akari H, Kato T.
- 掲載誌:
- Gut
お問い合わせ先
京都大学霊長類研究所
教授 明里宏文(ウイルス・再生医科学研究所 兼任教授)
Tel:075-751-4798
E-mail:akari.hirofumi.5z”AT”kyoto-u.ac.jp
国立感染症研究所ウイルス第二部
室長 加藤孝宣
Tel:03-5285-1111
E-mail:takato”AT”niid.go.jp
国立研究開発法人日本医療研究開発機構(AMED)戦略推進部医薬品研究課
〒100-0004 東京都千代田区大手町1-7-1
Tel:03-6870-2219
E-mail:souyakukiban”AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
関連リンク
掲載日 平成28年10月27日
最終更新日 平成28年10月27日


