腫瘍細胞遺残の有無を判断できる術前画像診断の開発を目指す―日本(JCOG)と欧州(EORTC)の国際共同臨床研究 DREAM study 開始、低侵襲の治療開発および国際共同臨床研究を強力に推進―
プレスリリース
国立研究開発法人国立がん研究センター
日本臨床腫瘍研究グループ
国立研究開発法人日本医療研究開発機構
国立研究開発法人国立がん研究センター(理事長:中釜斉、所在地:東京都中央区)中央病院(病院長:西田俊朗)は、2016年度より日本医療研究開発機構(AMED)の「国際共同臨床研究実施推進事業」の拠点の1つとして選定され、国際共同臨床研究に積極的に取り組んでいます。またその一環として、がんの多施設共同臨床研究グループである日本臨床腫瘍研究グループ(JCOG)の中央支援機構(データセンター/運営事務局)を担い、JCOGとして2012年からは米国のNorth Central Cancer Treatment Group / Cancer and Leukemia Group B(NCCTG/CALGB)と、2008年からは韓国胃がん学会と共同研究を実施してきました。
そしてこの程、欧州でのがんの多施設共同臨床研究を主導するEuropean Organisation for Research and Treatment of Cancer(EORTC)と共同で、大腸がんの肝転移病変に対する画像診断の国際共同研究「DREAM study」を開始しました。本研究はJCOGとEORTCとの初の国際共同臨床研究で、欧州7か国から16施設、日本からは神奈川県立病院機構神奈川県立がんセンターと国立がん研究センター中央病院をはじめとする12施設、また米国からも2施設が参加します。3年間で計400名を登録、評価を行い、5年後の2022年に研究結果を公表することを目指します。
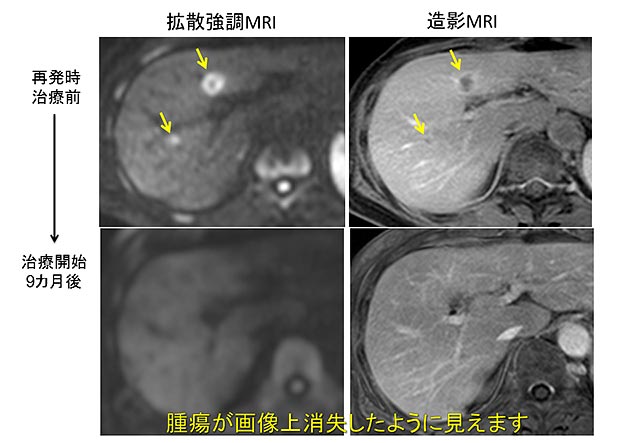
DREAM studyの目的は、化学療法後に画像上消失したと診断される大腸がんの肝転移病変を対象に、数種類のMRI(Magnetic Resonance Imaging:核磁気共鳴画像)とCT(Computed Tomography:コンピューター断層撮影)を用いて、腫瘍細胞遺残の有無を予測可能かどうか評価することです。近年、画像診断の向上に伴い、術前の画像診断から実際の腫瘍細胞の有無をより高い確率で予測することができる可能性がでてきました。
大腸がんの肝転移における外科的切除は、化学療法などで腫瘍を縮小させ、可能であれば切除する方針が採られることが一般的です。しかし、外科的切除前の画像診断で腫瘍の遺残を高い確率で正しく予測できれば、腫瘍細胞が遺残していないと判断される場合には外科的切除を行う必要がなく、低侵襲治療の確立につながることを期待しています。
本研究は、国立研究開発法人日本医療研究開発機構(AMED)国際共同臨床研究実施推進事業および革新的がん医療実用化研究事業の支援により実施するもので、低侵襲の治療開発および国際共同臨床研究を強力に推進します。
 写真 前列 中央左)国立がん研究センター JCOGデータセンター長: 福田 治彦
写真 前列 中央左)国立がん研究センター JCOGデータセンター長: 福田 治彦前列 中央右)EORTC Director General: Denis Lacombe
前列 右から2人目)EORTC研究代表者: Serge Evrard
前列 左から2人目)JCOG研究代表者: 塩澤 学
背景
大腸がんについて
画像診断について
なかでもMRIは、磁気共鳴法という強力な磁石の力を用いた検査で、体のさまざまな角度(体の輪切り像、前後や左右に縦割りにした像)の断面を見ることができる検査です。脊髄や骨盤の中、骨の断面など、CTでは撮影しにくい部分も調べることができます。被ばくがないことも大きな特徴です。
画像上の「消失」について
拡散強調MRI(DW-MRI; Diffusion-weighted MRI)は、腫瘍の活動性を反映する特性をもち、撮像時間が短く簡便で造影剤が不要なために、大腸がんでは直腸がんや大腸がん肝転移の診断における有用性が欧州を中心に数多く報告され、開発が進められています。EORTCのImaging Groupでも、DW-MRIの開発が進められ、DW-MRIの最適な撮像条件についてのガイダンスがすでに作成されています。その他のMRIとして、造影MRIも日常診療で広く用いられており、多くの病変において、病変の検出や機能的異常の評価に優れています。
小病変の検出において、造影MRI、特にGd-EOB-DPTAという造影剤を用いたEOB-MRIとDW-MRIを比較した論文がいくつか報告されており、両者の併用が最も診断能が高いという報告もされています。しかしながら全世界を通じて、画像上の消失(DLM)に対してCTとDW-MRI、造影MRIとを組み合わせてDLMの診断精度を前向きに評価した報告は未だありません。
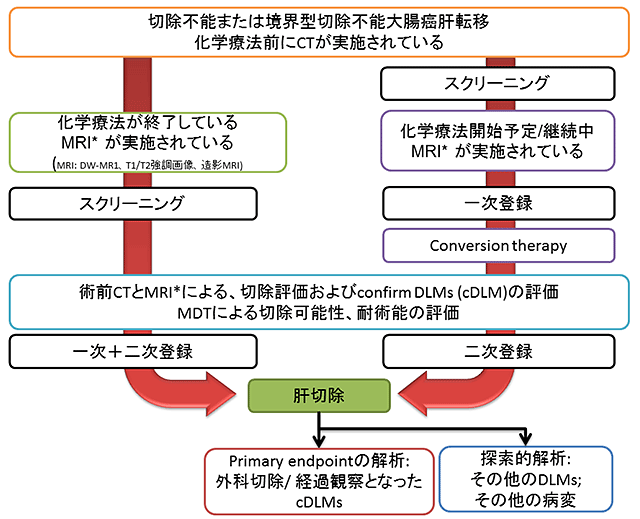
DREAM studyの概要
DREAM study:EORTC1527-GITCG-IG/JCOG1609-INT (Diffusion-weighted magnetic resonance imaging assessment of liver metastasis to improve surgical planning study)
化学療法にて消失した大腸がん肝転移病変に対するDW-MRIの術前診断能の妥当性に関する研究(UMIN000024890)
DREAM studyはCTおよびMRI(DW-MRI、T1/T2強調MRI、造影MRI)により切除不能(unresectable)または境界型切除不能(borderline resectable)大腸がん肝転移と診断された方が対象となります。まず化学療法を実施しますが、登録時点で化学療法の開始/継続が必要か、あるいは既に終了しているかどうかで、2通りの登録方法があります。
一次登録時点で大腸がん肝転移に対する化学療法の開始/継続が必要な場合は、登録後に化学療法が開始/継続されます。CT、MRIの診断の情報を元に、Multidisciplinary team(MDT)で外科的切除可能と判断されると、二次登録適格例となります(下図の右側矢印)。登録時点で既に化学療法が終了していて、外科的切除可能と判断された患者は、一次登録と二次登録が同時に実施されます。化学療法などの情報は登録後に後ろ向きに集められます(下図の左側矢印)。
次に外科的手術を受けた全患者の中から、CTとMRI(DW-MRI、T1/T2強調MRI、造影MRI)の全ての画像で消失が確認されたcDLM(confirmed disappearing liver metastases)の情報を収集します。cDLMが外科的に切除された場合は病理学的な遺残腫瘍細胞の有無を評価し、cDLMが外科的に切除されず経過観察となった場合は術後の再発の有無を画像検査で評価します。術前にcDLMと診断された病変の中で、病理学的に遺残腫瘍細胞のない病変あるいは術後2年間再発のない病変の割合をprimary endpointとして評価します。
DREAM studyの臨床データはVista TrialsというWeb患者登録システムを通じて全てEORTCデータセンターに集められます。JCOGデータセンターは日本の各参加施設の倫理審査委員会の承認状況の把握と、データ入力についての督促、DREAM studyに関する質問の対応などの調整業務を行い、その結果を定期的にEORTCデータセンターに報告します。
 Conversion therapy:手術で切除できないがんを化学療法で小さくして根治切除を目指す治療法
Conversion therapy:手術で切除できないがんを化学療法で小さくして根治切除を目指す治療法cDLM(confirmed disappearing liver metastases):画像上消失した肝転移病変
MDT(multidisciplinary team):腫瘍内科医、肝臓専門外科医、大腸専門外科医、消化器専門の画像診断医から
成る多職種医療チーム
国際共同研究を推進する意義
研究期間が短期化し、新規治療開発が早期に患者さんに還元
外科手術手技の品質管理など臨床研究における日本の先進的ノウハウをグローバルに展開
このような国際共同臨床研究を実施するには、研究計画の立案から各国の規制要件への対応を含む実施に至るまで、一貫して研究支援を行う体制も欠かせません。DREAM studyはAMEDの「国際共同臨床研究実施推進事業」のメインプロジェクトの1つとして、国立がん研究センター中央病院 臨床研究支援部門の国際研究支援室が支援を行います。
今後の展望
参加施設
日本国内
- 神奈川県立病院機構神奈川県立がんセンター
- 国立がん研究センター中央病院
- 山形県立中央病院
- 群馬県立がんセンター
- 自治医科大学附属さいたま医療センター
- 千葉県がんセンター
- 東京医科歯大学
- 新潟県立がんセンター新潟病院※
- 岐阜大学医学部
- 静岡県立静岡がんセンター
- 大阪府立病院機構大阪府立成人病センター
- 県立広島病院
※患者登録未開始施設(2017年2月中には登録開始予定です)
欧州
- オーストリア
-
- Der Wiener Krankenanstaltenverbund - Krankenanstalt Rudolfstiftung
- Medizinische Universität Innsbruck
- Medical University of Vienna
- フランス
-
- Institute Bergonié
- Centre Leon Berard
- Gustave Roussy
- イタリア
-
- Hospital of Citadella
- Universita Degli Studi Di Siena
- イギリス
-
- Aintree University Hospital Trust
- Royal Marsden NHS Foundation Trust
- ベルギー
-
- UZ Ghent
- UZ Leuven
- ポーランド
-
- M Sklodowska-Curie Memorial Cancer Center
- Medical University of Lublin
- セルビア
-
- Military Medical Academy
- Oncology Institute of Vojvodina
米国
- Oregon Health and Science University Knight Cancer Institute
- The University of Texas MD Anderson Cancer Center
参考
日本臨床腫瘍研究グループ(Japan Clinical Oncology Group; JCOG)について
JCOGは、公的研究資金(国立がん研究センター研究開発費、厚生労働科学研究費など)により運営される、がん多施設共同研究グループです。JCOGの目的は、前向きの多施設共同臨床試験実施により有効性の高い標準治療(最も効果的な治療)を確立して、その研究成果を国内外に発信し、がん患者さんの診療の質と治療成績の向上を図ることです。開発を目指す新しい治療法には、抗腫瘍薬の組み合わせによる薬物療法、外科手術や放射線治療、内視鏡治療に加えて、これらを併用した集学的治療があります。16の専門分野別研究グループが実施するJCOG試験には、年間約3,000人のがん患者さんが参加されています。また、国内外の他の臨床試験グループとの共同研究も積極的に進めており、2012年からは米国のNorth Central Cancer Treatment Group / Cancer and Leukemia Group B(NCCTG/CALGB)と高齢の切除不能大腸がん患者に対する化学療法でオキサリプラチンという抗がん剤を追加する意義について評価する共同研究、2008年からは韓国胃がん学会と切除不能胃がん患者に対する化学療法前に胃切除を行う意義について評価する共同研究を実施してきました。
European Organisation for Research and Treatment of Cancer(EORTC)について
EORTCは、様々な国、組織からの研究資金により運営される30か国、600以上の参加施設からなる欧州最大のがん多施設共同臨床研究グループです。18の専門別分野グループおよび3つの基礎研究・トランスレーショナル研究グループが、研究者主導の臨床研究と、企業からの受託研究の両者を実施しており、年間約5,000~6,000人のがん患者さんが参加されています。米国や、欧州の他の研究グループ、オーストラリア等と数々の共同研究を手がけています。
論文
Japanese Journal of Clinical Oncology
Collaboration between EORTC and JCOG—how to accelerate global clinical research partnership
Kozo Kataoka, Kenichi Nakamura, Carmela Caballero, Serge Evrard, Anastassia Negrouk, Manabu Shiozawa, Laurence Collette, Haruhiko Fukuda, and Denis Lacombe
研究費
国立研究開発法人日本医療研究開発機構(AMED)国際共同臨床研究実施推進事業
代表者:国立がん研究センター中央病院 西田 俊朗
国立研究開発法人日本医療研究開発機構(AMED)革新的がん医療実用化研究事業
代表者:地方独立行政法人神奈川県立病院機構神奈川県立がんセンター 塩澤学
お問い合わせ先
国立研究開発法人国立がん研究センター
〒104-0045 東京都中央区築地5-1-1
中央病院 臨床研究支援部門 研究企画推進部 国際研究支援室 中村健一
TEL:03-3542-2511(代表) FAX:03-3547-1002
E-mail:kennakam“AT”ncc.go.jp
企画戦略局 広報企画室
TEL:03-3542-2511(代表) FAX:03-3542-2545
E-mail:ncc-admin“AT”ncc.go.jp
国立研究開発法人日本医療研究開発機構(AMED)
臨床研究・治験基盤事業部 臨床研究課
〒100-0004 東京都千代田区大手町1-7-1
TEL:03-6870-2229
E-mail:chukaku-rinsho“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
掲載日 平成29年2月1日
最終更新日 平成29年2月1日


