千葉県こども病院/千葉県がんセンター(研究所)国際連携による、拡張型心筋症をきたす新しい病因遺伝子の発見
プレスリリース
千葉県こども病院
千葉県がんセンター
国立研究開発法人 日本医療研究開発機構
千葉県こども病院遺伝診療センター・代謝科/千葉県がんセンター研究所の研究グループは、埼玉医科大学、順天堂大学と共同研究で、ミトコンドリア病[※1]を対象とした新規病因遺伝子の同定・病態解明研究や創薬研究を進めています。この度、拡張型心筋症[※2]を呈した千葉県内の患者さんにおいて、TOP3A遺伝子を新しい病因遺伝子として同定しました。本遺伝子の異常により染色体の分離異常が引き起こされた結果ミトコンドリア障害が起こり、心筋症などの症状を引き起こすことを証明しました。
さらに同様の症状を呈する症例が他国でも見つかり、この度、英国・デンマーク・米国・サウジアラビア・トルコ・スペイン等の国際共同論文として発表しましたので、報告いたします。
論文発表日
平成30年7月27日0時(現地時間7月26日午前11時)
(米国人類遺伝学会雑誌:The American Journal of Human Genetics)
概要
ミトコンドリア心筋症は小児の心筋症全体の約3%を占め、また小児ミトコンドリア病の20~40%に心筋症を合併することが知られている。しかしながら、ミトコンドリアDNAおよび核DNAにコードされる多様な遺伝子異常が原因となること、原因不明の心筋症とされている症例において本症の検索が十分なされていないことなどの理由により、ミトコンドリア心筋症の全容、病態は十分に解明されていない。
我々は、低出生体重、成長障害、拡張型心筋症を呈した千葉県内の症例に対して包括的遺伝子解析を行い、新しい病因遺伝子としてTOP3A遺伝子を同定した。同様の症状を呈しTOP3A遺伝子異常を認めた症例は、本邦以外にも米国、アラブ首長国連邦、シリア、スペイン、サウジアラビアなどの計9症例においても発見され、この度、国際共同論文として米国人類遺伝学会雑誌に報告した。
TOP3Aは、減数分裂や相同染色体の組み換えによるDNA複製(姉妹染色分体交換[※3])の際に、染色体の適切な分離を促進する重要な酵素の一つである一方、ミトコンドリアDNAの複製にも関与しているため、TOP3A異常症においては重篤な成長障害につながる染色体分離障害や、ゲノムの不安定性、また心筋症などのミトコンドリア障害を引き起こす。
今回の国際連携による新しい原因遺伝子の発見は、心筋症を呈する成因の理解、ミトコンドリア障害を引き起こすさらなる病態解明の進展、国際的な新規治療法の開発等につながるものと期待される。
※当該研究は、国立研究開発法人日本医療研究開発機構(AMED)「難治性疾患実用化研究事業」の支援により行われました。
発表のポイント
- 低出生体重、成長障害、拡張型心筋症などを呈する症例に対して包括的遺伝子解析を行い、新規病因遺伝子としてTOP3A遺伝子を同定し、英国・デンマーク・米国・サウジアラビア・トルコ・スペイン等との国際共同論文として米国人類遺伝学会雑誌(The American Journal of Human Genetics)に報告した。
- TOP3A異常症では姉妹染色分体交換が亢進し、異常な相同組み換えや有糸分裂の障害が起こり、染色体の分離異常やゲノムの不安定性が生じることで、胎児期からはじまる重篤な成長障害を引き起こす。
- TOP3AはミトコンドリアDNAの複製・分離にも関与しており、TOP3A異常症では拡張型心筋症などのミトコンドリア障害による症状を合併する。
- 小児ミトコンドリア病の20~40%に心筋症を合併することが知られているが、多様な遺伝子異常が原因となることから、本症の全容、病態は十分に解明されていない。今回の国際連携による原因遺伝子の発見が、ミトコンドリア心筋症の病態解明の進展や新規治療法の開発などにつながるものと期待される。
研究の背景
千葉県こども病院/千葉県がんセンター(村山圭 部長)はこれまで順天堂大学・難病の診断と治療研究センター(岡﨑康司 教授・センター長)、埼玉医科大学小児科(大竹明 教授)と共同で、2007年から希少難病であるミトコンドリア病の分子診断を手がけてきました。2015年度から日本医療研究開発機構(AMED)による難治性疾患実用化研究事業「ミトコンドリア病診療の質を高める、レジストリシステムの構築、診断基準・診療ガイドラインの策定および診断システムの整備を行う臨床研究」、2016年から「創薬を見据えた、ミトコンドリア病の新規病因遺伝子の発見とその病態解明」、2017年から「ミトコンドリア病診療マニュアルの改訂を見据えた、診療に直結させるミトコンドリア病・各臨床病型のエビデンス創出研究」を通して、日本におけるミトコンドリア病診療の基盤構築に寄与してきました。特にミトコンドリア病の新規病因遺伝子を見つけ、病態解明や創薬につなげていくことはミトコンドリア病診療の中でも重要な部分になります。
今回発見されたミトコンドリア病を引き起こす新しい遺伝子は、ミトコンドリア心筋症を呈する遺伝子であり、ミトコンドリア病全体の7%に相当します(図1)。これまで肥大型心筋症をきたすミトコンドリア病の新規病因遺伝子としては、C1QBP, GTPBP3, COQ4, ECHS1, QRSL1等を報告してきました。今回は拡張型心筋症をきたすミトコンドリア病の新規遺伝子としてTOP3A遺伝子を本邦の症例で発見し、同時に海外でも9症例存在していることがわかり、国際共同論文としての発表に至りました。
これまで、当研究グループでは図2のように国際連携による新しい病因遺伝子の発見を行ってきています(図2)。希少難病における国際連携はきわめて重要であり、しっかりした診断システム体制の維持や今後も登録制度などの充実などに取り組んでいきます。
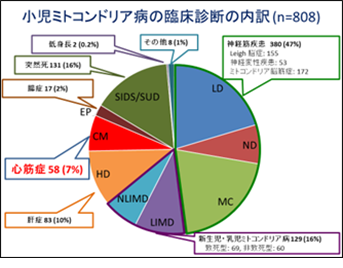
図1. わが国における小児ミトコンドリア病の臨床診断の内訳

図2. これまで行ってきた国際連携による新規病因遺伝子の発見
成果の概要
低出生体重、成長障害、拡張型心筋症を呈した症例に対し包括的遺伝子解析、および候補遺伝子の機能解析を行い、これまで心筋症の原因遺伝子として報告のなかったTOP3A遺伝子を同定しました。TOP3Aの異常は染色体の分離異常や、ゲノムの不安定性の原因となるだけでなく、ミトコンドリアDNAの複製・分離の異常も引き起こすことで、著明な成長障害、ミトコンドリア心筋症の原因となります。本邦以外にも、同様の症状を呈するTOP3A異常症例は、米国、アラブ首長国連邦、サウジアラビア、シリア、スペインにおいて発見され、国際共同論文として米国人類遺伝学会誌に報告しました。
TOP3A異常症の特徴
TOP3A異常症は、子宮内発育遅延、小頭症、カフェオレ斑、成長障害、発達遅滞、拡張型心筋症などを呈す疾患です。全10症例における臨床症状の内訳は、胎児期からはじまる成長障害(10/10)、カフェオレ斑(8/10)、拡張型心筋症 (4/10)、肥大型心筋症 (1/10)、発達遅滞(4/10)、皮下脂肪の減少 (3/10)、胃食道逆流症 (2/10)、反復性感染症 (3/10) となっています。
特に成長障害は胎児期より顕著であり、全ての症例が低出生体重児でした(平均出生体重 -2.6±0.9SD)。また、出生後の成長障害も明らかであり、現在の体重、身長および頭囲は、同年齢の平均値と比較すると著明に低下していました(平均体重 -4.8±1.8SD、平均身長 -3.9±1.0SD、平均頭囲 -4.0±1.2SD)(図3)。
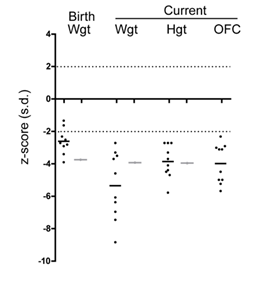
図3. TOP3A異常症の出生体重および現在の身体計測値
心筋症は10例中5例で認め、4例が拡張型心筋症で、1例が肥大型心筋症でした。うち2例は致死的な経過を辿り、10代前半で亡くなっております。本邦の症例も拡張型心筋症の進行を認めましたが、心臓移植術が行われ生存しております。
本邦の症例においては、骨格筋を用いた解析で87%のミトコンドリアDNAの枯渇を認め、病理学的検査ではシトクロムcオキシダーゼ(COX)の欠損を認めました。
TOP3A遺伝子変異と検証実験
全症例でエクソーム解析が行われ、TOP3A遺伝子の変異が同定され、そのうち4/5種類の変異がフレームシフト変異でした(図4A)。in silico解析では、これらの変異はTOP3Aの発現を低下させ、TOP3A活性に影響を与えると予測されました。皮膚由来線維芽細胞を用いたウエスタンブロッティングでは、患者由来細胞でTOP3Aの発現低下を認めました(図4B)。
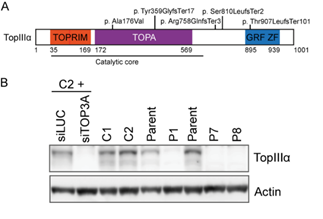
図4. TOP3A変異とタンパク質発現
姉妹染色分体交換の亢進
減数分裂や相同組み換えによるDNA複製時には、図5のように2つの二本鎖DNAが4本のDNA鎖を共有する、ダブルホリデイジャンクション(dHJ)と呼ばれる中間体を形成します。その後、dHJは解きほぐされるか(解消)、ホリデイジャンクション(HJ)開裂酵素により切断を受けることで、交差型または非交差型のDNAが複製されます。TOP3AはBLM、RMI1およびRMI2とともにBTRR複合体を形成して、減数分裂や相同組み換えによるDNA複製時に、中間体であるHJ構造を解消するヘリカーゼ活性を持ちます。
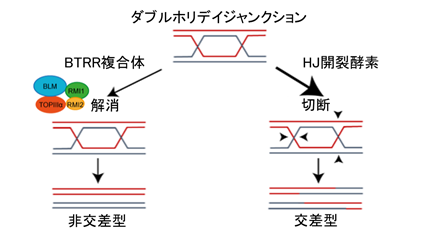
図5. 相同組み換えによるDNAの複製
BTRR複合体の構成タンパク質の1つであるBLMの障害は、Bloom症候群[※4]の原因となることが知られています。Bloom症候群ではBTRR複合体が機能しなくなるため、dHJが解消されないため、姉妹染色分体交換の亢進が起きることが分かっています。TOP3A異常症においても、BTRR複合体の機能が障害されるために、姉妹染色分体交換の亢進が確認されました(図6A)。本邦の症例(P5)を含め、患者由来細胞においては、コントロール細胞または両親由来の細胞の3~6倍の姉妹染色分体交換の亢進を認めました(図6B)。
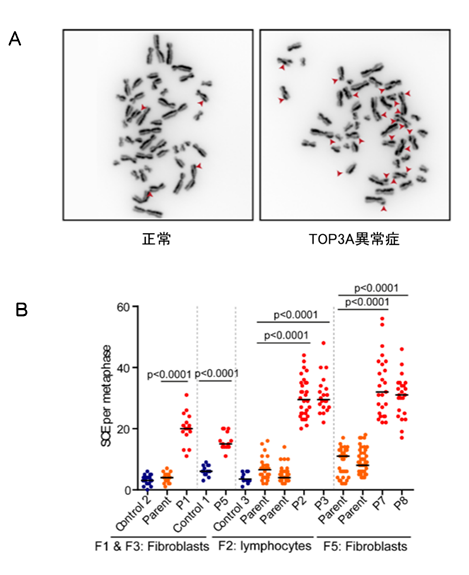
図6. 姉妹染色分体交換の亢進
染色体の分離異常とゲノムの不安定性
dHJの解離異常は、有糸分裂における染色体分離を妨げるような、持続的な姉妹染色分体のもつれを引き起こすと考えられます。TOP3A異常細胞では、クロマチンブリッジやラギングクロマチンの発現、およびultrafine DNA bridgeと呼ばれる微細な染色体ブリッジの発現が亢進しており、染色体分離の障害が確認されました(図7A, B)。また染色体分離障害の結果、小核を有する細胞の増加が確認されました(図7C)。G1期の細胞においては、DNA損傷応答タンパク質である53BP1陽性の小核の発現上昇が認められました(図7D)。以上より、TOP3A異常細胞におけるdHJの解離異常は、異常な相同組み換えや、有糸分裂の障害の原因となると考えられます。
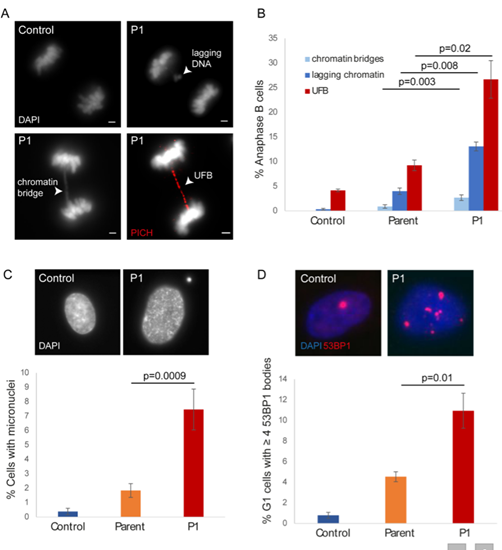
図7. 染色体の分離異常とゲノムの不安定性
まとめ
TOP3Aは、減数分裂や相同染色体の組み換えによるDNA複製の際に、染色体の適切な分離を促進する重要な酵素の一つである一方、ミトコンドリアDNAの複製にも関与しているため、TOP3A異常症においては重篤な成長障害につながる染色体分離障害や、ゲノムの不安定性、また心筋症などのミトコンドリア障害を引き起こします。
今回の国際連携による新しい原因遺伝子の発見は、心筋症を呈する成因の理解、ミトコンドリア障害を引き起こすさらなる病態解明の進展、国際的な新規治療法の開発等につながるものと期待されます。本研究に係わる論文・学会発表
- 論文
- Martin CA, Sarlós K, Logan C, Thakur RS, Parry D, Bizard AH, Leitch A, Cleal L, Ali NS, Al-Owain MA, Allen W, Altmüller J, Aza-Carmona M, Barakat BAY, Barraza-García J, Begtrup A, Bogliolo M, Cho MT, Cruz-Rojo J, Dhahrabi HAM, Elcioglu NH, GOSgene, Gorman GS, Jobling R, Kesterton I, Kishita Y, Kohda M, Stabej PLQ, Malallah AJ, Nürnberg P, Ohtake A, Okazaki Y, Pujol R, Ramirez MJ, Revah-Politi A, Shimura M, Stevens P, Taylor RW, Turner L, Williams H, Wilson C, Yigit G, Zahavich L, Alkuraya FS, Surralles J, Iglesais A, Murayama K, Wollnik B, Dattani M, Heath KE, Hickson ID, Jackson AP. Mutations in TOP3A cause a Bloom’s syndrome-like disorder, Am J Hum Genet.2018
- 学会
- Shimura M, Murayama K, et al. Identification of novel mitochondrial cardiomyopathy with elevated sister chromatid exchanges: TOP3A deficiency, JSIMD, 2018, Nov 8-10, Gifu, Japan.
用語解説
- ※1ミトコンドリア病
- ミトコンドリア病とは、ミトコンドリアの働きが低下することが原因で起こる病気の総称。エネルギー代謝系(ミトコンドリア呼吸鎖)の先天代謝異常症である。出生 5,000人に 1人の割合で発症し、いかなる症状、いかなる臓器・組織、何歳でも、いかなる遺伝形式でも発病し得る。特に幼少時期発症例は症状が多彩で重篤致死の症例が多い。MELASは学童期~成人期に多く、m.3243A>Gが8割を占める。根治的治療法がなく、対症的治療法にとどまる。
- ※2 拡張型心筋症
- 左心室の著明な拡張と、収縮能が著明に低下した心筋疾患を拡張型心筋症という。心拍出量の低下に伴い心不全症状が出現し、心臓移植術を必要とする症例もある。
- ※3 姉妹染色分体交換
- S期に複製された2コピーの娘DNAは、M期に凝集して染色体を形成する。この凝集した娘DNAをそれぞれ姉妹染色分体と呼ぶ。娘DNAは相同な領域を相互に交換することがあり、これを姉妹染色分体交換という。
- ※4 Bloom症候群
- TOP3AとともにBTRR複合体を形成するBLM遺伝子の異常により発症する。胎児期からはじまる成長障害、日光過敏性紅斑、免疫不全症、早老症、悪性腫瘍の合併を特徴とする疾患である。
お問い合わせ先
本件に関するお問い合わせ先
千葉県こども病院
事務局医事経営課
Tel:043-292-2111
AMED事業に関するお問い合わせ先
国立研究開発法人日本医療研究開発機構
戦略推進部 難病研究課
Tel:03-6870-2223
E-mail:nambyo-info"AT"amed.go.jp
※E-mailは上記アドレス”AT”の部分を@に変えてください。
関連リンク
掲載日 平成30年7月30日
最終更新日 平成30年7月30日


