B型肝炎ウイルスの治療薬候補「ペボネジスタット」を新たに同定
プレスリリース
東京大学
日本医療研究開発機構
発表者
關場 一磨(東京大学医学部附属病院 消化器内科/東京大学大学院医学系研究科 内科学専攻 消化器内科学 医学博士課程3年生)
大塚 基之(東京大学医学部附属病院 消化器内科/東京大学大学院医学系研究科 内科学専攻 消化器内科学 講師)
小池 和彦(東京大学医学部附属病院 消化器内科/東京大学大学院医学系研究科 内科学専攻 消化器内科学 教授)
発表のポイント
- B型肝炎ウイルス(注1)の複製を阻害する宿主タンパクSmc5/6(注2)のウイルスタンパクHBxによる分解を防ぐ薬剤候補としてペボネジスタットを同定しました。
- B型肝炎治療に広く用いられている核酸アナログ製剤(注3)では抑えられないウイルスRNAの産生をペボネジスタットが強力に抑制することを確認しました。
- 現在の医療では達成困難であるB型肝炎の治療目標「Functional cure」(HBs抗原陰性化)への展望を新たに拓くことが期待されます。
発表概要
B型肝炎ウイルス感染者は世界中で20億人、そのうち持続感染者は2.57億人、さらに年間90万人がB型肝炎ウイルス関連疾患で死亡しています。B型肝炎の克服は日本国内のみならず世界的な重要課題です。B型肝炎の長期予後改善のために、ウイルスタンパクであるHBs抗原の陰性化「Functional cure」が治療目標として掲げられていますが、既存のB型肝炎治療薬では達成困難であり、新薬の登場が切望されています。そうした中、ウイルスタンパクHBxによる、宿主ユビキチン・プロテアソーム系を介した宿主タンパクSmc5/6の分解がもたらすウイルスの複製促進機構が明らかとなり、新たな治療標的として注目されていました。そこで、東京大学医学部附属病院 消化器内科の關場一磨 大学院生、大塚基之 講師、小池和彦 教授らの研究グループは、Smc5/6タンパクが宿主ユビキチン・プロテアソーム系(注4)によって分解されること、また、このユビキチン化にはネディレーション(注5)によるユビキチン化酵素の活性化が必要なことに注目し、ネディレーション阻害薬であるペボネジスタット(Pevonedistat)がB型肝炎の新規治療薬となり得ると考えました。そして実際に、ペボネジスタットはネディレーションを阻害することによって、Smc5/6タンパクの分解を阻害して機能を回復し、ウイルスRNAをはじめとしたウイルス産物量を強力に抑えるという、既存のB型肝炎治療薬には無い効果を有することを、初代ヒト肝細胞(注6)を用いた検討などで明らかにしました。ペボネジスタットは白血病領域を中心とした悪性腫瘍の治療薬として開発が進められており、今後早期のB型肝炎治療薬への応用が期待されます。本研究成果は、米国肝臓病学会誌『Hepatology』に掲載されるのに先立ち、米国東部時間12月26日にオンライン版にて公開されました。なお、本研究は日本医療研究開発機構(AMED)肝炎等克服実用化研究事業の肝炎等克服緊急対策研究事業(研究開発課題名「B型肝炎ウイルスRNAと相互作用する宿主因子の網羅的同定とその制御による病態制御法開発」研究代表者:大塚基之)および文部科学省科学研究費補助金などの支援により行われました。
発表内容
研究の背景
B型肝炎の治療目標は「Functional cure」(HBs抗原陰性化)とされていますが、既存薬では達成困難です。これは、現在広く使われている抗ウイルス薬である核酸アナログ製剤が、ウイルスDNAの産生は効率的に阻害するものの、感染した肝細胞の核内にウイルスDNA複製の鋳型として存在するcccDNA(注7)からのウイルスRNA産生を抑制することが原理的にできないためと考えられています。したがって、ひとたび核酸アナログ製剤の服用を始めると一生服薬を継続せざるを得ないばかりか、服用していてもB型肝炎ウイルス関連の発癌を来すことがあり、新しい作用機序の薬の開発が望まれています。
B型肝炎ウイルスの効率的な複製にウイルスタンパクHBxが強く関わっていることは以前から知られていましたが、その制御機構の詳細は明らかではありませんでした。本研究グループは、「HBxタンパクは、宿主ユビキチン・プロテアソーム系を利用し、本来はウイルスRNA転写に抑制的に働くはずの宿主タンパクSmc5/6を分解してウイルスRNAの転写を活性化させている」という最近の報告(Decorsière A. et al. Nature (2016). Murphy C. M. et al. Cell Rep. (2016).)に着目しました。特に、ここで働くCRL4というユビキチン化酵素がネディレーションによる修飾が活性化に必須なものであることに着目し、最近開発されたネディレーション阻害剤であるペボネジスタットが抗ウイルス効果を有するのではないかと仮説を立てました。
研究内容
まず、HBx発現細胞にペボネジスタットを投与してSmc5/6タンパクの発現回復効果を検証したところ、その有意な効果を確認しました。次に、ミニサークルDNA技術(注8)を用いてウイルスのcccDNAを模倣するDNA分子を作製し、それに対するペボネジスタットの効果を見たところ、ウイルスRNA転写が有意に抑制されました。また、終止コドンを挿入してHBxタンパクの発現を欠損させた変異型の擬似cccDNAでは、このペボネジスタットによるウイルスRNA転写抑制効果は失われることから、ペボネジスタットの効果はHBxタンパクに依存することが確認されました。
さらに、初代ヒト肝細胞を用いたB型肝炎ウイルス感染系において、ペボネジスタットはSmc5タンパクの発現回復をもたらし、ウイルスRNAをはじめ、ウイルスタンパク、ウイルスDNA、cccDNA量を有意に低下させる(図1)ことが確認されました。
以上のことから、ペボネジスタットは、ネディレーション阻害を通したSmc5/6タンパクの発現回復という作用機序を持つ新規のB型肝炎治療薬となる可能性が示されました(図2)。
社会的意義・今後の予定
これらの結果は、ペボネジスタットが既存のB型肝炎治療薬では達成困難な「Functional cure」(HBs抗原陰性化)を実現する可能性を有していることを示しています。また、悪性腫瘍の治療現場では、治療に伴うB型肝炎ウイルス再活性化(注9)が大きな問題となっており、ペボネジスタットはそうした問題を解決し得る悪性腫瘍治療の選択肢としても期待しうる可能性が作用機序から推定されます。
今後は、これらのデータをもとに、動物モデルなどでの検討を加えて、新たな作用機序を持つB型肝炎治療薬候補としてヒトへの応用の可能性を探っていきたいと考えています。
発表雑誌
- 雑誌名:
- Hepatology
- 論文タイトル:
- Pevonedistat, a first-in-class NEDD8-activating enzyme inhibitor, is a potent inhibitor of hepatitis B virus
- 著者:
- Kazuma Sekiba, Motoyuki Otsuka*, Motoko Ohno, Mari Yamagami, Takahiro Kishikawa, Takahiro Seimiya, Tatsunori Suzuki, Eri Tanaka, Rei Ishibashi, Kazuyoshi Funato, Kazuhiko Koike(* Corresponding Author)
- DOI番号:
- 10.1002/hep.30491
- アブストラクトURL:
- https://aasldpubs.onlinelibrary.wiley.com/doi/abs/10.1002/hep.30491
用語解説
- 注1)B型肝炎ウイルス:
- 血液や体液などを介して肝臓に感染するDNAウイルス。感染したウイルスは炎症(肝炎)を惹起し、肝硬変や肝癌の原因となる。世界保健機関(WHO)は、B型肝炎ウイルス感染者は世界中で20億人、そのうちB型肝炎ウイルス持続感染者は2.57億人、さらに年間90万人がB型肝炎ウイルス関連疾患で死亡していると報告し、その克服を重要課題として挙げている。
- 注2)Smc5/6:
- Structural maintenance of chromosomes 5/6の略。染色体の高次構造維持などに関わるとされる宿主タンパクのひとつ。B型肝炎ウイルスのcccDNAにも結合し、ウイルスRNA転写の強力な阻害因子となることが明らかにされた。
- 注3)核酸アナログ製剤:
- B型肝炎の治療に広く用いられているウイルスDNA複製阻害剤。B型肝炎ウイルスはその生活環の中で、プレゲノムRNAからDNAへの逆転写を行うが、核酸アナログ製剤はウイルスDNAポリメラーゼ/逆転写酵素による基質の取り込みを競合的に阻害してDNA鎖の伸長を停止することでウイルスの増殖を阻害する。エンテカビルやテノホビルがその代表薬。
- 注4)ユビキチン・プロテアソーム系:
- ユビキチンの活性化から結合、プロテアソーム(タンパク分解酵素)によるタンパク分解までを担う一連の生化学経路。ユビキチン活性化酵素(E1)、ユビキチン結合酵素(E2)、ユビキチンリガーゼ(E3)の3種類の酵素の働きで、E3に選択的に識別された標的タンパクがポリユビキチン修飾を受けると、ポリユビキチン鎖が標識となって、ユビキチン修飾を受けたタンパクはプロテアソーム(タンパク分解酵素)によって分解される。
- 注5)ネディレーション:
- ユビキチンに似た小分子Nedd8が標的分子へ結合する一連の生化学経路。CRL4といったcullin型ユビキチンリガーゼはNedd8に修飾されることで活性化される。
- 注6)初代ヒト肝細胞:
- ヒトから採取された肝臓組織から培養した細胞。B型肝炎ウイルスはヒトやチンパンジーなど、感染できる宿主が限られており、一般的に研究に用いられる肝癌細胞株にも感染しないため、B型肝炎ウイルスの感染実験を行うには初代ヒト肝細胞を用いる。
- 注7)cccDNA:
- covalently closed circular DNAの略。B型肝炎ウイルスは肝細胞に侵入すると、もともと不完全環状二本鎖の形態をとっているウイルスDNAが核内に移行し、完全閉鎖環状二本鎖の形態cccDNAに変換される。cccDNAは核内に安定的に存在し続け、ウイルスRNAを作るための鋳型として働く。既存のB型肝炎ウイルス治療薬では排除が困難である。
- 注8)ミニサークルDNA技術:
- プラスミドDNAからバクテリア由来の複製開始点や抗生物質耐性遺伝子などバックボーン部分を取り除き、標的遺伝子配列のみの環状2本鎖DNA(ミニサークルDNA)を作成する技術。この技術を用いると、B型肝炎ウイルス遺伝子配列のみを完全閉鎖二本鎖の状態で合成することができ、cccDNAを模倣した状態を再現できる。
- 注9)B型肝炎ウイルス再活性化:
- 悪性腫瘍に対する化学療法などに伴う免疫機能の低下によって、急激にB型肝炎ウイルスが増殖すること。劇症肝炎による死亡例もある。キャリアや慢性肝炎と言われるHBs抗原陽性例のみならず、一過性感染後においても発症リスクがある。
添付資料
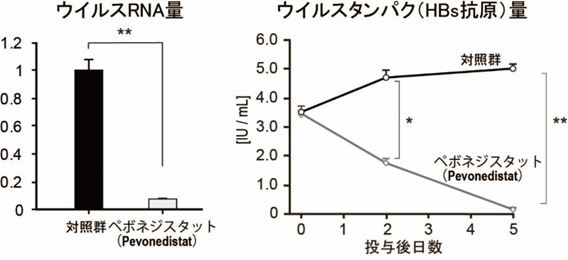
図1.初代ヒト肝細胞でのB型肝炎ウイルス感染系におけるペボネジスタットの効果
B型肝炎ウイルスを感染させた初代ヒト肝細胞に5日間連続でペボネジスタット(Pevonedistat)を投与した際のウイルスRNA量(左図)およびウイルスタンパク量(右図)の測定結果。ペボネジスタットは強力にウイルス複製を抑制する。
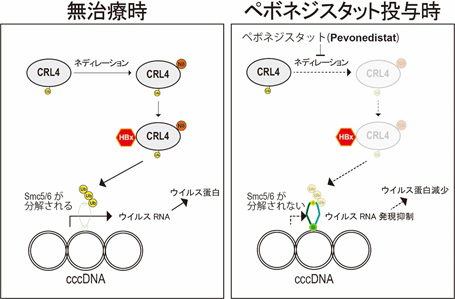
図2.ペボネジスタットによるB型肝炎ウイルスRNAの転写抑制
HBxは、宿主のユビキチン・プロテアソーム系を利用して、cccDNAからの転写を抑制する作用をもつSmc5/6複合体を分解する(左図)。ペボネジスタット(Pevonedistat)はネディレーションを阻害する結果、Smc5/6の分解を防ぐことで、cccDNAからのウイルスRNA転写を抑制すると考えられる。ウイルスRNAから翻訳されるウイルスタンパク量も減少する(右図)。(Ub:ユビキチン、N8:NEDD8)
問い合わせ先
研究に関するお問合せ先
東京大学医学部附属病院 消化器内科
大学院生 關場 一磨(せきば かずま)
電話:03-5800-8812(研究室直通)
E-mail:ksekiba-tky"AT"umin.ac.jp
講師 大塚 基之(おおつか もとゆき)
電話:03-5800-8812(研究室直通)
E-mail:otsukamo-tky"AT"umin.ac.jp
広報担当者連絡先
東京大学医学部附属病院 パブリック・リレーションセンター
担当:渡部、小岩井
電話:03-5800-9188(直通)
E-mail:pr"AT"adm.h.u-tokyo.ac.jp
AMEDの事業に関するお問い合わせ先
国立研究開発法人日本医療研究開発機構 戦略推進部 感染症研究課
(肝炎等克服実用化研究事業 担当)
電話:03-6870-2225 FAX:03-6870-2243
E-mail:hepatitis"AT"amed.go.jp
※E-mailは上記アドレス"AT"の部分を@に変えてください。
関連リンク
掲載日 平成31年1月11日
最終更新日 平成31年1月11日


