脂肪肝から肝炎発症の引き金となる細胞死を解明―脂肪性肝炎の予防や治療法の開発に期待―
プレスリリース
国立国際医療研究センター
日本医療研究開発機構
要旨
非アルコール性脂肪性肝炎(NASH)は、アルコールをほとんど飲まない人が、脂肪肝から肝炎を発症し、やがては肝硬変、肝癌へと進展しうる疾患です。メタボリックシンドロームの肝臓の表現型の一つと考えられており、我が国では約200万人が罹患していると推定されていますが、未だ有効な治療法は確立されていません。特に脂肪肝の中でどのような細胞死が起こり、NASH発症への引き金を引いているのかについてはこれまで不明でした。
今回、国立国際医療研究センター研究所・細胞組織再生医学研究部の鶴崎慎也研究員、田中稔室長らを中心とする研究グループは、マウスを用いた研究から、フェロトーシスと呼ばれる特殊な細胞死が、脂肪肝からNASH発症への引き金を引いていることを明らかにしました。これまでにNASHの病態を模倣するモデルマウスは数多く報告されていますが、田中室長らは、コリン欠乏エチオニン添加食餌を投与するモデルマウスでは極めて短期間に脂肪肝となり肝炎を発症することに着目し、その際に起こる細胞死について詳しく調べました。その結果、鉄依存的、過酸化脂質依存的な細胞死として報告されていたフェロトーシスが、脂肪肝内で最も早く起きる細胞死であることを突き止めました。また、フェロトーシスを阻害することで肝炎の発症をほぼ完全に抑制できることを示しました。本研究成果はNASH発症におけるフェロトーシスの関与を初めて明確に示したものであり、今後、フェロトーシス研究を通して、NASHの新しい予防法や治療法の開発につながることが期待されます。
なお、本研究は、東邦大学 中野裕康教授、北里大学 今井浩孝教授、東京大学 宮島篤教授らとの共同研究により、日本医療研究開発機構(AMED)の革新的先端研究開発支援事業(AMED-CREST)「生体組織の適応・修復機構の時空間的解析による生命現象の理解と医療技術シーズの創出」研究開発領域における研究開発課題「NASHにおける肝リモデリングを制御する細胞間相互作用の解明と革新的診断・治療法創出への応用」(研究開発代表者:田中稔)、文部科学省 新学術領域「ダイイングコード ―細胞死を起点とする生体制御ネットワークの解明―」における計画研究課題「肝幹細胞による肝再生を促進するダイイングコードの解明」(研究代表者:田中稔)の支援を受けて実施されました。その研究成果は、英国科学誌「Cell Death & Disease」に、2019年6月18日午前9時(日本時間)にオンライン版で発表されます。
研究の背景
肝臓に脂肪が多く溜まった状態は脂肪肝と呼ばれ、重篤な肝臓病の原因となりうることが知られています。従来、肝臓病といえば過剰な飲酒やウイルス感染を原因とする疾患と捉えられてきましたが、近年、あまりお酒を飲まない、または飲酒歴がないにも関わらず脂肪肝を背景に肝炎を発症し、やがては肝硬変や肝癌に進展しうる非アルコール性脂肪性肝炎(NASH)が注目されています。現在、我が国のNASH患者数は約200万人、炎症を伴わない脂肪肝からNASHまでを含む一連の肝疾患(NAFLD)は1,000万人以上であると推定されており、社会的にも極めて注目度の高い疾患となっています。今後もその患者数は増加していくことが予想されることから、予防法や治療法の開発は喫緊の課題となりますが、有効な治療法は未だ確立されていません。一方、炎症の原因となりうる細胞死の研究分野では、近年、細胞が自ら死のプログラムを実行することで死に至る「計画的細胞死」と呼ばれる現象が続々と明らかになってきており、様々な疾患の発症や病態形成における計画的細胞死の役割や意義が注目されています。脂肪肝からのNASH発症では、脂肪の異常蓄積による肝細胞死の関与が指摘されていましたが、どのような細胞死が原因となっているのかについてはこれまで不明でした。
本研究の概要・意義
NASHでは、脂肪を過剰に蓄積した肝細胞が死ぬことで、肝炎が起きることが予想されたことから、本研究では、脂肪肝からNASHが発症する過程で、どのような細胞死が起きているのかを詳細に調べました。まず、細胞死の様式はアポトーシス※1とネクローシス※2(壊死)に大別されるため、肝臓内でどちらの細胞死が起きているのかを簡便に調べられる方法を確立しました(図1)。この方法を用いて、コリン欠乏エチオニン添加食餌※3によるNASHモデルマウスの肝臓を調べたところ、NASH発症後にはアポトーシスとネクローシスの両方の細胞死が混在した状態にあることがわかりました。そこで、どちらの細胞死が先に起きているのかを食餌投与後から時間を追って調べたところ、ネクローシスが先行して起きることで肝炎を発症していることが明らかとなりました。さらに詳細に、どのような様式のネクローシスがNASH発症の引き金となっているのかを調べるため、特定の細胞死のみを阻害するような遺伝子改変マウスや阻害剤を用いて検討しました。その結果、ネクロプトーシス※4と呼ばれる計画的細胞死を阻害しても、肝細胞死は抑制できずに肝炎を発症しましたが、フェロトーシス※5と呼ばれる計画的細胞死を阻害した場合、肝細胞死は抑制されるとともに、その後の炎症もほぼ完全に抑制されました。これまでに線維化や発癌といったNASH発症後の病態の進展には、ネクロプトーシスやアポトーシスといった計画的細胞死が関与するという報告はありましたが、NASH発症の直接の引き金となる細胞死については不明でした。本研究成果は、脂肪肝からNASHを発症する起点にフェロトーシスという細胞死が関与することを、モデルマウスを用いた実験系で初めて明示しただけでなく、フェロトーシスの実行分子がNASHの予防や治療のための標的となりうることを示すものです(図2)。
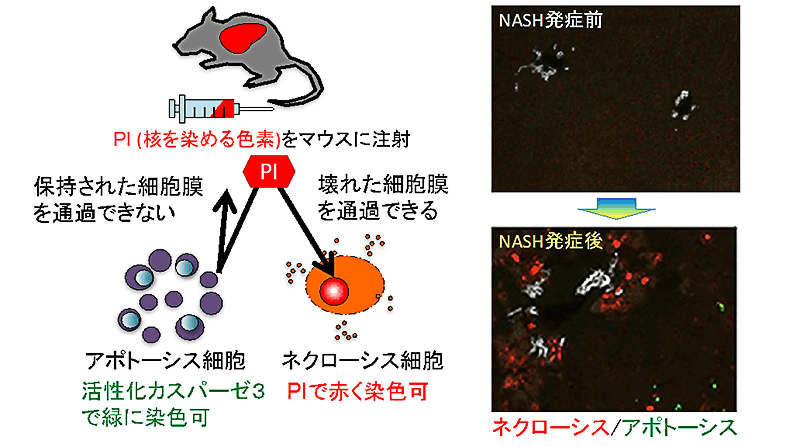
図1 ネクローシスとアポトーシスの肝臓内での検出法(左)とNASH発症後の解析像(右)
(右)NASH発症前の肝臓ではアポトーシスもネクローシスも認められないが、発症後には両細胞死が混在した状況にあることがわかる。
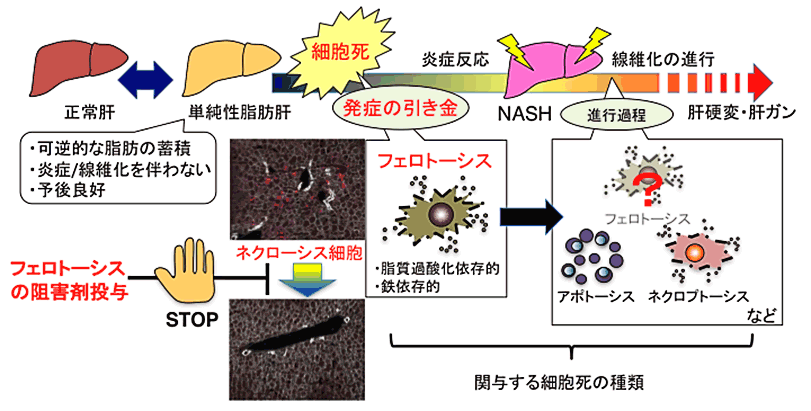
図2 脂肪肝からのNASH発症に関わる細胞死のモデル図
今後の展望
今回の結果から、NASH発症におけるフェロトーシスの関与およびその阻害による予防効果が明らかになったため、今後は他のモデルマウスでの検証や、病態進展におけるフェロトーシスの役割や阻害効果についても検討していく必要があります。今後、フェロトーシスの実行に関わる細胞内のプログラムを解読し、その関連分子が明らかになれば、それらを標的としたこれまでにないNASHの予防法や治療法の開発につながることが期待されます。
用語説明
- ※1 アポトーシス
- カスパーゼを始めとする細胞内の制御分子によって実行される細胞死様式の一つであり、核の凝縮やDNAの断片化、アポトーシス小体の形成などを特徴とする細胞死です。アポトーシスは発生過程では形態形成に関わる生理的な細胞死として起こるだけでなく、抗がん剤や放射線の照射などによっても起こることが知られています。
- ※2 ネクローシス
- 細胞内の小器官や細胞自体が膨潤、破裂することを特徴とする細胞死様式の一つです。破裂した細胞から内容物が放出されることで炎症反応が引き起こされます。計画的に進行するアポトーシスに対して、火傷や外傷などによって起こるネクローシスは偶発的かつ受動的細胞死と捉えられてきました。しかし近年、細胞内の分子に制御されたネクローシス様細胞死が存在することが続々と明らかになり、その様な細胞死は計画的ネクローシスと呼ばれています。
- ※3 コリン欠乏エチオニン添加食餌
- マウスに脂肪性肝炎を誘導するための餌の一種です。通常の餌からコリンを除き、エチオニンを添加すると、肝臓内でのフォスファチジルコリン(PC)の合成が阻害されます。通常、中性脂肪は超低比重リポタンパク質(VLDL)という形で肝臓から血液中に送り出されますが、この餌を投与すると、PCの減少によってVLDLが形成できなくなり、肝細胞内に急激に中性脂肪が蓄積して脂肪肝となります。
- ※4 ネクロプトーシス
- アポトーシスとは異なる経路の細胞内の分子により実行される細胞死様式の一つです。その実行因子であるMLKLは、3~4個が集まって多量体化し、細胞膜に穴を開けることでネクローシス様の細胞死を引き起こすと考えられています。
- ※5 フェロトーシス
- 鉄イオン依存的に制御されたネクローシス様の細胞死として、2012年にStockwellらによって提唱された細胞死様式の一つです。その実行には脂質の過酸化が重要な役割を果たすことが明らかとなっています。
発表雑誌
- 雑誌名:
- Cell Death & Disease
- 論文名:
- Hepatic ferroptosis plays a potential role as the trigger for initiating inflammation in nonalcoholic steatohepatitis
- 掲載日:
- 英国時間6月18日午前1時(日本時間6月18日午前9時)に、先行してオンライン版に掲載予定。
- 参照URL:
- https://www.nature.com/articles/s41419-019-1678-y
お問い合わせ先
本件に関するお問い合せ先
国立国際医療研究センター研究所 細胞組織再生医学研究部
細胞療法開発研究室長 田中 稔(たなか みのる)
TEL:03-3202-7181(内線2866) FAX:03-3202-7192
E-mail:m-tanaka"AT"ri.ncgm.go.jp
〒162-8655 東京都新宿区戸山1-21-1
取材に関するお問い合せ先
国立国際医療研究センター 広報企画室 広報係長
担当:三山 剛史
TEL:03-5273-5258(直通)<9時00~17時00>
E-mail:press"AT"hosp.ncgm.go.jp
AMED事業に関するお問い合わせ先
国立研究開発法人 日本医療研究開発機構
基盤研究事業部 研究企画課
〒100-0004 千代田区大手町1-7-1
TEL:03-6870-2224 FAX:03-6870-2246
E-mail:kenkyuk-ask“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
掲載日 令和元年6月18日
最終更新日 令和元年6月18日


