健康な骨の維持にはアミノ酸が重要!
プレスリリース
岐阜薬科大学
金沢大学
日本医療研究開発機構
岐阜薬科大学の檜井栄一教授(研究当時:金沢大学医薬保健研究域薬学系・准教授)らの研究グループは、金沢大学の金田勝幸教授、小川数馬准教授、東京医科歯科大学の越智広樹助教、佐藤信吾講師、松本歯科大学の小林泰浩教授、米国国立衛生研究所のYun-Bo Shi(ユンボシ)上席研究員、英国ダンディー大学のPeter M. Taylor(ピーターテイラー)教授らとの共同研究により、健康な骨の維持に重要なシグナルと新しい分子メカニズムを発見しました。
私たちのからだを構成している細胞は、アミノ酸を栄養源やタンパク質の原料として利用しています。細胞は、アミノ酸を自身で合成するだけではなく、細胞膜上に存在するアミノ酸トランスポーター(※1)を用いて細胞外からも取り入れています。これまでに、アミノ酸トランスポーターの異常が、がんや神経変性疾患、糖尿病等のさまざまな疾患の発症に関与することが知られています。しかしながら、アミノ酸トランスポーターを介した栄養環境シグナルが、どのように骨代謝に関与しているかについて、詳細は明らかになっていませんでした。
本研究グループは、アミノ酸トランスポーターの一種であるL-type amino acid transporter 1( LAT1)(※2)というタンパク質が、“健康な骨の維持”に重要な役割を果たしていることを発見し、その詳細な分子メカニズムを明らかにしました。
本成果は、骨が健康な状態で維持される仕組みについて、新しい知見や概念を提供します。さらに骨代謝異常や、骨組織の恒常性維持の破綻によって引き起こされるさまざまな運動器疾患や骨系統疾患に対する新しい知見と解決法を提供するものであり、アンメット・メディカル・ニーズ(※3)の解消にも貢献することが期待されます。
本研究成果は、2019年7月9日(米国東海岸標準時間)に米国学術雑誌『Science Signaling』のオンライン版に掲載される予定です。
研究の背景
超高齢社会を迎えたわが国において、骨粗しょう症を代表とする運動器疾患は健康寿命の短縮の大きな原因の一つになっています。従って、骨を健康な状態で維持する仕組みを明らかにすることは重要な課題となります。骨組織は、骨芽細胞による骨形成と破骨細胞による骨吸収により、骨リモデリング(※4)が繰り返されていることが知られています。本研究グループはこれまでに、グルコースやアミノ酸などの栄養環境シグナルが、骨格の形成やその恒常性の維持に重要な役割を果たしていることを明らかにしてきました。しかしながら、骨芽細胞や破骨細胞に発現しているアミノ酸トランスポーターが、どのようにして骨組織の恒常性を維持しているのかについて、詳細は明らかにされていませんでした。
研究成果の概要
LAT1は、アミノ酸トランスポーターの一種であり、ロイシンやイソロイシンなどの大型中性アミノ酸を細胞内へ輸送する働きを持っています。本研究グループは、アミノ酸シグナルによる骨組織の恒常性の維持に、LAT1が関与しているかどうかを明らかにすることを試みました。
まず、骨芽細胞特異的なLAT1不活性化マウスを作製してみたところ、骨代謝に異常は認められませんでした。一方で、破骨細胞特異的なLAT1不活性化マウスを作製してみたところ、骨量が大幅に減少することが明らかとなりました(図1)。このことから、破骨細胞に発現するLAT1を介したアミノ酸シグナルは骨代謝にとても重要であることが明らかになりました。
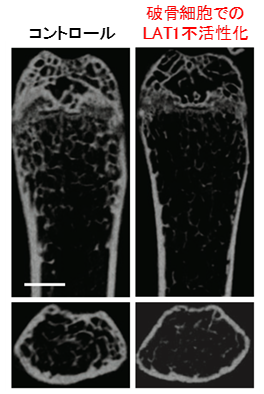
図1.成体マウス大腿骨の画像
次に、「どうして破骨細胞のLAT1を不活性化すると、骨代謝に異常がみられるのか」という疑問を解決することを試みました。そこで、 LAT1不活性化細胞における細胞機能を調べました。その結果、破骨細胞の数や大きさおよび骨吸収能が増加していることが分かりました。さらに詳細な解析を行ったところ、LAT1不活性化細胞では、mTORC1( ※5)シグナルが抑制されており、NFATc1( ※6)の発現量の増加と核内移行の亢進が観察されました。
以上のことから、破骨細胞におけるLAT1を起点とするアミノ酸シグナルは、mTORC1を介してNFATc1の発現量や機能を調節することで、骨代謝に重要な役割を果たしていることが明らかになりました(図2)。
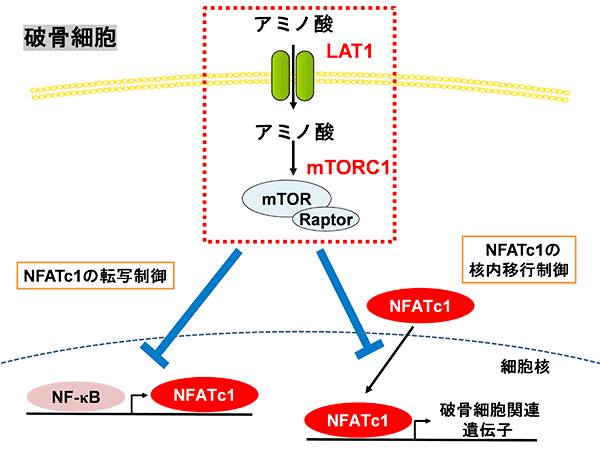
図2.LAT1/mTORC1経路によるNFATc1の転写および核内移行制御
研究成果の意義・今後の展開
本研究成果は、骨が健康な状態で維持される仕組みについて、新しい知見や概念を提供するとともに、「適切なタンパク質・アミノ酸を摂取する適切な食生活習慣は、健康な骨の維持に重要」という概念に新たなエビデンスを提供します。さらに骨代謝異常や、骨組織の恒常性維持の破綻によって引き起こされるさまざまな運動器疾患や骨系統疾患に対する新しい知見と解決法を提供し、アンメット・メディカル・ニーズの解消にも貢献することが期待されます。
本研究は、日本学術振興会科学研究費助成事業 基盤研究B(一般)「幹細胞ニッチのmTORシグナルによる造血機能制御:白血病治療展開への基礎研究」(研究代表者:檜井栄一)、基盤研究B(特設)「栄養環境センサーを分子基軸とした脊椎側弯症に対する発症・進行予測技術の開発」(研究代表者:檜井栄一)、新学術領域研究(研究領域提案型)「メカノセンサーとしての間葉系幹細胞」(研究代表者:檜井栄一)、国立研究開発法人日本医療研究開発機構(AMED)難治性疾患実用化研究事業「肋骨異常を伴う先天性側弯症の発症機序の解明」(研究開発代表者:檜井栄一)の支援を受けて行ったものです。
用語解説
- ※1 アミノ酸トランスポーター
- 細胞膜上に存在するタンパク質の一種。細胞内外のアミノ酸を輸送する働きを持つ。
- ※2 L-type amino acid transporter 1 (LAT1)
- LATと呼ばれるアミノ酸トランスポーターのグループの一つ。LAT遺伝子の一番目。
- ※3 アンメット・メディカル・ニーズ
- 未だ有効な治療方法が確立されていない疾病に対する医療への要望。
- ※4 骨リモデリング
- 破骨細胞が古い骨を壊し、次いで骨芽細胞がその欠失部を充填する現象。骨組織を常に新鮮な状態に維持するための重要な仕組みである。
- ※5 mTORC1
- 細胞の成長、増殖、生存、分化などのさまざまな機能を調節する、 複数のタンパク質による複合体。
- ※6 NFATc1
- 破骨細胞分化に必須の転写因子。破骨細胞の機能調節に関与するさまざまな遺伝子の発現を制御する。
掲載論文
- 雑誌名:
- Science Signaling
- 論文名:
- L-type amino acid transporter LAT1 inhibits osteoclastogenesis and maintains bone homeostasis through the mTORC1 pathway
(L型アミノ酸トランスポーターLAT1はmTORC1経路を介して破骨細胞形成を抑制し骨恒常性を維持する) - 著者名:
- Kakeru Ozaki, Takanori Yamada, Tetsuhiro Horie, Atsushi Ishizaki, Manami Hiraiwa, Takashi Iezaki, Gyujin Park, Kazuya Fukasawa, Hikari Kamada, Kazuya Tokumura, Mei Motono, Katsuyuki, Kaneda, Kazuma Ogawa, Hiroki Ochi, Shingo Sato, Yasuhiro Kobayashi, Yun-Bo Shi, Peter M. Taylor and Eiichi Hinoi
- (尾崎翔、 山田孝紀、 堀江哲寛、 石崎淳志、平岩茉奈美、家崎高志、朴奎珍、深澤和也、釜田ひかり、徳村和也、本野芽衣、金田勝幸、小川数馬、越智広樹、佐藤信吾、小林泰浩、ユンボシ、ピーターテイラー、檜井栄一)
- 掲載日:
- 2019年7月9日(米国東海岸標準時間)にオンライン版掲載
- DOI:
- https://doi.org/10.1126/scisignal.aaw3921
本件に関するお問い合わせ先
研究に関すること
岐阜薬科大学
教授 檜井 栄一(ひのい えいいち)
TEL:058-230-8100 E-mail:hinoi-e"AT"gifu-pu.ac.jp
広報に関すること
岐阜薬科大学
事務局庶務会計課 中尾 真一郎
TEL:058-230-8100 E-mail:syomuk"AT"gifu-pu.ac.jp
金沢大学
総務部広報室 嘉信 由紀
TEL:076-264-5024 E-mail:koho"AT"adm.kanazawa-u.ac.jp
AMED事業に関すること
国立研究開発法人 日本医療研究開発機構
戦略推進部 難病研究課
〒100-0004 東京都千代田区大手町1-7-1
TEL:03-6870-2223 E-mail:nambyo-info"AT"amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
関連リンク
掲載日 令和元年7月10日
最終更新日 令和元年7月10日


