スーパーコンピュータ「京」から迫る肺がんの分子機構―肺がんの増殖に関わる新規長鎖ノンコーディングRNAの発見―
プレスリリース
日本医療研究開発機構
ハイライト
- スーパーコンピュータ「京」と実験を統合的に用いて、肺がん細胞の増殖に重要な長鎖ノンコーディングRNA、”MYMLR”を発見しました。
- MYMLRは、代表的ながん遺伝子MYCの発現にとって重要なことを明らかにしました。
- 本研究成果に基づきMYMLRを標的とする阻害薬の開発を進めています。
概要
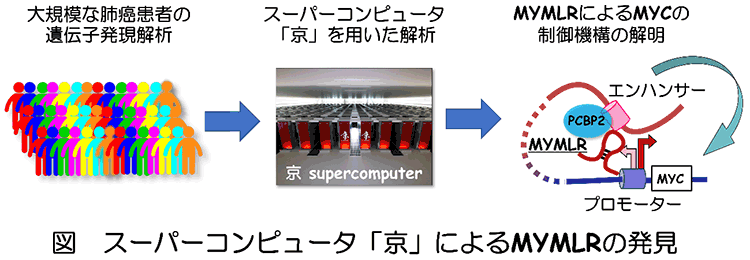
愛知県がんセンター分子診断トランスレーショナルリサーチ分野(田口歩分野長)の梶野泰祐主任研究員と高橋隆総長らの研究グループは、名古屋大学(島村徹平教授)、東京大学医科学研究所(宮野悟教授)らとの共同研究により、肺がん細胞の増殖に極めて重要な、タンパク質に翻訳されないRNA(ノンコーディングRNA)を発見しました。肺がん細胞の生存や増殖には、キナーゼ1)や転写因子2)などのタンパク質による制御が重要と考えられています。一方、ヒトゲノムには数万種類もの比較的長い長鎖ノンコーディングRNA3)が存在することが分かってきたものの、その機能の詳細はほとんど未解明なままです。肺がんでMYCの異常が報じられてから30数年経ちますが、この度の研究チームの発見は、スーパーコンピュータ「京」を用いて肺がんの腫瘍組織における遺伝子の発現情報を解析し、代表的ながん遺伝子のMYCの発現制御を通じて肺がん細胞の増殖を維持する長鎖ノンコーディングRNA(MYMLRと命名)を発見したものです(図)。MYMLRを抑制することによって、MYCの発現を著しく低下させて肺がん細胞の増殖を抑制できます。したがって、本研究の成果は、代表的な難治がんの肺がんにも有効な、MYMLRを標的とした新たな治療法の開発に道を拓くものと期待されます。
本研究の詳細は、2019年7月30日付で、欧州分子生物学機構(EMBO)の機関誌「The EMBO Journal」に、オンライン速報版が掲載される予定です。
研究の背景
肺がんは、我が国におけるがん死亡原因の第1位であり、一部の肺がん患者には変異型の上皮成長因子受容体EGFRに対する分子標的薬や免疫チェックポイント阻害薬などの新しい治療の有効性が示されてはいますが、依然として年間に7万人以上が亡くなっている代表的な難治がんです。近年のゲノム研究から、細胞内には数万種類とも言われるタンパク質に翻訳されずにRNAのままで機能する長鎖ノンコーディングRNAが発現しており、タンパク質と長鎖ノンコーディングRNAの間には、複雑な制御関係が存在することが最近分かってきました。この長鎖ノンコーディングRNAによる制御機構の破綻が、細胞のがん化に密接に関わる可能性が示唆されており、肺がんの発生・増悪に重要な役割を担う長鎖ノンコーディングRNAの発見が求められていました。
研究内容と成果
研究チームは、代表的ながん遺伝子であり、肺がん細胞の増殖に必須な転写因子であるMYCに着目し、MYCを制御する長鎖ノンコーディングRNAを探索しました。スーパーコンピュータ「京」を用いて肺がん患者の腫瘍組織における遺伝子の発現情報を解析し、MYCを制御する新規長鎖ノンコーディングRNA“MYMLR”を発見しました。肺がん細胞株を用いてMYMLRの機能について調べたところ、MYMLRはMYCの発現維持に必要であり、肺がん細胞の増殖において重要な働きを持つことがわかりました。このMYMLRによるMYCの制御機構を詳細に解明するために、MYMLRと協調して働くタンパク質を探索し、MYMLRと結合するタンパク質としてPCBP2を同定しました。さらにMYMLRはPCBP2と結合してMYC遺伝子近傍のゲノムDNAを湾曲させ、遺伝子の発現制御を担うエンハンサー4)をプロモーター5)に近接させることによりMYCの転写を制御していることを解明しました。
今後の展望
細胞の増殖制御は、キナーゼや転写因子によって適切に制御されており、その破綻が細胞のがん化に繋がると考えられています。一方で、ゲノム上に数万種類が存在すると考えられてきながらも、長鎖ノンコーディングRNAの機能はほとんど未解明でした。今回、長鎖ノンコーディングRNAの一つであるMYMLRの肺がん細胞の増殖における重要性とその機能の詳細が明らかとなったことによって、MYMLRを標的とする革新的な治療法の開発が進むものと期待されます。また、スーパーコンピュータを駆使したシステム生物学的手法6)による探索を通じて、長鎖ノンコーディングRNAとタンパク質の制御関係に迫れることを示した本研究は、数万種類もの長鎖ノンコーディングRNAの機能の解明に道を拓きました。
研究支援
本研究は文部科学省科学研究費補助金 新学術領域研究・システム癌新次元「肺がんの分子病態をノンコーディングRNAから俯瞰するシステム的統合研究」(研究代表者:高橋隆、15H05910)、若手研究(B)「新規ノンコーディングRNA、MYMLRによるMYCの制御機構の解明」(研究代表者:梶野泰祐、16K19050)、および国立研究開発法人日本医療研究開発機構(AMED)革新的がん医療実用化研究事業「MYCを制御し肺がんの生存・増殖を担うMYMLR lncRNAの機能解明と革新的分子標的薬の開発」(研究開発代表者:梶野泰祐、18ck0106363h9902)の一環として行われました。
用語解説
- 1)キナーゼ
- ATP活性によって標的の遺伝子をリン酸化するタンパク質。上皮成長因子受容体EGFRなどのキナーゼに変異が導入されると正常細胞ががん化する。
- 2)転写因子
- ゲノムDNAと結合し、標的遺伝子の転写を制御するタンパク質。
- 3)長鎖ノンコーディングRNA
- ゲノムDNAより転写されるが、タンパク質に翻訳されないRNAのうち、200塩基以上の長さを持つもの。タンパク質やゲノムDNAなどと結合して機能するとされるが、ほとんどが機能未解明。
- 4)エンハンサー
- 遺伝子の発現の開始と発現量の制御に関わるプロモーターに働きかけて、遺伝子の発現を調節するゲノム領域。
- 5)プロモーター
- 遺伝子の上流に位置し、転写因子などが結合することにより、下流の遺伝子の発現を制御するゲノム領域。
- 6)システム生物学的手法
- 生物学に数理計算モデルや統計学的手法を導入し,生命現象を遺伝子やタンパク質が構成するシステムとして俯瞰的に理解する手法。
掲載論文
- タイトル
- Divergent lncRNA MYMLR regulates MYC by eliciting DNA looping and promoter-enhancer interaction
- 著者
- Taisuke Kajino, Teppei Shimamura, Shuyi Gong, Kiyoshi Yanagisawa, Lisa Ida, Masahiro Nakatochi, Sebastian Griesing, Yukako Shimada, Keiko Kano, Motoshi Suzuki, Satoru Miyano and Takashi Takahashi*
*Corresponding author - 掲載誌
- The EMBO Journal(欧州分子生物学機構【EMBO】の機関誌)
- DOI
- 10.15252/embj.201798441
お問い合わせ先
研究に関すること
愛知県がんセンター
総長 高橋 隆(たかはし たかし)
〒464-8681 名古屋市千種区鹿子殿1-1
TEL:052-762-6111(内線)7001
E-mail:tak“AT”aichi-cc.jp
広報に関すること
愛知県がんセンター運用部経営戦略室
川津、鈴木
TEL:052-762-6111(内線2511)FAX:052-764-2963
E-mail:kosuzuki“AT”aichi-cc.jp
AMED事業に関すること
国立研究開発法人日本医療研究開発機構(AMED)
戦略推進部 がん研究課
TEL:03-6870-2221
E-mail:cancer“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
関連リンク
掲載日 令和元年7月30日
最終更新日 令和元年7月30日


