ゲノム編集を用いた革新的な遺伝子治療による視覚再建―遺伝子変異を正常化する遺伝子治療の実現へ―
プレスリリース
国立大学法人東北大学大学院医学系研究科
国立研究開発法人日本医療研究開発機構
発表のポイント
- 病気の原因となる遺伝子変異を正常配列に置換するための、ゲノム編集注1による遺伝子治療注2で用いるアデノ随伴ウイルス(AAV)注3の単一化に成功した。
- この技術を用いることにより、従来の方法の約2~5倍の効率でゲノム編集を実現し、ゲノム編集が起こりにくく、これまで治療例がなかった成体マウス神経細胞の遺伝子変異の正常化が可能になった。
- この技術を用いた遺伝子治療の結果、全盲の網膜変性マウスにおいて正常の6割程度の視力を回復し、同治療の実用性を実証した。
研究概要
東北大学大学院医学系研究科の視覚先端医療学の西口 康二(にしぐち こうじ)准教授と眼科学分野の中澤 徹(なかざわ とおる)教授らのグループは、新しい遺伝子治療の方法を開発し、全盲の網膜変性マウスにおいて正常の6割程度の視力回復を実現しました。
現在、ゲノム編集を用いた遺伝子治療として、主に病気の原因となる遺伝子を「破壊」することにより病気を治療する方法での臨床応用の研究が進んでいます。それに対して、病気の原因となる遺伝子を「正常化」するゲノム編集を用いた遺伝子治療は技術的に難易度が高く、臨床への実用化が難しい状況でした。しかし、遺伝子を「正常化」する遺伝子治療は、実用化されると極めて汎用性が高い「究極」の遺伝子治療です。本研究は、遺伝子変異の「正常化」を可能にするゲノム編集を用いた遺伝子治療(変異置換ゲノム編集治療)の単一ウイルス化に成功しました。この治療法を網膜変性疾患のマウスに応用し、実用化可能なレベルの治療効果を実証しました。本研究の成果により、これまで治療が不可能であった多くの遺伝性疾患が治療できる可能性があります。
本研究成果は、2020年1月24日午前10時(英国時間、日本時間1月24日午後7時)Nature Communications誌(電子版)に掲載されます。
研究内容
国の指定難病である網膜色素変性注4は有効な治療法がない遺伝性疾患で、本邦の失明原因の第2位の疾患です。近年、重症型の網膜色素変性の治療として、アデノ随伴ウイルス(AAV)を使って正常な遺伝子全体を病気の細胞に補充する遺伝子治療(遺伝子補充療法)が有効であると示されました。しかし、一度に導入できる遺伝子の大きさには制約があるため、一部の網膜色素変性患者に対してのみ効果がある治療法でした。一方、ゲノム編集を用いた遺伝子治療(ゲノム編集遺伝子治療)では、病気の原因となる変異部分だけを「正常化」することができ、多くの網膜色素変性患者を治療できる可能性があります(図1A)。しかし、従来のゲノム編集遺伝子治療は、病気の細胞に対して、複数のウイルスを用いて異なる遺伝子を同時に導入する必要があるため、遺伝子改変の効率が悪く、実用化の目途はたっていませんでした。
本研究において、西口康二准教授と中澤徹教授らの研究グループは、これまで複数のAAVで行われていたゲノム編集を、一つのAAVで行うことができる革新的な遺伝子治療技術を確立しました。この遺伝子治療技術をゲノム編集が難しいとされる神経疾患のモデルマウスに適用した結果、ゲノム編集効率の大幅な改善と、高い治療効果を実現しました。この新規の遺伝子治療技術では、ゲノム編集に必要な構成要素の小型化を行うことで、これまでの2つのAAVに分けていたゲノム編集に必要な構成要素を一つのAAVにまとめることができました(図1B)。特に、正常配列を挿入するゲノム修復機構にマイクロホモロジー媒介末端結合(MMEJ)注5を利用したことで、正常配列を含む最小限のDNAで正確にゲノムを修復することができました。このAAVを成体の全盲網膜変性のマウスに投与したところ、病因変異の約10%が正常化され、光感度が10,000倍改善し、視力が正常の約6割にまで回復しました(図2)。更に、従来の遺伝子補充療法と同等の治療効果を示したことから、新規治療法の実用性を実証しました。この成果は、これまで治療の対象にならなかった網膜色素変性だけでなく、多くの遺伝病性疾患に対する遺伝子治療の開発への道を開くものです。
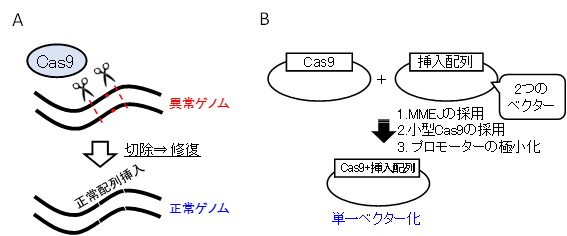
- 変異置換ゲノム編集治療ではCas9タンパクを用いて変異の両端のゲノムを切除し、同部位に正常配列を挿入します。
- 従来の変異置換ゲノム編集治療では、Cas9と挿入配列を2つのAAVベクターに分けて治療を行っていましたが、本研究では、小型のゲノム編集パーツを採用することにより、単一AAVベクター化に成功しました。
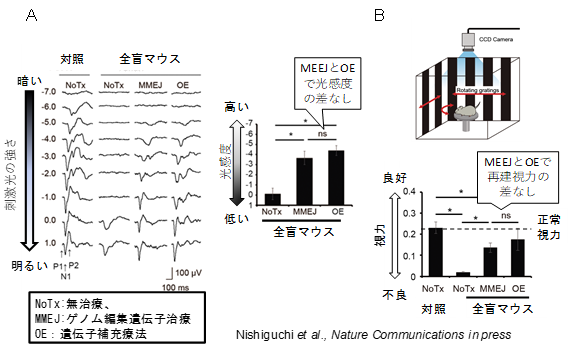
- 脳波による光感度測定。変異置換ゲノム編集後の眼(MMEJ)に対応する脳波では無治療眼(NoTx)のそれに比べての光感度が約10,000倍改善していた。この改善効果は、従来の遺伝子補充療法(OE)と同等であった。
- 一定速度で回転する縦じま模様に対する首振り反応観察による視力測定では、変異置換ゲノム編集後のマウス(MMEJ)と遺伝子補充治療後のマウス(OE)の測定視力の差はなかった。
本研究は、国立研究開発法人日本医療研究開発機構(AMED)難治性疾患実用化研究事業の支援を受けて行われました。中澤徹は東北大学大学院医学系研究科視覚先端医療学、眼科画像情報解析学、網膜疾患制御学の教授も併任しています。
用語説明
- 注1 ゲノム編集:
- Cas9というDNA切断酵素と人工的にデザインしたRNAなどを細胞に導入し、ゲノム局所を選択的に改変する手法。
- 注2 遺伝子治療:
- 細胞内に核酸(DNAやRNA)を導入する治療法。
- 注3 アデノ随伴ウイルス:
- 哺乳類の細胞に感染するウイルス。非病原性ウイルスであるため、遺伝子治療に利用されている。神経系細胞などに高い効率で安定的に遺伝子を導入できるため、遺伝子治療の標準的な担体になりつつある。
- 注4 網膜色素変性:
- 遺伝性の指定難病であり、失明原因2位の疾患。夜盲と視野異常で発症し、徐々に視機能が低下する。有病率は約3,000人に1人。
- 注5 マイクロホモロジー媒介末端結合:
- Cas9により切断された異常配列(変異)に対して、正常子配列の両端に約20塩基対の相同配列を配置することにより同配列を異常配列のかわりにゲノムに挿入する方法。正確なゲノム編集を可能にする。
論文題目
- Title:
- Single AAV-mediated mutation replacement genome editing in limited number of photoreceptors restores vision in mice
- Authors:
- Koji M Nishiguchi, Kosuke Fujita, Fuyuki Miya, Shota Katayama, Toru Nakazawa
- 論文題目:
- 「少数の視細胞に対する単一AAVによる変異置換ゲノム編集によるマウスの視覚再建」
- 著者名:
- 西口康二、藤田浩輔、宮冬樹、片山翔太、中澤徹
- 雑誌名:
- Nature Communications
- DOI:
- 10.1038/s41467-019-14181-3
お問い合わせ先
研究に関すること
東北大学大学院医学系研究科
視覚先端医療学
準教授 西口 康二(にしぐち こうじ)
Eメール:nishiguchi"AT"oph.med.tohoku.ac.jp
取材に関すること
東北大学大学院医学系研究科・医学部広報室
電話番号:022-717-7891
FAX番号:022-717-8187
Eメール:pr-office"AT"med.tohoku.ac.jp
AMED事業に関すること
国立研究開発法人日本医療研究開発機構(AMED)
戦略推進部 難病研究課
電話番号:03-6870-2223
Eメール:nambyo-info"AT"amed.go.jp
※Eメールは上記アドレス“AT”の部分を@に変えてください。
関連リンク
掲載日 令和2年1月27日
最終更新日 令和2年1月27日


