「難治性重症心不全患者を対象とした同種iPS細胞由来再生心筋球移植の安全性試験」の臨床研究について
プレスリリース
慶應義塾大学医学部
慶應義塾大学病院
日本医療研究開発機構
慶應義塾大学医学部内科学(循環器)教室の福田恵一教授らが計画中の「難治性重症心不全患者(注1)を対象とした同種iPS細胞由来再生心筋球(注2)移植の安全性試験」の臨床研究について、同研究の内容を定めた第1種再生医療等提供計画が、慶應義塾特定認定再生医療等委員会により、再生医療等の安全性の確保等に関する法律(平成25年法律第85号)および同法施行規則(厚生労働省令第110号)に規定する再生医療等提供基準に適合している旨の判定を2月5日付で受けました。
今後、慶應義塾大学医学部および慶應義塾大学病院では、この新たな治療法の実現を目指す臨床研究の実施に向けて、再生医療等の安全性の確保に関する法律および同法施行規則の規定に基づき、厚生労働大臣へ本提供計画を提出するなど、必要な手続きを遅滞なく進めていきます。
研究の背景と研究計画の概要
- 〔研究課題名〕難治性重症心不全患者を対象とした同種iPS細胞由来再生心筋球移植の安全性試験
- 〔実施責任者〕慶應義塾大学医学部教授 福田恵一(内科学(循環器)教室)
研究の背景
心不全は、心筋梗塞や心筋炎等のさまざまな理由により心筋細胞が失われ、心臓の収縮機能が低下する病態です。国内には100万人以上の心不全の患者さんがおり、このうち10万人以上が難治性重症心不全の患者さんです。これまで難治性重症心不全の治療としては心臓移植がなされていますが、ドナー不足のため年間50例程度しか実施することができず、これ以外には有効な治療法はありませんでした。しかし、福田教授らによるこれまでの研究により、再生心筋細胞をこれらの患者さんの心臓に移植すれば、難治性重症心不全に対する有効な治療になる可能性があることが分かってきました。また近年、山中伸弥教授(京都大学)らにより開発された人工多能性幹細胞(iPS細胞)に、福田教授らが開発した高効率で均質な心筋細胞へ分化誘導する技術を適用することにより、難治性重症心不全に対する移植治療に必要な再生心筋細胞を、迅速かつ大量に作製することができるようになってきました。すなわち、あらかじめiPS細胞から十分な移植用の再生心筋細胞を用意しておくことにより、速やかに、これを難治性重症心不全の患者さんの心臓に移植することが可能になります。
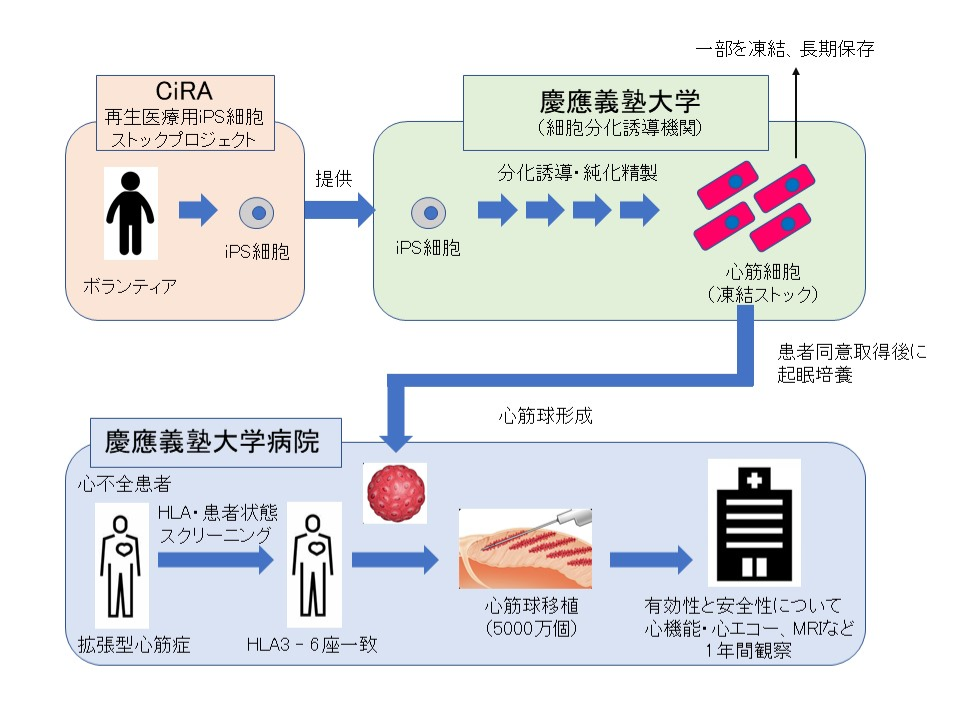
本臨床研究は、京都大学iPS細胞研究所(CiRA)が構築している再生医療用iPS細胞ストックプロジェクトから、医療用iPS細胞の提供を受け、あらかじめ移植用の再生心筋細胞を作製して用いる計画です(図1)。
また本臨床研究は、2017年度から2019年度まで、国立研究開発法人 日本医療研究開発機構(AMED)再生医療実用化研究事業の支援を受けています。
研究の概要
本臨床研究では、難治性重症心不全の患者さんを対象に、主要な目的としてiPS細胞から作製した移植用の再生心筋細胞および移植方法の安全性を、また副次的な目的としてそれらの難治性重症心不全治療における有効性を確認します。移植細胞は、あらかじめCiRAから提供を受けた医療用iPS細胞より、慶應義塾大学で移植用の再生心筋細胞を作製し、凍結ストックとして保存しておきます。
研究計画に定められた基準を満たす難治性重症心不全の患者さんから、本臨床研究への参加に関する同意が得られた場合、凍結保存済みの移植用の再生心筋細胞を解凍して移植用に最終調製し、心臓の左心室の壁内へ移植します。
移植後は、一定期間の免疫抑制剤の使用、および通常の保険診療の範囲内のリハビリテーション治療などを行い、約1年間の経過観察を詳しく行う計画です。
本臨床研究についてご理解いただききたいこと
本臨床研究は、難治性重症心不全に対する再生心筋細胞の移植という、従来にない、世界で初めての治療法に関する最初の臨床研究であるため、国内に10万人以上いる難治性重症心不全の患者さんの中で、特に「拡張型心筋症」という、非常に限られた患者さんを対象として慎重に行います。
また、研究に参加される患者さんの安全性を最優先するため、移植する心筋細胞は、本研究チームが本臨床研究の準備段階で行った検討(非臨床試験)で安全性を確認できた最小限の細胞数(患者さん1人当たり5000万個)とする計画です。
そのため、研究の対象となった患者さんに治療上の有効性が認められる可能性はありますが、今回の臨床研究における主要な目的は、移植した再生心筋細胞および移植方法の安全性を確認することです。
本臨床研究で安全性が確認できた場合、将来的な計画として、移植する細胞数を増やすことによる有効性の検討や、「拡張型心筋症」だけでなく、虚血性心疾患(注3)など他の原因に起因する種々の心不全における安全性や有効性の検討を行いたいと考えています。
今後の手続きについて
慶應義塾大学医学部および慶應義塾大学病院では、今後、本臨床研究の実施に向けて、遅滞なく必要な手続きを進める予定です。
本臨床研究は、再生医療等の安全性の確保等に関する法律および同法施行規則に規定される「第1種再生医療等技術」を用いて行われるものです。「第1種再生医療等提供計画」として特定認定再生医療等委員会(慶應義塾特定認定再生医療等委員会)へ申請され、同委員会における審議を経て、このたび再生医療等の安全性の確保等に関する法律および同法施行規則に規定する「再生医療等提供基準」に適合している旨の判定を受けました。
これを受けて慶應義塾大学病院は、院内の所定の手続きを経て、本提供計画の実施を厚生労働大臣へ申請する予定です。
本提供計画は、提出後90日の間(延長される場合があります)、再生医療等提供基準への適合性について確認を受け、その結果、計画の変更その他の必要な措置をとるべきことを命じられる場合があります。また提供基準への適合性が確認された場合、その旨の通知を受け、本臨床研究を開始することが可能になります。
用語解説
- (注1) 難治性重症心不全患者:
- 心不全の症状改善のために通常使用される内服薬やペースメーカー、心臓再同期療法を使用しても、充分な効果が上げられず臨床症状の改善がみられない患者。補助人工心臓や心臓移植が必要とされることが多い。
- (注2) 心筋球:
- iPS細胞由来の再生心筋細胞を純化精製し、球状の形態にしたもの。約1000個の心筋細胞を使用して作製する。心室壁内に移植した際には、高い生着率を保つことができる。
- (注3) 虚血性心疾患:
- 動脈硬化等により冠動脈が狭窄し、狭心症あるいは心筋梗塞を生じた状態。心筋梗塞を発生した際には心不全を合併することが多い。
お問い合わせ
本リリースの発信元
慶應義塾大学
信濃町キャンパス総務課:山崎・小川
〒160-8582 東京都新宿区信濃町35
TEL:03-5363-3611 FAX:03-5363-3612
E-mail:med-koho“AT”adst.keio.ac.jp
慶應義塾大学医学部・医学研究科
AMED再生医療実用化研究事業に関するお問い合わせ
国立研究開発法人日本医療研究開発機構(AMED)
戦略推進部 再生医療研究課
TEL:03-6870-2220 FAX:03-6870-2242
E-mail:saisei3“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
関連リンク
掲載日 令和2年2月6日
最終更新日 令和2年2月6日


