妊娠中の食物繊維摂取は胎児の代謝機能の発達を促し、出生後、子の肥満になりにくい体質をつくる
プレスリリース
国立大学法人 東京農工大学
学校法人慶應義塾 慶應義塾大学薬学部
国立研究開発法人 日本医療研究開発機構
国立大学法人東京農工大学大学院農学研究院応用生命化学部門の木村郁夫教授らと慶應義塾大学薬学部の長谷耕二教授らの研究グループは、妊娠中の母親の腸内細菌が産生する短鎖脂肪酸が胎児の発達に影響を与えることによって、出生後の子の代謝機能の成熟に関与し、その結果、肥満発症の抑制に繋がることを明らかにしました。周産期における母体の食生活や腸内環境の改善など、母体の栄養管理を介した先制医療や予防医学による新たな治療法の確立に向けて、今後、本成果の応用が期待されます。
本研究成果は、米国科学誌「Science」(2月28日付)に掲載されます。
- 論文タイトル:
- Maternal gut microbiota in pregnancy influences offspring metabolic phenotype in mice(妊娠中の母親の腸内細菌叢は子孫のエネルギー代謝機能に影響を与える)
- DOI:
- 10.1126/science.aaw8429
- URL:
- https://science.sciencemag.org/
現状
近年の抗生物質の使用拡大や、欧米食に代表される高糖質・高脂肪な高カロリー食、食物繊維の摂取不足のような食生活の変化は、腸内細菌叢に異常をきたし、その結果、肥満や糖尿病に代表される生活習慣病を含むさまざまな病気の罹患率を高めることが分かってきています。このように、成人の生活環境に対する腸内細菌叢の影響についてさまざまな報告がなされてきていますが、胎児期での腸内細菌叢の影響に関してはあまり知られていませんでした。また、将来の健康や特定の病気への罹りやすさは、胎児期や生後早期の環境の影響を強く受けて決定されるというDOHaD仮説(注1)に関しても、コホート研究(注2)等により、低出生体重児は成人期に糖尿病や高血圧、高脂血症などの生活習慣病を発症するリスクが高い等の報告がされてきましたが、その根底にあるメカニズムは未だ不明なままでした。そこで、本研究グループは、母体の腸内細菌叢が胎児の発達と出生後の疾患への感受性に及ぼす影響についてマウス実験により詳細な研究を行いました。
また、短鎖脂肪酸(注3)に代表される腸内細菌叢由来の代謝産物は、宿主のエネルギー源として利用されるだけではなく、シグナル伝達分子として脂肪酸受容体(注4)であるGPR41やGPR43のような宿主側の受容体を介して、宿主の生理機能にまで影響を及ぼします。我々は以前から、食由来成分や腸内細菌叢由来の代謝産物との相互作用を通じて、エネルギー代謝におけるこれら脂肪酸受容体の生物学的重要性を明らかにしてきました。
研究体制
本研究は、東京農工大学の木村郁夫教授(大学院農学研究院/グローバルイノベーション研究院)、宮本潤基特任助教(大学院農学研究院)、慶應義塾大学の長谷耕二教授(薬学部)らの研究グループと、京都大学、慶應義塾大学、東京農業大学、岡山大学、神戸大学との共同研究により実施されました。
研究成果
本研究グループは、始めに、妊娠マウスを通常環境下、および無菌環境(注5)下で飼育しました。分娩後は成長環境を同一にするために、両群の出生仔を通常環境下で仮親によって成育させました。離乳後、高脂肪食を摂取させたところ、 無菌母親マウスの仔は、成長に伴って重度の肥満になり、高血糖・高脂血症などのメタボリック症候群の症状を示しました(図1)。また、妊娠中に食物繊維をほとんど含まない餌を与えた母親マウスの仔でも、同様な症状が観察されました。一方で、食物繊維を豊富に含む餌を妊娠母親マウスに与えた場合には、生まれてきた仔マウスは肥満になりにくいことが分かりました。このとき、母体の腸内細菌によって食物繊維が分解されて、短鎖脂肪酸が多く産生されることで、その一部は血液を介して胎児に届けられていることが分かりました。
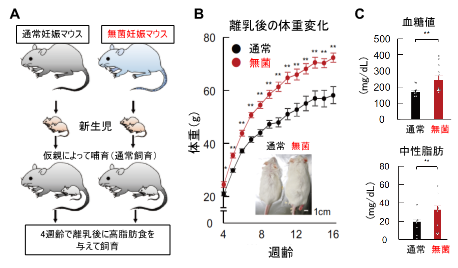
そこで、無菌飼育した妊娠マウスや低食物繊維の餌を与えた妊娠マウスの餌に、短鎖脂肪酸の1つであるプロピオン酸を補充したところ、生まれてきた仔マウスの肥満が抑制されました。このことから、妊娠中の母親の腸内細菌叢が産生する短鎖脂肪酸は、生まれてきた仔の肥満を予防することが分かりました。
興味深いことに、胎児の交感神経、腸管、膵臓には短鎖脂肪酸の受容体であるGPR41とGPR43が高発現していました。胎児は腸内細菌を持たないため、自分では短鎖脂肪酸を多く作ることはできません。よって、胎児組織のGPR41とGPR43は、母体の腸内から届けられた短鎖脂肪酸を感知していると考えられます。短鎖脂肪酸によって胎児のGPR41とGPR43が活性化すると、神経細胞、GLP-1(注6)陽性の腸内分泌細胞、膵β細胞(注7)の分化を促進することが分かりました。その結果として、生後の仔の代謝・内分泌系が正常に成熟し、成長時のエネルギー代謝を整えることで、肥満になりくい体質を作ることを明らかにしました。
今後の展開
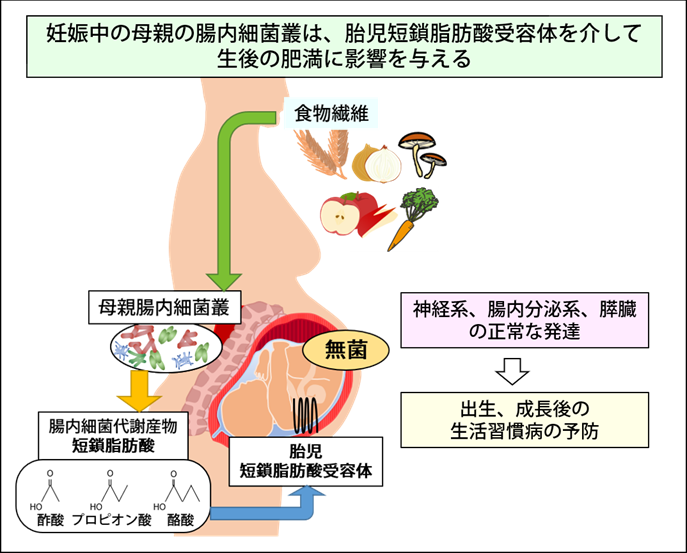
本研究により、妊娠中の母体の腸内細菌叢は、短鎖脂肪酸を産生することにより、胎児の短鎖脂肪酸受容体を介して、出生後、子の肥満に対する抵抗性を与えることを明らかにしました。これらの発見は、妊娠中の母体の腸内環境が、生活習慣病を防ぐために子孫の代謝プログラミング(注8)の決定に重要であることを示しています。したがって、今回の発見は、母体の腸内環境と子の生活習慣病というDOHaD仮説の新たな連関を提唱するものです。また、本研究の成果は、母体への食事介入や栄養管理を介した先制医療や予防医学、更には腸内代謝産物や、その生体側の受容体を標的とした新たな代謝性疾患の治療薬の開発に寄与する可能性が大いに期待されます。
用語解説
- (注1)DOHaD仮説:
- Developmental Origins of Health and Diseaseの略。胎児期や生後直後の健康・栄養状態が、成人になってからの健康に影響を及ぼすという概念のこと。
- (注2)コホート研究:
- 介入を行わず対象者の生活習慣や疾患などを一定期間に渡り調査・観察する「観察研究」の一つ。
- (注3)短鎖脂肪酸:
- 炭素数6以下の脂肪酸の総称。主に酢酸、プロピオン酸、酪酸がありエネルギー源や脂肪合成の基質として使用される。最近では、受容体を介したシグナル分子としての作用やエピジェネティック(DNAの配列変化によらず遺伝子発現を制御するシステム)な作用なども報告されている。
- (注4)脂肪酸受容体:
- GPCR(G蛋白質共役型受容体:G-protein coupled receptor)群の一つ。脂肪酸をリガンドとする細胞膜を7回貫通する細胞膜上受容体の一つであり、三量体のGタンパク質を介して細胞内にシグナルを伝達する。短鎖脂肪酸受容体(GPR41やGPR43)、中鎖脂肪酸受容体(GPR84)、長鎖脂肪酸受容体(GPR40やGPR120)が知られている。
- (注5)無菌環境:
- 空気中の細菌や宿主の共生細菌が存在しない環境のこと。
- (注6)GLP-1:
- Glucagon like peptide-1の略。腸内分泌細胞のL細胞から分泌される腸管ホルモンの一種であり、摂食調節やインスリン分泌の促進に関与する。
- (注7)膵β細胞:
- 膵臓のランゲルハンス島(島状に散在して内分泌を営む細胞群)内に局在するインスリン分泌細胞のこと。グルコース濃度に応じてインスリン分泌を促す。
- (注8)代謝プログラミング:
- 胎児期や生後早期などの臓器形成・成熟の感受性が高い時期における栄養環境などにより、代謝システムの形成に影響を及ぼすこと。
本研究は、国立研究開発法人日本医療研究開発機構(AMED)の革新的先端研究開発支援事業AMED-CREST「微生物叢と宿主の相互作用・共生の理解と、それに基づく疾患発症のメカニズム解明」領域(研究開発総括:笹川千尋)における研究開発課題「腸内代謝物に基づく宿主エネルギー恒常性維持への腸内細菌叢関与の解明と生活習慣病予防・治療基盤の確立」(研究開発代表者:木村郁夫)の一環で行われました。
お問い合わせ
研究に関する問い合わせ
東京農工大学大学院農学研究院
応用生命化学部門 教授
木村 郁夫(きむら いくお)
TEL/FAX:042-367-5748
E-mail:ikimura“AT”cc.tuat.ac.jp
東京農工大学大学院 農学研究院 応用生命化学専攻 代謝機能制御学研究室
慶應義塾大学薬学部
生化学講座 教授
長谷 耕二(はせ こうじ)
TEL:03-5400-2484
E-mail:hase-kj“AT”pha.keio.ac.jp
事業に関する問い合わせ
国立研究開発法人日本医療研究開発機構(AMED)
基盤研究事業部 研究企画課
TEL:03-6870-2224 FAX:03-6870-2246
E-mail:kenkyuk-ask“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
掲載日 令和2年2月28日
最終更新日 令和2年2月28日


