健診データから分かったパーキンソン病の早期変化
プレスリリース
名古屋大学
日本医療研究開発機構
名古屋大学大学院医学系研究科神経内科学の勝野雅央教授、横井克典(筆頭研究者、大学院生)の研究グループは、難治神経変性疾患※1のひとつであるパーキンソン病※2を対象とした臨床研究において、患者さんが過去に受診した健康診断の結果を解析することで、運動症状の発現前に血圧、ヘマトクリット※3、血清コレステロールの値が変化することを見出しました。
パーキンソン病はドーパミン神経※4の細胞死を原因とする進行性の神経変性疾患であり、手のふるえや動作緩慢などの運動症状が主症状ですが、運動症状の発現時にはすでに50%以上のドーパミン神経が死滅していることがわかっており、早期診断・治療が重要と考えられるようになってきています。この研究の目的は、パーキンソン病の運動症状発現前の体内の変化を、健康診断の結果から解明することです。
勝野教授らの研究チームは、久美愛厚生病院(岐阜県高山市)と名古屋大学医学部付属病院(愛知県名古屋市)に通院中の45人のパーキンソン病患者が運動症状発現前から受けていた健康診断結果の経時的変化を解析しました。同時に、だいどうクリニック(愛知県名古屋市)の健康診断を受診した120人の健康な方のデータについても経時的変化を解析しました。
その結果、女性のパーキンソン病患者では運動症状発現前に血圧が上昇しており、発症が近づくにつれて血圧が低下してくることがわかりました。男性のパーキンソン病患者ではヘマトクリット値、総コレステロール、低密度リポタンパク質コレステロール(LDL-コレステロール)※5が運動症状発現前から低下してくることが明らかになりました。
本研究の結果から、健康診断の項目のうち、血圧、ヘマトクリット値、血清コレステロール値がパーキンソン病の運動症状発現前のバイオマーカー※6となる可能性が示唆されました。さらにこれらの結果は、パーキンソン病の運動症状発現前に、すでに自律神経機能や貧血、代謝などに関する生体変化が始まっていることを示しているものと考えられます。
本研究成果は、英国科学雑誌「Scientific Reports」(2020年11月25日付の電子版)に掲載されます。
ポイント
- パーキンソン病はドーパミン神経の細胞死を原因とする神経変性疾患であり、その主な症状は振戦(手のふるえ)、筋強剛(筋肉や関節がかたくなる)、無動(動作が遅く、小さくなる)、姿勢反射障害(転びやすい)などの運動症状である。
- パーキンソン病の運動症状の発現時には、すでに半数以上のドーパミン神経が細胞死に陥っていることが知られており、運動症状が発現する前からドーパミン神経の変性が始まっていることが明らかとなっている。
- 近年、パーキンソン病患者は運動症状の発現10~20年前から便秘やREM期睡眠行動異常症(RBD)※7、嗅覚低下などの非運動症状を呈することが分かっており、運動症状発現前の早期変化として注目されている。
- 本研究において女性のパーキンソン病患者では運動症状発現前の血圧が上昇し、男性の患者ではヘマトクリット値、総コレステロール、低密度リポタンパク質コレステロール(LDL-コレステロール)が運動症状発現前から低下することが明らかになった。
- 本研究により、運動症状発現以前に、これまで知られてきた非運動症状以外にも自律神経機能や貧血、代謝などに関する生体変化が始まっていることが明らかになった。
- 一般的に行われている簡便な健康診断の項目の中から、パーキンソン病の早期診断に役立つバイオマーカーの候補を明らかにすることができた。
背景
パーキンソン病は、神経変性疾患の中でアルツハイマー病に次いで2番目に患者の多い疾患です。罹患の頻度は比較的高く、我が国の患者数は15~20万人(65歳以上の100人に1人)といわれています。その原因は脳内のドーパミン神経の死滅です。パーキンソン病の主な症状は振戦(手のふるえ)、筋強剛(筋肉や関節がかたくなる)、無動(動作が遅く、小さくなる)、姿勢反射障害(転びやすい)などの運動症状ですが、認知機能障害、幻視、便秘、レム睡眠行動障害(RBD)、嗅覚低下、うつ病などの非運動症状もみられることが知られています。運動症状の発現時には、すでに50%以上のドーパミン神経が死滅していることが知られています。また、非運動症状のうち、便秘、レム睡眠行動障害(RBD)、嗅覚低下、うつ病は、運動症状が発現する10~20年前から現れます。これらのことから、パーキンソン病にかかわる生体変化は、運動症状の発現よりかなり前から始まっていると考えられています。
症状の発現前に神経細胞が死滅しているという現象は、パーキンソン病に限らず、多くの神経変性疾患に共通する現象です。例えば、アルツハイマー病でも主症状である認知症が発現する20年以上前からアミロイドβという異常な蛋白質が脳内にたまることが知られており、認知症の発症前に診断・治療を開始する試みが進められています。こうした試みを実用化するためには、症状が発現しないうちに脳や体の状態を見極めるための生体指標(バイオマーカー)が必要です。
しかし、パーキンソン病の運動症状発現前のバイオマーカーの連続した変化についてはほとんど知られていません。本研究は、パーキンソン病患者が過去に受診した健康診断の結果の経時的変化を解析することで、運動症状の発現前に体内で始まっている変化をとらえることで、早期診断のためのバイオマーカー開発につなげようとして計画されました。
研究成果
本研究では、運動症状発現前の健診結果を持っていた45人のパーキンソン病患者(男性22人と女性23人)、4年以上の健診の受診歴を持ち、神経疾患の既往やパーキンソン病の家族歴、パーキンソン病の非運動症状を持たない120人の健常者(健康な方、男性60人と女性60人)の健康診断結果を分析しました。
まず、パーキンソン病患者群と健常者群の各項目のベースライン値(パーキンソン病患者では運動症状が発現した年、健常者では最終の健診を受けた年)を性別ごとに比較しました。その結果、男性では、体重、肥満度指数(BMI)、ヘマトクリット(Ht)、総コレステロール(T-Cho)、低密度リポタンパク質コレステロール(LDL-Cho)、クレアチニン(Cr)において、両群の間に統計学的有意差があり、すべての項目でパーキンソン病患者群の方が低い値を認めました。女性では、収縮期血圧、拡張期血圧、アスパラギン酸アミノトランスフェラーゼ(AST)、T-Choでパーキンソン病患者群と健常者群の間に統計学的有意差が見られ、収縮期血圧、拡張期血圧、ASTの値は健常者に比べて女性患者で高かったのに対し、他の指標の値は女性患者で低値を認めました。
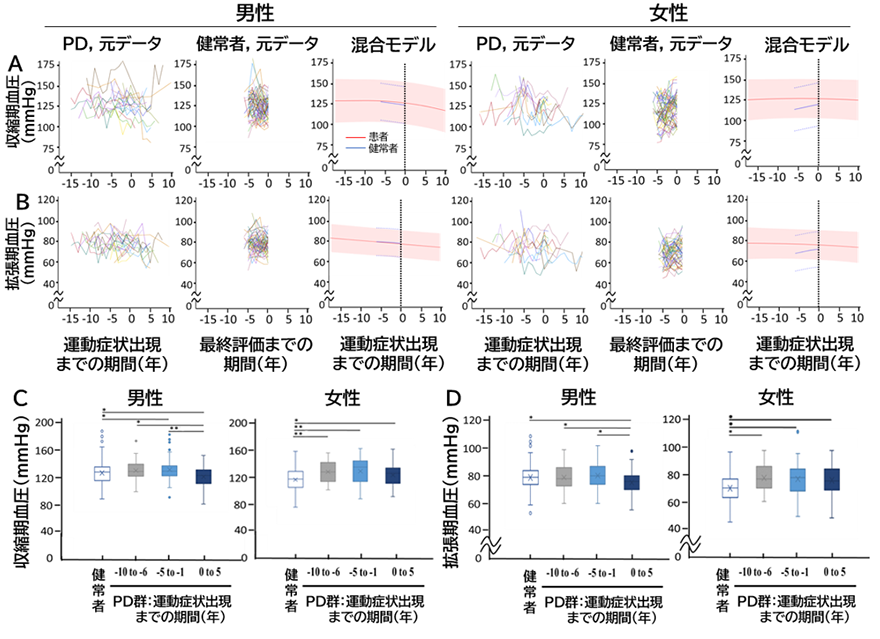
次に、パーキンソン病患者群の運動症状発現前の身体的変化を検索するために、身長、体重、BMI、収縮期血圧、拡張期血圧を男女それぞれで混合モデル※8で分析しました。その結果、収縮期および拡張期血圧の値は、女性患者では運動症状発現前に上昇し(図1の混合モデル上に記載される赤線)、運動症状の発現が近づくにつれて低下し、健常者に近づきましたが、これらの傾向は男性では認められませんでした(図1A、B)。混合モデル分析の結果を確認するために、各項目の実際のデータを発症前5年毎に区切って直接比較しました(図1C、D)。収縮期および拡張期血圧の上昇は、女性患者の運動症状発現の6年以上前に観察されましたが、混合モデルと同様に、健常者との差は徐々に小さくなりました。
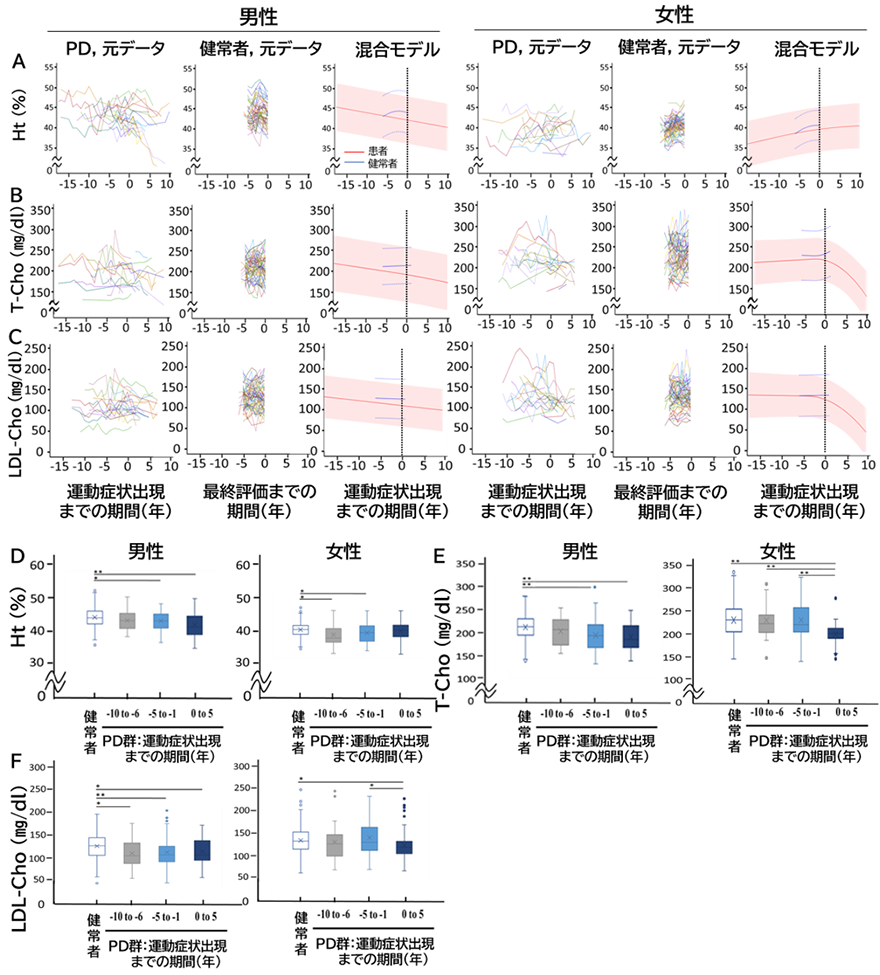
さらに、血液検査項目のうちベースラインでパーキンソン病患者群と健常者群とで統計的有意差を示したHt、AST、T-Cho、LDL-Cho、Crの項目についても、混合モデルを用いて解析を行いました。男性患者では、運動症状の発現前にヘマトクリット値が低下し始めました(図2A、混合モデルの赤線)。T-ChoおよびLDL-Cho値も、男性患者の運動症状の発現前に低下を認めました(図2B、C)。女性患者では、これらの値の運動症状発現前の変化は観察されませんでした。実際のデータを直接比較すると、男性患者のヘマトクリット値は、運動開始の5年前から1年前で健常者より低下していました(図2D)。男性患者の血清T-Choレベルは、運動症状発現の5~1年前に低下し始めましたが、女性患者では運動症状発現後にのみ値が低下しました(図2E)。血清LDL-Choレベルについても同様の結果が得られました(図2F)。
以前の研究において、男性ではコレステロールの値が高いとパーキンソン病を発症するリスクが減ること、および女性では血圧が高いとパーキンソン病を発症するリスクが増えることが報告されており、本研究の結果と合致していました。また、男女を問わず貧血があるとパーキンソン病を発症するリスクが増えることも報告されており、本研究における男性患者の健診結果と合致しましたが、女性でそのような変化が見られなかったことについては、今後さらなる解析が必要と考えられます。
今後の展開
本研究の結果、女性のパーキンソン病患者では運動症状発現前に血圧が高く、男性の患者では運動症状発現前からヘマトクリット値、T-Cho、LDL-Choが低下してくることが明らかになりました。これらの検査値を、非運動症状などに関する他の検査と組み合わせることで、将来的にパーキンソン病の早期診断(運動症状の発現前の早期発見)が可能になると考えられます。
現在、本研究チームは健康診断の受診者の中でパーキンソン病の非運動症状を有する方(ハイリスク者)の解析を並行して行っており、2021年1月からは薬剤を用いてパーキンソン病の発症を遅らせることを目的とした臨床試験を開始する予定です。
用語説明
- ※1 神経変性疾患
- 特定の種類の神経細胞が進行性に変性する(死滅する)疾患の総称。神経変性疾患に共通する病理学的な特徴として、神経細胞の中や周囲に異常な蛋白質が蓄積し、それによって特定の種類の神経細胞が障害されることが知られている。パーキンソン病、アルツハイマー病、筋萎縮性側索硬化症などが神経変性疾患の代表的疾患。
- ※2 パーキンソン病
- 神経細胞内にαシヌクレインという異常な蛋白質が蓄積し、主に脳内のドーパミン神経に障害を起こすことで、振戦(手足の震え)、筋強剛(筋肉や関節がかたくなる)、動作緩慢、姿勢反射障害(転びやすくなる)などの運動症状を引き起こす進行性の難病。
- ※3 ヘマトクリット
- 血液全体に対する赤血球の割合。血液の濃度を表す値であり、貧血時に低下する。
- ※4 ドーパミン神経
- ドーパミンを産生する神経細胞。
- ※5 低密度リポタンパク質コレステロール
- LDL-コレステロール。脂肪とタンパク質の比重が低いタンパク質でできたコレステロール。この値が高いと心筋梗塞、脳梗塞の発症にかかわるといわれている。
- ※6 バイオマーカー
- 体内で起きている変化を検査などで捉えるための指標。
- ※7 REM期睡眠行動異常症(RBD)
- 夜間に怖い夢を見て大声を出したり体をばたつかせる症状。RBDが発現すると、多くの方がその後にパーキンソン病などの神経変性疾患を発症することが知られており、パーキンソン病の前触れ症状として注目されている。
- ※8 混合モデル
- 複数名の経時的データから、集団全体における経時的変化を推定するための統計学的手法。
発表雑誌
- 掲雑誌名
- Scientific Reports(英国時間2020年11月25日付電子版)
- 論文タイトル
- Longitudinal analysis of premotor anthropometric and serological markers of Parkinson’s disease
- 著者
- Katsunori Yokoi, MD1, Makoto Hattori, MD1, Yuki Satake1, MD, Yasuhiro Tanaka, PhD1, Maki Sato1, Atsushi Hashizume, MD, PhD1, Akihiro Hori, MD, PhD2, Motoshi Kawashima, MD3, Akihiro Hirakawa, PhD4, Hirohisa Watanabe, MD, PhD5,6, Masahisa Katsuno, MD, PhD1
- 所属
-
- Department of Neurology, Nagoya University Graduate School of Medicine, Nagoya, 4668560, Japan
- Kumiai Kosei Hospital, Takayama, Gifu, 5068502, Japan
- Medical Examination Centre, Daido Clinic, Nagoya, 4578511, Japan
- Department of Biostatistics and Bioinformatics, Tokyo University Graduate School of Medicine, Tokyo, 1130033, Japan
- Brain & Mind Research Centre, Nagoya University Graduate School of Medicine, Nagoya, 4668560, Japan
- Department of Neurology, Fujita Medical University, Toyoake, Aichi, 4701192, Japan
- DOI
- 10.1038/s41598-020-77415-1
研究助成
本研究は、日本医療研究開発機構(AMED)認知症研究開発事業の助成などにより行われました。
お問い合わせ先
研究について
名古屋大学医学部・医学系研究科
神経内科学 教授 勝野雅央
TEL:052-744-2389 FAX:052-744-2384
E-mail:ka2no“AT”med.nagoya-u.ac.jp
広報担当
名古屋大学医学部・医学系研究科総務課総務係
TEL:052-744-2228 FAX:052-744-2785
E-mail:iga-sous“AT”adm.nagoya-u.ac.jp
AMED事業について
国立研究開発法人日本医療研究開発機構(AMED)
ゲノム・データ基盤事業部 医療技術研究開発課
TEL:03-6870-2221 FAX:03-6870-2244
E-mail:brain-d“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
関連リンク
掲載日 令和2年11月25日
最終更新日 令和2年11月25日


