血管により硬い歯がつくられる仕組みを解明―虫歯・歯周病により失われた歯の再生医療への応用に期待―
プレスリリース
慶應義塾大学医学部
日本医療研究開発機構
慶應義塾大学医学部解剖学教室の久保田義顕教授は、同生理学教室、同医化学教室、同内科学教室(循環器)、自治医科大学、長崎大学、滋賀医科大学、米国コネチカット大学との共同研究で、歯の血管の立体構造に関して新たなイメージング技術を開発し、歯が硬くなる過程において、血管が深くかかわっていることを明らかにしました。
歯は人体で最も硬い構造物で、特に食事においてその硬さが不可欠です。その硬い歯の中央部には歯髄(注1)というやわらかい組織があり、歯髄内の血管は、歯の健康維持に重要ですが、歯が硬くなる過程でもなんらかの役割があることが示唆されてきました。しかし、他のやわらかい組織とは違い、組織を細かく観察するために歯の「切片を切る」という作業が、その硬さゆえにほぼ不可能であったため、血管がどのように歯に入っていくか、そして血管がどのように歯の硬さに貢献しているかは不明でした。
本研究ではまず、歯の血管を可視化すべく従来の実験手法にさまざまな改良を加え、マウスの歯の切片をきれいに切ることに成功しました。そして、歯の血管の立体構造を単一細胞レベルで可視化する技術を確立することに成功しました。
この技術を用いて血管の走行を詳細に観察したところ、歯の硬化を担う象牙芽細胞(注2)の周辺にまとわりつき、象牙芽細胞の成熟を促すとともに、リンなどの硬化に必要な成分を供給しているユニークな血管細胞集団を見つけました。さらにその特定の血管細胞だけを除去するような遺伝子改変マウスを作成したところ、歯が硬くならないことを見出しました。
本研究は、世界で初めて、歯の高精度なイメージング技術を確立するとともに、その技術を用いて歯が硬くなるメカニズムを解明しました。将来的には、虫歯や歯周病などにより失われた歯の再生、特に硬い歯をつくるための技術への応用が期待されます。
本研究成果は2022年3月23日(米国東部時間)の『Journal of Experimental Medicine』オンライン版に掲載されました。
研究の背景
歯は骨よりさらに硬く、人体で最も硬い構造物です。歯は食事や会話において重要な役割を果たしますが、特に食事においてはその硬さが不可欠です。歯の中央部には歯髄というやわらかい組織があり、ここに血管や神経が通っており、歯の栄養補給、免疫、痛覚を担っています。特に深くまで進んだ虫歯(う蝕)の治療において、いわゆる「根の治療」を行いますが、これは歯髄の血管や神経を徹底的に取り除いてきれいにし、その部分に充填剤を流し込んで埋めるというものです。この歯髄の血管が歯の発生、特にもともと柔らかい幼弱な歯が硬くなる過程で、なんらかの役割を果たしていることは示唆されてきましたが、詳細は不明でした。
研究の概要と成果
本研究では、歯の血管を可視化すべく、従来骨で行われてきた脱灰や免疫染色の実験操作を改変した上で、その溶液の組成や時間にさまざまな試行錯誤を繰り返し、マウスの歯の「切片を切る」ことに成功しました。そして、歯の血管の立体構造を単一細胞レベルで可視化する技術を確立しました。この技術を用いて歯の血管の走行を詳細に観察した結果、象牙芽細胞の周辺にまとわりつき、血管の成長に必須であるVEGF(注3)の受容体を強く発現し、かつ周りに旺盛に突起を伸ばし、周囲の細胞と積極的にコンタクトしようとするユニークな血管細胞(図1)を見出しました。本研究グループは、これを傍象牙芽細胞先端様血管内皮細胞(periodontal tip-like endothelial cell : POTC)と名付けました。
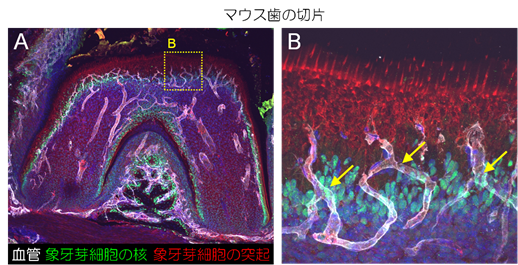
次に、シングルセルRNAシーケンシング(注4)によりPOTCの遺伝子発現プロファイルを解析したところ、他の血管内皮細胞とは異なる特徴的な遺伝子発現パターンが見られました。特に上記の旺盛に突起を伸ばす性質や、高いVEGF受容体の発現が裏付けられるとともに、象牙芽細胞を成熟させる因子や歯のミネラルの主成分であるカルシウムやリンのトランスポーター(輸送体)を強く発現していることを見出しました。これらの知見より、以降このPOTCにフォーカスし、さまざまな遺伝子改変マウスを用いて、POTCの機能を解析することにしました。
またVEGF受容体の遺伝子改変マウスの解析結果から、POTCは、他の血管に比べて可塑性(外界の変化に対応し、成長したり伸縮したりする能力)が高いこと、そして歯を硬化させる象牙芽細胞の能力を高めるような物質を放出していること、そしてリンなどの歯の硬化に必要な成分を象牙芽細胞に提供していることを見出しました。
一方、象牙芽細胞からはVEGFが供給され、POTCの受容体に結合することで成長を促している、つまりPOTCと象牙芽細胞は相互依存関係にあり、その相互作用が歯の硬化には必須であることを見出しました(図2)。
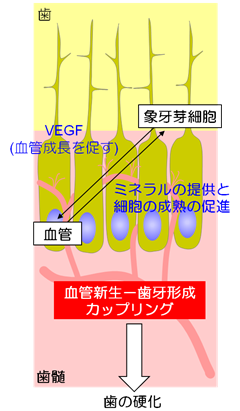
研究の意義・今後の展開
本研究では、世界で初めて、歯の組織の高精度イメージングを可能にしただけではなく、その技術を用いて、歯の硬化に重要な特定の血管細胞集団を同定し、血管による歯の硬化の詳細なメカニズムを解明しました。将来的には、本研究で見出された細胞メカニズム、網羅的に同定された血管由来の象牙芽細胞成熟因子などの解析をさらに進めることによって、虫歯・歯周病により失われた歯の再生への応用が期待されます。
特記事項
本研究は、日本医療研究開発機構(AMED) 革新的先端研究開発支援事業(PRIME)「生体組織の適応・修復機構の時空間的解析による生命現象の理解と医療技術シーズの創出」研究開発領域における研究開発課題「血管・リンパ管の独立性を担保する分子機構とその病態への応用」(研究開発代表者:久保田義顕)、科学技術振興機構ムーンショット型研究開発事業「神経グリア血管単位-リンパ管系に着目した血管性認知症および混合型認知症における臓器間ネットワークの解明とヒトへのトランスレーションによるリスク予見法の創出」の支援を受けました。
論文について
- 英文タイトル
- Coupling of angiogenesis and odontogenesis orchestrates tooth mineralization in mice
- タイトル和訳
- 血管新生と歯牙形成のカップリングは歯の硬化を制御する
- 著者名
- 松原智子、伊賀隆史、杉浦悠毅、楠本大、佐野坂司、田井育江、武田憲彦、Guo-Hua Fong、 伊藤公成、依馬正次、岡野栄之、神山淳、久保田義顕
- 掲載誌
- Journal of Experimental Medicine(オンライン版)
- DOI
- 10.1084/jem.20211789
用語解説
- (注1)歯髄
- 歯の中心に位置し、歯の硬い組織で囲まれた空洞(歯髄腔)にあるやわらかい組織。この中に神経や血管が多量に含まれ、痛みの発生や血流を通じて、歯の健康を保つための構造。
- (注2)象牙芽細胞
- 歯髄の最外層にある細胞。エナメル質と並んで、歯の硬い成分の一つである象牙質をつくり、これが石灰化することが、歯の硬化の過程の一つである。
- (注3)VEGF:血管内皮細胞成長因子(Vascular endothelial growth factor)
- 1989年、Napoleon Ferraraらによって発見されたタンパク質。強力な血管に対する増殖作用を有し、生体内における血管の発生、伸展に必須の分泌性タンパク質である。遺伝学的VEGFを欠損させたマウスでは体内に血管が全くつくられず、胎生初期に致死となる。
- (注4)シングルセルRNAシーケンシング
- 次世代シーケンサーを用いた最新の分子生物的手法。組織内の一個一個の細胞の遺伝子発現を網羅的に解析するで、個々の細胞の異なる生態や類似性を把握し、細胞亜集団の動態を包括的に理解することができる。
お問い合わせ先
本発表資料に関するお問い合わせ先
慶應義塾大学医学部 解剖学教室
久保田義顕(くぼた よしあき)教授
TEL:03-5315-4358 FAX:03-5315-4359 Email:ykubo33"AT"a3.keio.jp
慶應医学部・解剖学教室|久保田義顕
本リリースの配信元
慶應義塾大学 信濃町キャンパス総務課:山崎・飯塚・奈良
〒160-8582 東京都新宿区信濃町35
TEL:03-5363-3611 FAX:03-5363-3612 E-mail:med-koho”AT”adst.keio.ac.jp
慶應義塾大学医学部・医学研究科
AMED事業に関するお問い合わせ先
日本医療研究開発機構(AMED)
シーズ開発・研究基盤事業部 革新的先端研究開発課
革新的先端研究開発支援事業(PRIME)
TEL:03-6870-2224 FAX:03-6870-2246 E-mail:kenkyuk-ask”AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
関連リンク
掲載日 令和4年3月24日
最終更新日 令和4年3月24日


