抗体を非破壊的に高次構造評価する技術の確立に成功―独自のNMR技術により保存条件での高分子バイオ医薬の評価が可能に―
成果情報
次世代天然物化学技術研究組合
国立大学法人東京大学大学院薬学系研究科
国立研究開発法人産業技術総合研究所
中外製薬株式会社
国立研究開発法人日本医療研究開発機構
近年、創薬に用いられるモダリティが拡大し、抗体に代表されるバイオ医薬(注1)も大きな注目が集まっています。バイオ医薬が十分な薬効を安全に発揮するためには、その主成分である抗体などのタンパク質が、製剤組成中において適切な高次構造(HOS; higher order structure)(注2)を保つことが必要です。しかし、バイオ医薬のHOSは熱や不適切な溶液条件により劣化しやすい特徴を持ちます。バイオ医薬のHOSが劣化すると、薬効が失われるだけでなく、副作用が増強するおそれがあります。一方、これまでの分析技術では、測定自体がバイオ医薬のHOSに影響を与えてしまう恐れがありました。そのため、製剤組成そのままに、バイオ医薬のHOS情報を非破壊的に取得する技術が求められてきました。
東京大学大学院薬学系研究科および次世代天然物化学技術研究組合の嶋田一夫教授、産業技術総合研究所細胞分子工学研究部門の竹内恒研究グループ長と徳永裕二研究員、中外製薬株式会社の奥出順也博士、小里一友博士、および鳥澤拓也博士のグループは、独自の核磁気共鳴(NMR)(注3)技術:N-CRINEPT法(15N-detected cross-correlated relaxation and insensitive nuclei enhanced by polarization transfer、窒素15直接観測と交差緩和による低感度核の感度増強法)(注4)を開発することで、抗体のHOS情報を、製剤溶液条件下で低温保存温度において、非破壊的に取得することに成功しました。N-CRINEPT法により、糖鎖などの修飾や溶液条件の違いによるHOS変化が検出できるため、バイオ医薬の生産、製剤化、保存、輸送の様々な局面での活用が期待されます。また、N-CRINEPT法は高分子量タンパク質に対して広く適用できることから、中分子などが標的とする難標的タンパク質-タンパク質相互作用の立体構造解析など、バイオ医薬に限らず、様々なモダリティへの展開が期待されます。
研究開発のポイント
- 困難であった低温保存条件でのバイオ医薬の高次構造評価を、独自のNMR技術開発により可能にした。
- バイオ医薬の代表格、抗体について、製剤保存条件における非破壊的なHOS情報の取得に成功した。
- バイオ医薬の高機能化を含む、創薬研究への幅広い貢献が期待される。
研究概要
バイオ医薬の躍進に伴い、その薬効および安全性をHOSに基づいて評価することが求められています。しかしながら、溶液組成や測定温度の制約を受けることなく、抗体などの高分子量バイオ医薬のHOS情報を取得する技術はこれまで確立されていませんでした。
そこで、東京大学大学院薬学系研究科および次世代天然物化学技術研究組合の嶋田一夫教授、産業技術総合研究所細胞分子工学研究部門の竹内恒 研究チーム長と徳永裕二研究員、中外製薬株式会社の奥出順也博士、小里一友博士、および鳥澤拓也博士のグループは、東京大学と産総研が保持するNMR測定技術を高度化し、高分子量条件においてNMR信号の生成効率を最大化する工夫を施すことで、感度・情報量を大幅に改善する窒素核観測CRINEPT法(以下、N-CRINEPT法)を開発しました。N-CRINEPT法により、HOS情報の網羅性がされるだけでなく、安価な安定同位体標識のみを施すことで、完全な非破壊性が実現されます。
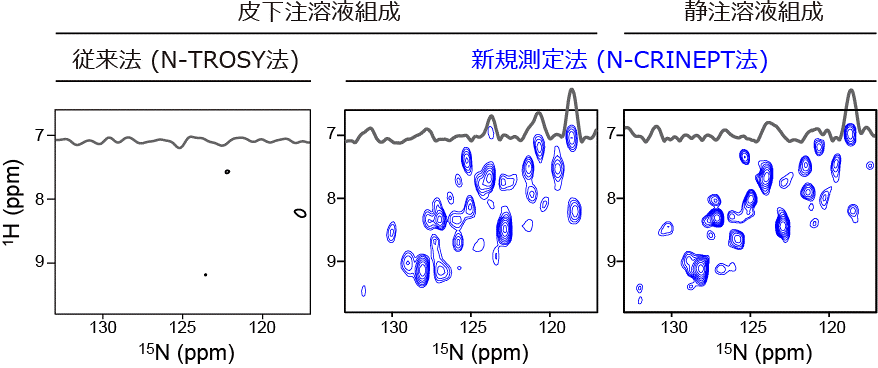
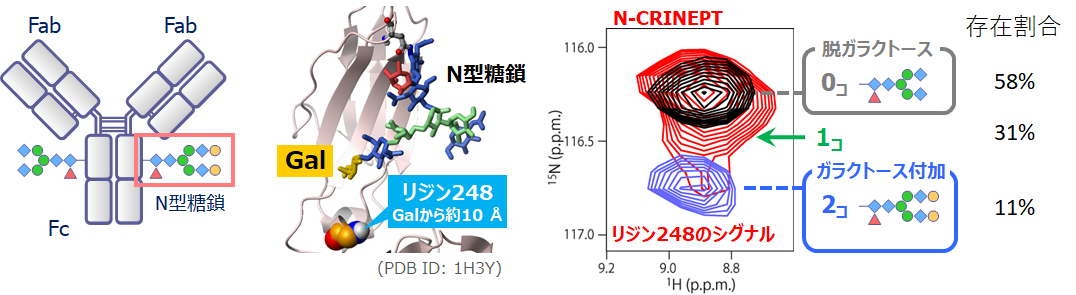
実際、N-CRINEPT法を、医薬品として使用されているものとほぼ同一の抗体分子(配列相同性が99%以上;以下、抗体医薬アナログ)に適用した結果、従来のNMR測定技術(N-TROSY)では全く検出できなかった抗体医薬アナログに由来するシグナルを、2つの異なる製剤組成下(皮下注および静脈注)、保存温度4℃で捉えることに初めて成功しました(図1)。さらに、N-CRINEPT法により、糖鎖末端のガラクトースの有無というわずかな変化に対しても、HOSの不均一性を定量的に検出することにも成功しました(図2)。よって、本手法により、抗体の糖鎖修飾をはじめとする様々な翻訳後修飾や溶液条件の違いがHOSに与える影響を検出できると期待され、生産、製剤化、保存、輸送などバイオ医薬の管理を必要とする様々な局面や、高機能化を目指す研究開発における活用が期待されます。なお、本手法は高分子量タンパク質の解析に広く適用できることから、タンパク質-タンパク質相互作用の立体構造解析や低分子、中分子などとの相互作用解析、様々なモダリティを活用する現在の創薬に、広く貢献するものです。本手法を用いることで、例えば、容易に発現できない大きなトランスポータータンパク質とその機能を阻害する中分子の相互作用を解析し、中分子の結合部位を明らかにして最適化に役立てるといった研究が可能となります。
この技術の詳細は、2020年05月06日(米国時間)に米国の科学誌Journal of Medicinal Chemistryに掲載されました。
注釈
- (注1)バイオ医薬
- タンパク質などの生体高分子を材料として製造された医薬品。古くはインスリンなどが知られているが、最近では、特に抗体を用いたバイオ医薬の開発が盛んになっている。
- (注2)高次構造(HOS; higher order structure)
- αヘリックスなどの2次構造や3次元立体構造などタンパク質の高次の構造を特徴づける概念。バイオ医薬は特定の高次構造を持つことで機能を果たす一方、その乱れは免疫原性等の原因となるため、薬効および安全性の観点から高次構造情報が重視される
- (注3)核磁気共鳴(NMR)法
- 水溶液に溶けたタンパク質などを、強力な磁場の中におくことで生じる「原子の共鳴現象」を観測することで、溶液中のタンパク質などの分子の構造や運動性の性質を原子レベルで調べることができる分光法。タンパク質試料を水溶液のままで解析できるため、製薬だけでなく、食品、材料、化学などさまざまな分野で活用されている。
- (注4)N-CRINEPT法
- NMR観測技術の一つで、アミド窒素の直接観測と、交差緩和による低感度核の感度増強を行う新たな実験スキームにより、分子量15万を超えるタンパク質のアミド基の観測を、重水素化を行うことなく可能にしたNMR測定方法。N-CRINEPT法では感度の高いアミド水素核から感度の低いアミド窒素核へ、交差緩和法を用いて磁化を移動し、感度を増大させている。また交差緩和による磁化の移動は、分子量が大きくなるほど速くなるという特性があるため、抗体などの高分子量タンパク質のNMRシグナルの観測が可能になった。
特記事項
※この研究は、日本医療研究開発機構(AMED)「次世代治療・診断実現のための創薬基盤技術開発事業」(革新的中分子創薬技術の開発)および「文部科学省科学研究費補助金」の支援によって行われました。
論文情報
- 雑誌名:
- Journal of Medicinal Chemistry(2020年5月6日オンライン版)
- 論文タイトル:
- Structural fingerprints of an intact monoclonal antibody acquired under formulated storage conditions via 15N direct detection nu-clear magnetic resonance
- 著者:
- Yuji Tokunaga, *Koh Takeuchi, Junya Okude, Kazutomo Ori, Takuya Torizawa, *Ichio Shimada
- DOI番号:
- 10.1021/acs.jmedchem.0c00231
お問い合わせ先
内容に関するお問い合わせ
国立大学法人東京大学大学院薬学系研究科 薬科学専攻
教授 嶋田 一夫(しまだ いちお)
TEL:03-5841-4810 FAX:03-5841-4818
E-mail:shimada“AT”iw-nmr.f.u-tokyo.ac.jp
AMEDの事業に関するお問い合わせ
国立研究開発法人日本医療研究開発機構
創薬事業部 医薬品研究開発課
次世代治療・診断実現のための創薬基盤技術開発事業担当
E-mail:jisedai-med“AT”amed.go.jp
(E-mailは上記アドレス“AT”の部分を@に変えてください)
関連リンク
掲載日 令和2年6月24日
最終更新日 令和2年6月24日


