皮膚バリア形成に最も重要な脂質(アシルセラミド)の産生の分子機構の全容を解明
プレスリリース
国立大学法人北海道大学
国立研究開発法人日本医療研究開発機構
研究成果のポイント
- 皮膚バリアに最も重要な脂質(アシルセラミド注1)の産生に関わる遺伝子(PNPLA1)を同定。
- アシルセラミド産生の分子機構の全容を解明。
- アトピー性皮膚炎や先天性魚鱗癬(ぎょりんせん)注2などの皮膚疾患の治療薬の開発に期待。
研究成果の概要
皮膚バリアは,病原体やアレルゲンなどの侵入を阻止する生体の防波堤のような役割をしています。そのため,皮膚バリアの異常は,アトピー性皮膚炎や魚鱗癬などの皮膚疾患を引き起こします。皮膚バリアの本体は脂質であり,その中でもアシルセラミドと呼ばれる脂質が最も重要です。木原教授らの研究グループは,アシルセラミド産生に関わる酵素遺伝子の中でも最後まで未同定なまま残されていた遺伝子(PNPLA1)の同定に成功し,アシルセラミド産生の分子機構の全容を解明しました。本研究により,皮膚バリア増強という新たな方策による皮膚疾患治療薬の開発が期待されます。
なお,本研究は,国立研究開発法人日本医療研究開発機構(AMED)の革新的先端研究開発支援事業(AMED-CREST)「画期的医薬品等の創出をめざす脂質の生理活性と機能の解明」研究開発領域(研究開発総括:横山信治)における研究開発課題「脂質による体表面バリア形成の分子機構の解明」(研究開発代表者:木原章雄)の一環として行われました。
論文発表の概要
- 研究論文名:
- Formation of the skin barrier lipid ω-O-acylceramide by the ichthyosis gene PNPLA1
(魚鱗癬原因遺伝子PNPLA1による皮膚バリア脂質アシルセラミドの産生) - 著者:
- 大野祐介,中路翔太,神山 望,木原章雄(北海道大学大学院薬学研究院)
- 公表雑誌:
- Nature Communications(DOI: 10.1038/NCOMMS14610)
- 公表日:
- 英国時間 2017年3月1日(水)午前10時(オンライン公開)
研究成果の概要
背景
私達の体は常に外界の病原体や汚染物質の侵入の脅威に曝されており,その最大の防御機構が皮膚によるバリアです。この皮膚バリアの本体は脂質で,皮膚の最も外側にある角質層に脂質の多層構造体が存在します。脂質は生体の水に溶けない物質の総称で,皮膚には皮膚にしか存在しない特殊な脂質アシルセラミド(セラミドの一種)が存在し,近年の研究から,アシルセラミドこそが皮膚バリアの機能に最も重要な脂質であることが分かってきました。アトピー性皮膚炎患者ではアシルセラミド量が低下しています。また,アシルセラミドが合成できない遺伝子異常は,先天性魚鱗癬と呼ばれる重篤な皮膚疾患を引き起こします。アシルセラミドの存在は30年以上も前から知られており,その重要性も認められてきましたが,生体内でアシルセラミドがどのように作られるのかは長年明らかにされてきませんでした。木原教授らの研究グループでは,アシルセラミド産生の分子機構の解明に取り組み,これまでにアシルセラミドの産生経路の中間体の解明,化学反応の順序の解明,数々のアシルセラミド関連酵素遺伝子の同定に成功してきました。しかし,アシルセラミド産生の最終ステップに関わる酵素遺伝子の同定が不明なまま残されていました。この酵素遺伝子の解明は,アシルセラミド産生の全容解明につながるだけでなく,皮膚バリア形成の分子機構解明のためにも重要な問題でした。
研究手法
アシルセラミドは,3つの構成成分(長鎖塩基,オメガ水酸化超長鎖脂肪酸,リノール酸)からなります。このうちの長鎖塩基とオメガ水酸化超長鎖脂肪酸が結合したオメガ水酸化超長鎖セラミドにリノール酸を付加するステップがアシルセラミド産生の最終ステップですが,その反応を触媒する酵素の遺伝子が未だ不明でした。研究グループはオメガ水酸化超長鎖セラミドを産生する培養細胞系を確立し,この細胞を用いてアシルセラミド産生活性の評価を行ってきました。脂質の検出は,質量分析または放射性同位体標識体の薄層クロマトグラフィーによる分離によって行いました。また,PNPLA1タンパク質を無細胞タンパク質翻訳系によってリポソーム存在下で合成し,生化学的に酵素活性を測定しました。野生型のPNPLA1タンパク質だけでなく,魚鱗癬患者に見られる変異型PNPLA1タンパク質の酵素活性も測定しました。
研究成果
本研究において,アシルセラミド産生の最終ステップを触媒する酵素遺伝子として,PNPLA1を同定することに成功しました。アシルセラミド産生は複数のステップからなり,各ステップに関わる遺伝子は表皮の角化細胞が分化した時に発現するのみで,通常の細胞には発現していません。一方,分化した角化細胞には遺伝子導入効率が低いという実験上の扱いづらさがあり,このことが長年アシルセラミド合成関連遺伝子の同定ができなかったことの一因でした。このような背景の中,研究グループはこれまでに,遺伝子導入効率が良い一般的な培養細胞中に同定してきた遺伝子群を導入することによって,アシルセラミドを産生できる系を確立してきました。本研究では,この細胞系を用いることで,今回PNPLA1の同定に成功しました。PNPLA1タンパク質はオメガ水酸化セラミドに脂肪酸であるリノール酸を付加してアシルセラミドを作り出す反応を触媒します。研究グループは,このリノール酸の供給源がトリグリセリド(グリセロールに3つの脂肪酸が付加した中性脂質)であること,PNPLA1タンパク質はトランスアシラーゼと呼ばれる酵素に分類されることも生化学的な手法によって明らかにしました。また,PNPLA1は先天性魚鱗癬の原因遺伝子として知られていましたが,今回の結果によって遺伝子変異と病態の関連も明らかになりました。
今後への期待
国民の約10人に1人がアトピー性皮膚炎と言われていますが,未だに対症療法に頼っており,根治可能な原因療法が存在しません。また,魚鱗癬の治療薬は全く存在しません。これらの皮膚疾患の有効な治療薬の開発には,病気の原因となっている皮膚バリアの回復が不可欠です。本研究により,アシルセラミド産生の分子機構の全容が解明されたことで,今後アシルセラミドの産生を増強する化合物の探索を行うことが可能となり,皮膚バリア増強という新たな方策による皮膚疾患治療薬の開発が期待されます。
お問い合わせ先
北海道大学大学院薬学研究院
教授 木原 章雄(きはら あきお)
TEL:011-706-3754 FAX:011-706-4900
E-mail:kihara”AT”pharm.hokudai.ac.jp
北海道大学総務企画部広報課
〒060-0808 札幌市北区北8条西5丁目
TEL:011-706-2610 FAX:011-706-2092
E-mail:kouhou”AT”jimu.hokudai.ac.jp
教授 木原 章雄(きはら あきお)
TEL:011-706-3754 FAX:011-706-4900
E-mail:kihara”AT”pharm.hokudai.ac.jp
北海道大学総務企画部広報課
〒060-0808 札幌市北区北8条西5丁目
TEL:011-706-2610 FAX:011-706-2092
E-mail:kouhou”AT”jimu.hokudai.ac.jp
AMED事業に関すること
国立研究開発法人日本医療研究開発機構(AMED)戦略推進部 研究企画課
東京都千代田区大手町1−7−1 読売新聞ビル22階
TEL:03-6870-2224
E-mail:kenkyuk-ask”AT”amed.go.jp
※E-mailは上記アドレス”AT”の部分を@に変えてください。
用語解説
- (注1)アシルセラミド:
- 表皮にのみ存在するセラミド分子種。皮膚バリア形成に重要。構造的には一般的なセラミドと異なり,脂肪酸部分のオメガ末端がアシル化(リノール酸の付加)されている。
- (注2)魚鱗癬(ぎょりんせん):
- その名の通り,表皮の角質層が異常に蓄積し,正常より厚くなって皮膚の表面が魚の鱗のように見える。
概念図
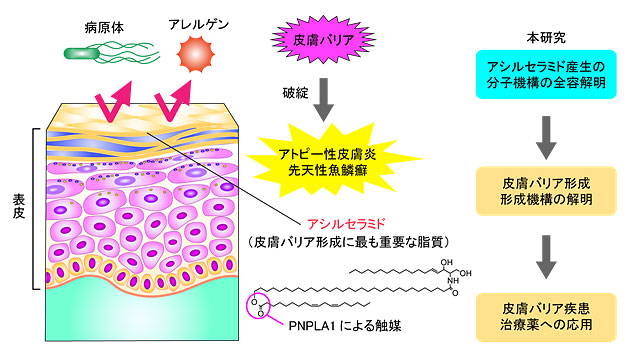
掲載日 平成29年3月2日
最終更新日 平成29年3月2日


