稀な病型の悪性リンパ腫に対する世界初の前向き臨床試験の結果公表―患者の予後の改善につながる標準的治療法を確立―
プレスリリース
名古屋大学
日本医療研究開発機構
名古屋大学医学部附属病院血液内科の島田 和之 講師、同大大学院医学系研究科血液・腫瘍内科学の清井 仁 教授、三重大学医学部附属病院血液内科の山口 素子 講師らは、IVL研究会(木下 朝博 代表)※1に参加する国内の多施設の研究者と共同して、血管内大細胞型B細胞リンパ腫(IVLBCL)※2の患者を対象にした世界初の前方向視試験※3を行い、IVLBCLに対する現在の標準的治療法(みなし標準といいます)を確立しました。
悪性リンパ腫は血液がんの一種であり、多様な病型を持つことが知られています。IVLBCLは稀な悪性リンパ腫の一病型であり、悪性リンパ腫の一般的な特徴であるリンパ節の腫れが認められないため、しばしば診断が難しいことで知られてきました。IVLBCLの治療は、従来、悪性リンパ腫の中で最も高頻度に生じるびまん性大細胞型B細胞リンパ腫(DLBCL)※4と同じR-CHOP療法※5が行われてきましたが、経過中における中枢神経(脳)への病変の広がりが多いことが、治療上の課題になっていました。また、稀で診断が難しいこともあって、IVLBCLに対する治療を評価した前方向視試験はこれまでになく、標準治療は未確立でした。
本研究では、R-CHOP療法と中枢神経への病変の広がりを予防する治療(高用量メトトレキサート療法※6と髄腔内抗がん剤注射)を組み合わせた治療を試験治療として、臨床第Ⅱ相試験※7を行いました。未治療で診断時に中枢神経に明らかな病変を認めないIVLBCLの38例の患者に対して試験治療を適用したところ、2年無増悪生存割合が76%、2年全生存割合が92%、2年中枢神経進展・再発累積割合が3%と良好な治療成績が得られました。副作用(有害事象)は許容の範囲内でした。本研究は、IVLBCLを対象にした世界で初めての前方向視試験であり、稀で大規模な臨床試験の実施が困難なことから、本研究の試験治療が、IVLBCLに対する現在の標準的治療法(みなし標準)と言えます。本試験治療は、現在の我が国での保険診療の範囲内で行うことが可能であり、この治療法により患者の予後の改善が期待されます。本研究は、日本医療研究開発機構(AMED)革新的がん医療実用化研究事業「未治療血管内大細胞型B細胞リンパ腫に対する治療研究」の支援により行われ、「The Lancet Oncology」電子版(グリニッジ標準時2020年3月11日23時30分付)に掲載されました。
ポイント
- 血管内大細胞型B細胞リンパ腫は、稀な悪性リンパ腫の一病型であり、リンパ腫の一般的な特徴であるリンパ節の腫脹を欠き、診断が難しいことで知られています。この病気の患者の治療では、リンパ腫の中で最も患者数が多いびまん性大細胞型B細胞リンパ腫と同じR-CHOP療法が行われてきましたが、中枢神経(脳)への病変の広がりが多いことが課題になっていました。
- 本研究では、血管内大細胞型B細胞リンパ腫の患者に対して、びまん性大細胞型B細胞リンパ腫の標準治療であるR-CHOP療法に中枢神経への病変の広がりを予防する治療(高用量メトトレキサート療法と髄腔内抗がん剤注射)を組み合わせる治療法について、安全性と有効性を調べる前方向視試験を行い、良好な治療成績が得られました。
- 本研究は、血管内大細胞型B細胞リンパ腫の患者を対象にした世界初の前方向視試験であり、この病気の患者に対する初めての標準的治療法(みなし標準)を確立したと言えます。
背景
血液がんの一種である悪性リンパ腫の中の一つの病型であるIVLBCLは、稀で、悪性リンパ腫の一般的な特徴であるリンパ節の腫れが認められないため、しばしば診断が難しいことで知られています。この病気の患者の治療は、悪性リンパ腫の中で最も患者数が多いDLBCLの治療と同じR-CHOP療法が行われてきましたが、残念ながら再発される患者も多く、特に中枢神経(脳)への病変の広がりを高頻度(20%程度)に認めることが治療上の課題になっていました。また、この病気の患者に対して、前方向視試験が行われたことがなく、標準治療は定まっていませんでした。
研究成果
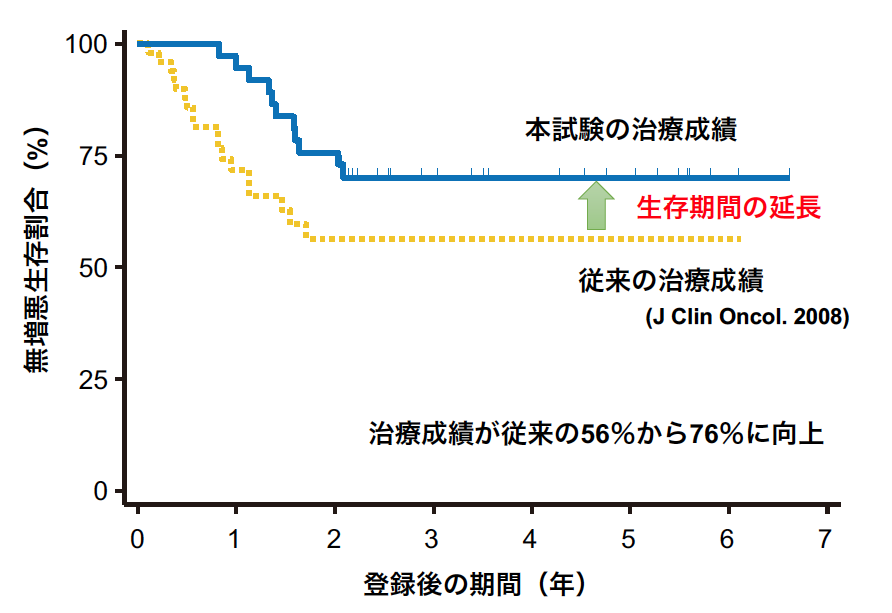
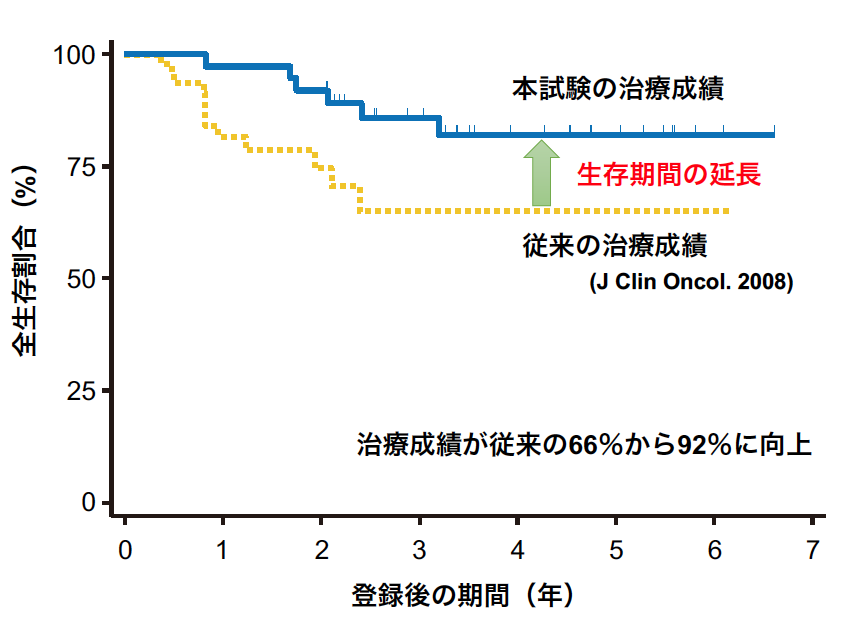
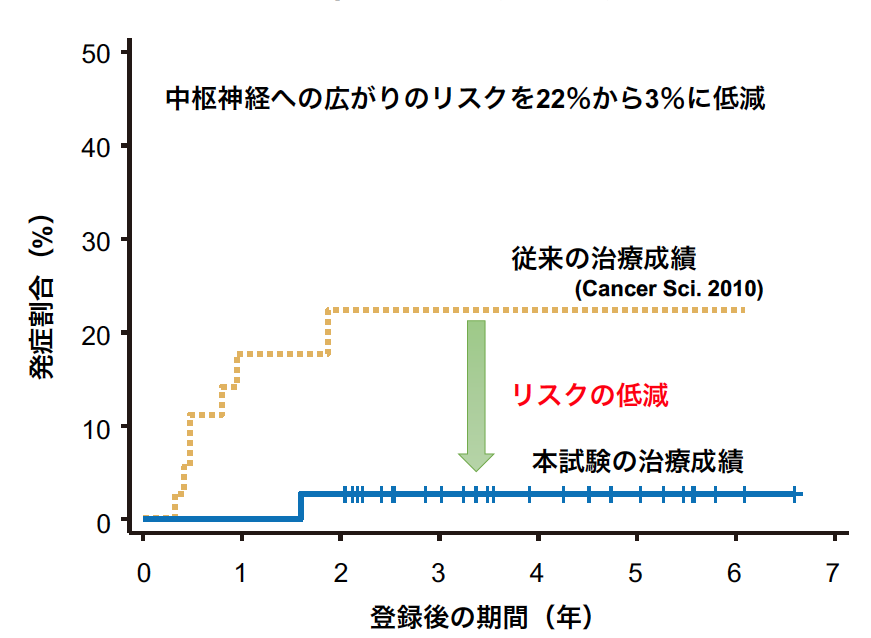
今回、世界で初めてIVLBCLの患者を対象に、DLBCLの標準治療であるR-CHOP療法に中枢神経への病変の広がりを予防する治療(高用量メトトレキサート療法と髄腔内抗がん剤注射)を組み合わせる治療について、安全性と有効性を調べる前方向視試験を行いました。未治療で診断時に中枢神経に明らかな病変を認めないIVLBCLの患者を対象に臨床第Ⅱ相試験を行い、38歳から78歳までの患者38名に参加いただきました。試験治療により、2年無増悪生存割合が76%(図1)、2年全生存割合が92%(図2)、2年中枢神経進展・再発累積割合が3%(図3)と良好な治療成績が得られ、副作用(有害事象)(表)は許容の範囲内でした。
| 表1.本試験治療で認められた主な有害事象 |
|---|
| 骨髄抑制(好中球減少、貧血、血小板減少など) |
| 骨髄抑制期の発熱(治療中の感染症を含む) |
| 血液検査値の異常(肝機能、電解質など) |
| 便秘・しびれ(末梢神経障害) |
| 悪心・食欲不振・嘔吐 |
| 脱毛 |
| 下痢 |
| 口腔粘膜炎 |
| など |
今後の展開
今回の研究成果により、未治療のIVLBCLに対して、世界初の前方向視試験の結果が示されました。稀で大規模な臨床試験を実施することが困難であることから、本研究で行われた試験治療が、現在の標準的治療法(みなし標準)と言えます。この研究で行われた治療は、現在の我が国での保険診療の範囲内で可能です。20歳から79歳までの患者には、すぐに実際の診療に応用することが可能になり、この病気の予後の改善が期待されます。
用語説明
- ※1 IVL研究会
- 血管内大細胞型B細胞リンパ腫に関する研究の趣旨に賛同した、国内の多施設の研究者が参加する研究グループ。
- ※2 血管内大細胞型B細胞リンパ腫(IVLBCL)
- 血液がんの中で最も発症する患者数が多い悪性リンパ腫の一種。日本では、全悪性リンパ腫の患者の1%程度を占めると推測されている。発熱、全身のだるさ、息切れなどの症状で発症する。悪性リンパ腫の特徴であるリンパ節の腫れを認めず、しばしば診断が困難であることが知られている。
- ※3 前方向視試験
- 予め定めた検査や治療などの手順に従って、患者に試験に参加いただき、主に治療の有効性を評価する臨床試験。
- ※4 びまん性大細胞型B細胞リンパ腫(DLBCL)
- 悪性リンパ腫の中で最も患者数が多い病型であり、全リンパ腫のおよそ30~40%を占める。リンパ節の腫れで発症するだけでなく、全身のさまざまな臓器から発症することがある。病気のタイプや発症部位により経過が異なることがあるため、後述のR-CHOP療法を基本にして病気に合わせた治療を行うことがある。
- ※5 R-CHOP療法
- DLBCLに対する現在の標準治療。リツキシマブ、シクロホスファミド、ドキソルビシン、ビンクリスチン、プレドニゾロンの5つの薬剤を組み合わせて行う多剤併用化学療法。
- ※6 高用量メトトレキサート療法
- 通常の抗がん剤より中枢神経への薬剤の移行に優れるメトトレキサートを用いた治療法。中枢神経にリンパ腫の病変が生じた際に用いられる。今回の試験治療では、通常の治療に用いられるより、回数を少なくして病変の広がりを予防する治療とした。
- ※7 臨床第Ⅱ相試験
- 前方向視試験の中で、比較的少数の患者を対象に、予め定めた治療薬や治療法の有効性と安全性を調べる臨床試験。
発表雑誌
- 掲雑誌名
- The Lancet Oncology(日本時間3月12日午前8時30分付の電子版)
- 論文タイトル
- Rituximab, cyclophosphamide, doxorubicin, vincristine, and prednisolone combined with high-dose methotrexate plus intrathecal chemotherapy for newly diagnosed intravascular large B-cell lymphoma (PRIMEUR-IVL): a multicentre, single-arm, phase 2 trial
- 著者
- Kazuyuki Shimada, Motoko Yamaguchi, Yoshiko Atsuta, Kosei Matsue, Keijiro Sato, Shigeru Kusumoto, Hirokazu Nagai, Jun Takizawa, Noriko Fukuhara, Koji Nagafuji, Kana Miyazaki, Eiichi Ohtsuka, Masataka Okamoto, Yasumasa Sugita, Toshiki Uchida, Satoshi Kayukawa, Atsushi Wake, Daisuke Ennishi, Yukio Kondo, Tohru Izumi, Yoshihiro Kin, Kunihiro Tsukasaki, Daigo Hashimoto, Masaaki Yuge, Atsumi Yanagisawa, Yachiyo Kuwatsuka, Satoko Shimada, Yasufumi Masaki, Nozomi Niitsu, Hitoshi Kiyoi, Ritsuro Suzuki, Takashi Tokunaga, Shigeo Nakamura, Tomohiro Kinoshita
- 所属
- Department of Hematology and Oncology, Nagoya University Graduate School of Medicine, Nagoya, Aichi, Japan (K Shimada MD, Prof H Kiyoi MD); Department of Hematology and Oncology, Mie University Graduate School of Medicine, Tsu, Mie, Japan (M Yamaguchi MD, K Miyazaki MD); Japanese Data Center for Hematopoietic Cell Transplantation, Nagoya, Aichi, Japan (Y Atsuta MD, A Yanagisawa BSc, Y Kuwatsuka MD); Division of Hematology/Oncology, Internal Medicine, Kameda Medical Center, Kamogawa, Chiba, Japan (K Matsue MD); Department of Hematology, Nagano Red Cross Hospital, Nagano, Japan (K Sato MD); Department of Hematology and Oncology, Nagoya City University Graduate School of Medical Sciences, Nagoya, Aichi, Japan (S Kusumoto MD); Department of Hematology, National Hospital Organization Nagoya Medical Center, Nagoya, Aichi, Japan (H Nagai MD, T Tokunaga MD); Department of Hematology, Endocrinology and Metabolism, Niigata University Faculty of Medicine, Niigata, Japan (J Takizawa MD); Department of Hematology and Rheumatology, Tohoku University Hospital, Sendai, Miyagi, Japan (N Fukuhara MD); Division of Hematology and Oncology, Department of Medicine, Kurume University School of Medicine, Kurume, Japan (Prof K Nagafuji MD); Department of Hematology, Oita Prefectural Hospital, Oita, Japan (E Ohtsuka MD); Department of Hematology, Fujita Health University School of Medicine, Toyoake, Aichi, Japan (Prof M Okamoto MD); Department of Hematology, Oami Municipal Hospital, Oamishirasato, Chiba, Japan (Y Sugita MD); Department of Hematology and Oncology, Japanese Red Cross Nagoya Daini Hospital, Nagoya, Aichi, Japan (T Uchida MD); Department of Clinical Oncology, Nagoya Memorial Hospital, Nagoya, Aichi, Japan (S Kayukawa MD); Department of Hematology, Toranomon Hospital Kajigaya, Kawasaki, Kanagawa, Japan (A Wake MD); Department of Hematology and Oncology, Okayama University Hospital, Okayama, Japan (D Ennishi MD); Department of Internal Medicine, Toyama Prefectural Central Hospital, Toyama, Japan (Y Kondo MD); Division of Hematology, Tochigi Cancer Center, Utsunomiya, Tochigi, Japan (T Izumi MD); Department of Hematology, Daini Osaka Police Hospital, Osaka, Japan (Y Kin MD); Department of Hematology, National Cancer Center Hospital East, Kashiwa, Chiba, Japan (Prof K Tsukasaki MD); Department of Hematology, Hokkaido University Faculty of Medicine, Graduate School of Medicine, Sapporo, Japan (D Hashimoto MD); Division of Hematology, Ichinomiya Municipal Hospital, Ichinomiya, Aichi, Japan (M Yuge MD); Department of Advanced Medicine (Y Kuwatsuka MD), and Department of Pathology and Clinical Laboratories (S Shimada MD, Prof S Nakamura MD), Nagoya University Hospital, Nagoya, Aichi, Japan; Department of Hematology and Immunology, Kanazawa Medical University, Uchinada, Ishikawa, Japan (Prof Y Masaki MD); International Medical Center, Saitama Medical University, Hidaka, Japan (Prof N Niitsu MD); Department of HSCT Data Management and Biostatistics, Nagoya University School of Medicine, Nagoya, Aichi, Japan (R Suzuki MD); Division of Hematology and Cell Therapy, Aichi Cancer Center, Nagoya, Aichi, Japan (T Kinoshita MD)
- DOI
- 10.1016/S1470-2045(20)30059-0
- URL
- http://www.thelancet.com/journals/lanonc/article/PIIS1470-2045(20)30059-0/fulltext
お問い合わせ先
研究について
名古屋大学大学院医学系研究科
血液・腫瘍内科学 教授 清井 仁
TEL:052-744-2136 FAX:052-744-2157
E-mailkiyoi“AT”med.nagoya-u.ac.jp
広報担当
名古屋大学医学部・医学系研究科総務課総務係
TEL:052-744-2228 FAX:052-744-2785
E-mail:iga-sous“AT”adm.nagoya-u.ac.jp
AMED事業に関すること
国立研究開発法人日本医療研究開発機構(AMED)
戦略推進部 がん研究課
〒100-0004 東京都千代田区大手町一丁目7番1号
TEL:03-6870-2221
E-mail:cancer“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
関連リンク
掲載日 令和2年3月12日
最終更新日 令和2年3月12日


