前立腺癌における新たなエクソソーム分泌機構を解明―エクソソームを標的とした新たな前立腺癌治療法への期待―
プレスリリース
東京医科大学
東京慈恵会医科大学
テオリアサイエンス株式会社
日本医療研究開発機構
概要
東京医科大学医学総合研究所の落谷孝広教授らと東京慈恵会医科大学・泌尿器科学講座の頴川晋教授、占部文彦助教、およびテオリアサイエンス株式会社(代表:水谷隆之)らの共同研究チームは、独自に開発したスクリーニング法を用いて、前立腺癌における新たなエクソソーム分泌機構を解明しました。本研究成果は、2020年4月29日14時(米国東部標準時間)米国科学誌「Science Advances」電子版に掲載されました。
本研究により、エクソソームを標的とした新しいがん治療法の開発が期待されます。
研究の背景
エクソソームは、さまざまな種類の細胞が分泌する100nm程の脂質二重膜で囲まれた小胞で、細胞間相互作用に重要な役割を担っていることが知られています。特にがん細胞由来のエクソソームは、がん細胞の周辺の細胞を制御し、がんの進展に関わることがこれまでに多数報告されています。さらに、がん細胞は正常細胞よりもエクソソームの分泌量が多い傾向にあるため、エクソソームの分泌はがんの様々な悪性段階に関わると考えられています。そこで、最近では、がん細胞由来のエクソソームの分泌を抑制することが新しいがんの治療法になると注目されています。
これまでにエクソソームの分泌に関わる遺伝子としてRAB27やnSMASE2 (※1)などが報告されていました。しかしながら、これらの遺伝子は、がん細胞特異的に高発現している遺伝子ではないため、がん細胞のみを標的とすることができず、選択性に乏しいことから治療標的とすることが困難とされてきました。
本研究では、前立腺癌におけるエクソソーム分泌について網羅的な解析を行い、その特異的な分泌機構を明らかにすることにより、前立腺癌の新たな治療標的を同定することを目指しました。
本研究で得られた結果・知見
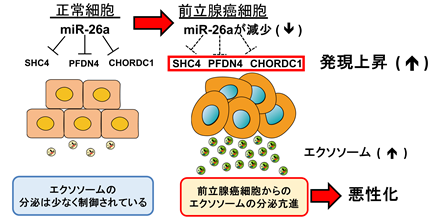
今回、同研究チームは、独自に開発したエクソソームの超高感度測定法であるExoScreen法(※2)(吉岡ら、Nat Commun、2014)と、マイクロRNAライブラリー(※3)を組み合わせた、がん細胞におけるエクソソーム分泌関連遺伝子のスクリーニング法を新たに開発しました。エクソソームを網羅的に測定できるExoScreen法と、様々な遺伝子の発現を同時に抑制することが知られているマイクロRNAを組み合わせたこの方法を用いて、前立腺癌細胞株を対象にスクリーニングを行い、miR-26a(※4)とその制御遺伝子であるSHC4、PFDN4、CHORDC1(※5)がエクソソームの分泌を制御していることを同定しました(図1)。
次いで、これらの遺伝子の発現を抑制した前立腺癌細胞をマウスに移植したところ、エクソソームの分泌が低下し、担がんマウスにおける腫瘍の増大が抑えられました。さらにエクソソームの分泌が低下した前立腺癌細胞移植時に移植部位に前立腺癌細胞から分泌されるエクソソームを同時に注入すると、腫瘍の増殖が回復することがわかりました。
今後の研究展開および波及効果
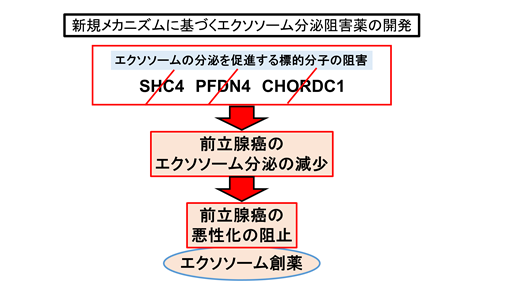
本研究で同定した、前立腺癌のエクソソーム分泌を制御する遺伝子(SHC4, PFDN4, CHORDC1)は過去にがんの悪性化に関わるとの報告はなく、前立腺癌の治療としてこれらの遺伝子を標的とした薬剤の開発が期待されます。また、従来の治療法とは異なる、エクソソーム治療という、新たな治療法確立への道を拓くことが期待されます(図2)。
さらに本研究において確立されたスクリーニング技術は、他のがん種においても利用可能であり、さまざまながん種のエクソソーム分泌機構の解明に役立つと考えられます。
用語解説
- ※1 RAB27やnSMASE2:
- これらの分子は細胞内で、エクソソームの分泌過程に働いているとされる。
- ※2 ExoScreen法:
- 同・東京医大の研究チームが2014年に開発した体液中や培養液中のエクソソームを好感度に検出する方法。Nature Communications誌に発表。
- ※3 マイクロRNAライブラリー:
- マイクロRNAを模したmimicからなるライブラリー、マイクロRNAの機能的スクリーニングなどに用いる。
- ※4 miR-26a:
- マイクロRNAの一種。マイクロRNAは細胞内に存在する長さ21~25塩基長のnoncoding RNA(非翻訳RNA)。このマイクロRNAは、平滑筋細胞の分化制御や、肝癌など悪性腫瘍、転移・浸潤能、血管新生などに関する報告がなされていた。
- ※5 SHC4、PFDN4、CHORDC1:
- miR-26aによってその発現が制御(抑制)される遺伝子群。これらの遺伝子がエクソソームの分泌促進を介してがん悪性化に関与している。
論文情報
- 掲載誌名
- Science Advances
- 論文タイトル
- miR-26a regulates extracellular vesicle secretion from prostate cancer cells via targeting SHC4, PFDN4, and CHORDC1.
- 著者
- Urabe F, Kosaka N*, Sawa Y, Yamamoto Y, Ito K, Yamamoto T, Kimura T, Egawa S, Ochiya T.
*小坂展慶(責任著者) - DOI
- 10.1126/sciadv.aay3051
- URL
- https://advances.sciencemag.org/content/6/18/eaay3051
主な競争的研究資金
- AMED 革新的がん医療実用化研究事業「がん悪性化に寄与する細胞外小胞顆粒の分泌制御因子を標的とした治療薬の開発」
研究代表者:小坂展慶 - AMED 次世代がん医療創生研究事業「がん特異的エクソソームの捕捉による新規体液診断の実用化研究」
研究代表者:落谷孝広
その他の研究資金
- テオリアサイエンス株式会社(代表:水谷隆之)による東京医科大学・産学連携講座「細胞外小胞創薬研究講座」
お問い合わせ先
本研究に関する問い合わせ先
東京医科大学 医学総合研究所 分子細胞治療研究部門
落谷 孝広
E-mail:tochiya”AT”tokyo-med.ac.jp
東京慈恵会医科大学 泌尿器科学講座
占部 文彦
E-mail : h18ms-urabe”AT”jikei.ac.jp
AMED事業に関すること
国立研究開発法人日本医療研究開発機構
創薬事業部 医薬品研究開発課
E-mail:cancer”AT”amed.go.jp
プレスリリースに関するお問い合わせ
東京医科大学 総務部 広報・社会連携推進課
TEL: 03-3351-6141(代表)
E-mail:d-koho”AT”tokyo-med.ac.jp
学校法人慈恵大学 経営企画部 広報課
TEL: 03-3433-1111(代表)
E-mail: koho”AT”jikei.ac.jp
※上記の”AT”は@に置き換えてください。
掲載日 令和2年4月30日
最終更新日 令和2年4月30日


