線維性被膜が薄いプラークへのEPAの優先的な取り込み―魚油の抗動脈硬化作用の解明に貢献―
成果情報
国立大学法人浜松医科大学
国立研究開発法人日本医療研究開発機構(AMED)
概要
浜松医科大学・細胞分子解剖学講座の佐藤智仁特任助教と瀬藤光利教授らは、動脈硬化モデルマウスに経口投与したEPA(エイコサペンタエン酸)が、線維性被膜の薄いプラークに優先的に取り込まれることを見出しました。
この成果は、米国心臓協会 (American Heart Association: AHA)の学術雑誌「Arteriosclerosis, Thrombosis, and Vascular Biology」に8月1日に掲載されました。
研究の背景
動脈硬化が進むと血管壁に脂質やマクロファージの死骸、増殖した血管平滑筋細胞などが集積し、いわゆる「プラーク」が形成されます。プラークを覆っている線維性被膜が破綻し、コレステロールを主成分とする沈着物が血管内に漏出すると、血栓という血の塊を作り、容易に血管を閉塞させてしまいます。これが心臓で発生すると心筋梗塞になります。一般的に、線維性被膜の薄いプラークは、破綻しやすい不安定なプラークと考えられています。
魚油で知られるオメガ3系脂肪酸*1のEPAやDHA(ドコサヘキサエン酸)が、抗動脈硬化作用を持つことや、動脈硬化のプラークに集積することは過去に報告されていますが、プラーク内でどのような分布を示すか、どのようなプラークに取り込まれやすいか、また、取り込まれる際に他の脂質分子とどのような関連があるかについては不明なままでした。
研究の成果
研究グループは、動脈硬化モデルであるApoe-/-マウスにEPAを投与し、プラークが形成されやすい大動脈という太い血管内にできたプラークを質量顕微鏡*2により解析することで、EPAは線維性被膜の厚いプラークに比べて、薄いプラークにより多く取り込まれやすいことを見出しました。また、オメガ3系脂肪酸はプラークの血管内腔側に多く分布し、深部にかけて少なく分布することや(参考図)、主にコレステロールエステルの形態で取り込まれることが明らかとなりました。さらに近年、炎症を収束させる機能を有するとして注目を集めているオメガ3系脂肪酸代謝物*3の12-HEPE(12-hydroxy-eicosapentaenoic acid)や14-HDoHE(14-hydroxy-docosahexaenoic acid)のプラーク内分布のイメージングに成功し、経口投与したEPAやDHAがプラークの局所において、抗動脈硬化作用を示す様子を視覚的に捉えることができました。
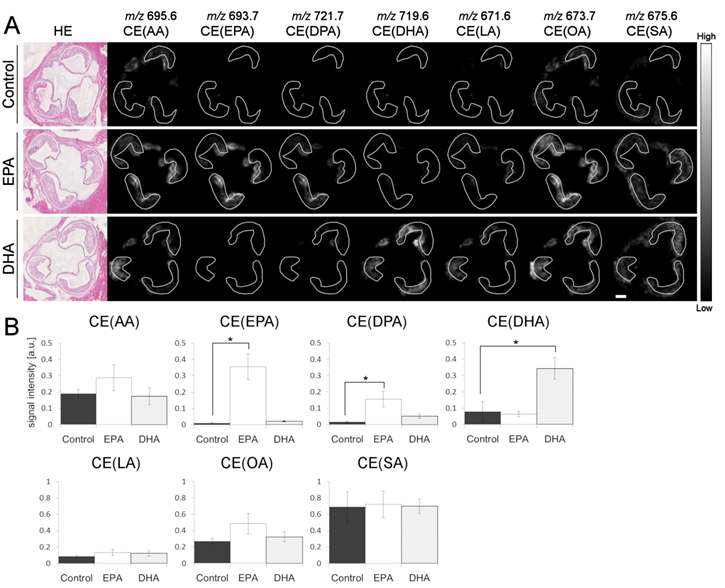
図B:各脂質分子のシグナル強度を比較すると、EPA投与群においてEPAと結合したコレステロールエステルCE(EPA)が、DHA投与群においてDHAと結合したコレステロールエステルCE(DHA)が有意に強く検出された。
CE(AA):コレステロールエステル(アラキドン酸と結合した)、AA:アラキドン酸、EPA:エイコサペンタエン酸、DPA:ドコサペンタエン酸、DHA:ドコサヘキサエン酸、LA:リノレン酸、OA:オレイン酸、SA:ステアリン酸
今後の展開
今回の研究成果は、高解像度のイメージングを可能とするマトリクス支援レーザー脱離イオン化法(MALDI)や、遊離脂肪酸とその代謝物の検出を得意とする脱離エレクトロスプレーイオン化法(DESI)、遊離脂肪酸とフラグメントの脂肪酸の総数を検出することに特化した銀ナノ粒子を用いたnano-PALDI法など、複数のイオン化手法と質量顕微鏡装置を用いることにより、遊離脂肪酸や、他の脂質分子から分離した脂肪酸、脂肪酸代謝物など様々な形態の脂質分子の分布を解析できることを示しており、これら手法は他の様々な脂質関連疾患の研究へも応用可能です。
また、EPAがフォスファチジルコリンのような他のリン脂質ではなく、主にコレステロールエステルとしてプラーク内へ取り込まれることは、これまで悪いもの、動脈硬化の元凶と考えられがちなコレステロールが、同時にEPAの運搬を担う運び屋として機能していることを示しています。これは、単に血中コレステロールの低下のみを動脈硬化治療の目標とするのではなく、血管内の脂質全体をコントロールすることの重要性を示唆しています。
EPAなどのオメガ3系脂肪酸が被膜の薄いプラーク、すなわち不安定プラークへ優先的に取り込まれることは、不安定なプラークを有する患者を対象として、早期にEPAによる治療介入を行うことで、プラーク破綻、心筋梗塞の発生率を抑えることができる可能性を示唆しています。
こうした発見は、創薬研究や不安定なプラークを有する患者群を対象とした臨床研究などへ発展することが期待されます。
用語説明
- *1 オメガ3系脂肪酸:
- 構造上、末端のメチル基より3番目の炭素に二重結合があることから、オメガ3系脂肪酸とよばれるEPA、DHA、α-リノレン酸などの脂肪酸は、魚貝類や海藻類に多く含まれる。炎症や血栓、動脈硬化を抑制することで知られている。
- *2 質量顕微鏡:
- 組織切片上の様々な質量範囲の生体分子を、網羅的にかつ局在情報を保持したまま取得することで、多数の生体分子の分布を解析する手法。
- *3 脂肪酸代謝物:
- オメガ3系脂肪酸由来の活性代謝物は、炎症収束を促進する新しいタイプの抗炎症性脂質メディエーターとして注目されている。
発表雑誌
Arteriosclerosis, Thrombosis, and Vascular Biology
論文タイトル
Preferential Incorporation of Administered Eicosapentaenoic Acid Into Thin-Cap Atherosclerotic Plaques.
著者
Tomohito Sato, Makoto Horikawa, Shiro Takei, Fumiyoshi Yamazaki, Takashi K. Ito, Takeshi Kondo, Takanobu Sakurai, Tomoaki Kahyo, Koji Ikegami, Shumpei Sato, Ryota Sato, Yasutaka Jinno, Hiroyuki Kawano, Satoko Naoe, Makoto Arita, Yukiyasu Kashiwagi, Mitsutoshi Setou
(佐藤智仁、堀川誠、武井史郎、山崎文義、伊藤孝、近藤豪、櫻井孝信、華表友暁、池上浩二、佐藤駿平、佐藤亮太、神野泰隆、河野浩之、直江智子、有田誠、柏木行康、瀬藤光利)
研究支援
本研究は浜松医科大学細胞分子解剖学講座、理化学研究所生命科学研究センターメタボローム研究チーム、持田製薬株式会社、地方独立行政法人大阪産業技術研究所ナノマテリアル研究室との共同研究で、国立研究開発法人日本医療研究開発機構(AMED)の革新的先端研究開発支援事業(AMED-CREST)「画期的医薬品等の創出をめざす脂質の生理活性と機能の解明」研究開発領域(研究開発総括:横山信治)における研究開発課題「光による脂質の同定制御観察技術すなわちオプトリピドミクスの創生」(研究開発代表者:瀬藤光利)、日本学術振興会の新学術領域研究、文部科学省先端研究基盤共用促進事業「原子・分子の顕微イメージングプラットフォーム」、公益財団法人持田記念医学薬学振興財団からの研究費を受けてまとめられた成果です。
本件に関するお問い合わせ先
国立大学法人浜松医科大学細胞分子解剖学講座
〒431-3192 浜松市東区半田山1-20-1
特任助教 佐藤 智仁
TEL:053-435-2085
FAX:053-435-2468
E-mail:07485496"AT"hama-med.ac.jp
AMED事業に関するお問い合わせ先
国立研究開発法人日本医療研究開発機構(AMED)
基盤研究事業部 研究企画課
〒100-0004 東京都千代田区大手町1-7-1 読売新聞ビル
TEL:03-6870-2224 E-mail:kenkyuk-ask”AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
掲載日 令和元年11月20日
最終更新日 令和元年11月20日


