令和6年度 「医療機器等における先進的研究開発・開発体制強靭化事業(医療機器開発体制強靱化)」に係る公募について
基本情報
| 公募の段階 | 公募 |
|---|---|
| 開発フェーズ | 応用,非臨床研究・前臨床研究,臨床試験,治験 |
| 分野 | 医療機器・ヘルスケアプロジェクト,感染症,その他の疾患 |
| 公募締め切り | 令和6年3月14日(木) 12時00分00秒【厳守】※締め切りに間に合わず不受理となるケースが発生していますので、余裕を持った対応をお願いします。特にe-Radの新規利用者は、研究機関/研究者の新規登録手続も必要であり、これらに要する日数も考慮の上、早めの対応をお願いします。AMEDではe-Radに登録された研究提案情報をダウンロードして評価システムに組み入れています。提案書の記載情報とe-Radへの入力情報に齟齬がないよう、提案前に双方の記載内容を十分確認してください。 |
| お問い合わせ先 |
|
公募内容
新型コロナウイルス等の感染症、各種災害等の非常事態において国民の生命を守るためには、状況に応じて必要な医療機器を迅速に医療現場等に供給できることが必要です。今般の新型コロナウイルス感染症や国際情勢の変化により、国内外で人工呼吸器や体外式膜型人工肺(ECMO)等の医療機器不足や、医療機器の製造に必要な原材料の入手難に直面するなど、安定供給リスクが顕在化しました。
本事業では、非常事態において必要な医療機器、又は本邦の医療提供の維持に必要な医療機器について、国内生産体制を構築し、将来にわたって維持していくことを目標とし、事業終了時において、検証的試験を終えて薬事承認申請の目途が立っていること、提案医療機器の国内生産体制を構築する目途が立っていることを成果とし、「医療機器等における先進的研究開発・開発体制強靭化事業(医療機器開発体制強靱化)」に係る公募を行います。
各分野に定める医療機器については、供給途絶リスクを低減し、国内生産体制の構築・維持に資する研究開発を対象とします。
なお、各採択分野に定める医療機器のうち、①感染症、各種災害等の非常事態の対応に必要となる医療機器、または②我が国の医療提供の維持に必要な医療機器であり、かつ供給途絶リスクの高いものの例としては、以下のとおりです。(以下はいずれも例示であり、対象とする医療機器をこれらに限定するものではありません。)
- 人工呼吸器
- 体外式膜型人工肺(ECMO)
- 透析関連装置
- 生体情報モニタ
- IABPバルーンカテーテル
- 逐次型空気圧式マッサージ器
- 胸腔排液用装置
- 体内固定用組織ステープル
- 癒着防止材
供給途絶リスクの高いものについては、薬事工業生産動態統計調査その他のデータより、高い輸入依存度であることが客観的に示されているものや、国内生産している場合であっても部素材にサプライチェーンにおいて特定の地域への依存度が高いものが該当します。
これらの医療機器の国内生産を維持するために、既存製品の課題解決により競争力強化に資する開発・改良や、特定地域に依存する希少部素材の使用量を低減するための開発・改良を行う研究開発を推奨します。
また、提案医療機器が感染症、各種災害等の非常事態の対応、及び我が国における医療提供の維持に必要となるものであり、供給途絶が生じた場合に国民の生命にかかわる医療機器であるという点を明確にした提案を求めます。
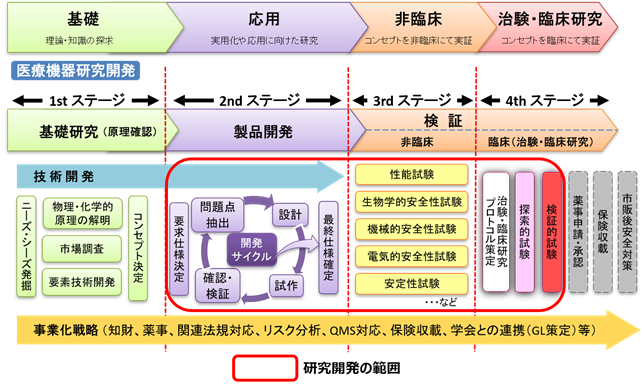
研究開発フェーズ
本プロジェクトで主として対象とする開発フェーズは、応用~臨床フェーズとなります。医療機器本体(部品・消耗品は除く)を提案する場合には、提案時に、提案医療機器のコンセプトが既に決定されており、プロトタイプ機に準ずる機器があるものが望まれます。また、上市済みの医療機器の製造販売承認事項一部変更等も対象とします。
対象となる研究開発の範囲
公募詳細
本公募の補助金の規模・事業実施期間・新規採択課題予定数等について、下表に示します。
| # | 分野、領域、テーマ等 | 補助金額 (間接経費を含まず) |
研究開発実施 予定期間 |
新規採択課題 予定数 |
|---|---|---|---|---|
| 1 | 供給途絶リスク等がある医療機器※1(医療機器本体※2)の開発・改良 | 1課題当たり年間 82,000千円(上限) |
令和6年5月(予定)
~ 令和8年度末
|
0~1課題程度 |
| 2 | 供給途絶リスク等がある医療機器※1(医療機器本体以外※2)の開発・改良 | 1課題当たり年間 36,000千円(上限) |
0~1課題程度 |
※1 供給途絶リスク等がある医療機器とは、感染症、各種災害等の非常事態の対応に必要となる医療機器または我が国の医療機器の維持に必要な医療機器であって、供給途絶リスクがあり、かつ国内生産を維持できる医療機器を意味します。また、供給途絶リスクがある医療機器とは、輸入依存度が高い医療機器や、特定の地域に依存し希少性の高い資源・原材料・部品等を使用する医療機器等を意味します。
※2 医療機器本体とは、医療機器本体の新規開発又は競争力強化を伴う開発を意味し、医療機器本体以外とは、機器関連の付属品、消耗品等の開発、本体部品の代替品開発を意味します。
【注意事項(抜粋)】その他、内容詳細については公募要領p.3を必ずご確認ください。
- 補助金額等は、申請額がそのまま認められることを確約するものではありません。また研究開発実施予定期間は、予算の成立状況によっては、期間の途中でも研究開発支援が終了することがあります。
- 課題申請時に規定されていた予算上限を超えていた場合は不受理とします。
- 複数の公募研究開発課題への応募は認められますが、研究費の不合理な重複及び過度の集中(詳細は第4章を参照してください。)に該当しないことを確認するため、同時に応募した研究開発課題の情報を研究開発提案書の該当欄へ必ず記載してください。また、応募中の研究開発課題が採択された場合は、速やかにAMEDの本事業担当課に報告してください。
- 当該公募年度に既に研究開発代表者、補助事業代表者として医療機器等における先進的研究開発・開発体制強靭化事業に参画している場合は、補助事業代表者として本公募に応募できません。
- 採択課題数は、それぞれの分野における応募の数、また内容に応じて、予定数から増減します。
- 補助金額は、補助対象経費に補助率2/3を乗じた金額となります。
事業概要
事業の現状
新型コロナウイルス等の感染症、各種災害等の非常事態において国民の生命を守るためには、状況に応じて必要な医療機器を迅速に医療現場等に供給できることが必要です。今般の新型コロナウイルス感染症においては、世界的なパンデミックの影響により国内外で人工呼吸器や体外式膜型人工肺(ECMO)等の医療機器不足に直面するなど、グローバルサプライチェーンに伴う安定供給リスクが顕在化しました。
我が国においては、従前より医療機器の多くを海外からの輸入に頼っており、医療の安全保障の観点からも、非常事態において必要な医療機器を国内で生産できる体制を構築することが課題となっています。非常事態において必要な医療機器を国内で生産できるためには、平時より国内で継続供給する体制とともに、有事に備えて国内生産設備やサプライチェーンを整えておくことも重要です。近年のBCP(事業継続計画)の重要性の高まりとともに、医療機器産業の国際競争力の強化・イノベーションの創出推進も課題となっています。また、サプライチェーンの混乱に伴い希少性の高い資源・原材料の入手困難等の課題も生じています。
今般の新型コロナウイルス感染症への対応にあたっては政府において人工呼吸器等の医療機器について設備投資支援等により国内生産体制の構築を支援してきました。本事業では非常事態において必要な医療機器を生産できるようにするための研究開発を支援します。
事業の目標と成果
本事業では、非常事態において必要な医療機器、又は本邦の医療提供の維持に必要な医療機器について、国内生産体制を構築し、将来にわたって維持していくことを目標とし、事業終了時において、検証的試験を終えて薬事承認申請の目途が立っていること、提案医療機器の国内生産体制を構築する目途が立っていることを成果とします。
応募資格者
本事業の応募資格者は、別に定める要件を満たす国内の民間企業に所属し、かつ、主たる研究場所とし、応募に係る補助事業課題について、補助事業実施計画の策定や成果の取りまとめなどの責任を担う代表者(補助事業代表者)とします。
本事業の代表機関は、医療機器の製造販売業許可を有する国内の民間企業とし、応募に係る補助事業課題について、事業計画の策定や成果の取りまとめなどの責任を担う機関とします。
※詳細について、公募要領p.8「3.1応募資格者」を参照ください。
公募期間
※ 全ての研究開発提案書、承諾書類等について、期限を過ぎた場合には一切受理出来ませんのでご注意ください。
公募説明会
公募説明
公募説明会は開催しません。
公募要領の記載内容、提出書類の記入方法等については、【公募説明資料】をご参照ください。
個別相談
既に公募期間中につき、具体的な提案内容に関わる問い合わせには個別にお答え出来ませんのでご容赦ください。
不明点、ご質問
何かご不明な点、ご質問等などございましたら、mailにて連絡をお願いします。
医療機器・ヘルスケア事業部 医療機器研究開発課 担当
E-mail: A-kiki“AT”amed.go.jp
※ E-mailは上記アドレス“AT”の部分を@に変えてください。
※ メールタイトル文頭に必ず【R6強靱化】と記載ください。
応募方法
応募は、e-Rad(府省共通研究開発管理システム)を通じて申請します。提案書類の詳細は、公募要領の「第5章 提案書等の作成 ・提出方法」の記載を確認の上、作成願います。補助事業代表者が応募に必要な書類を指示されたファイル形式でe-Radへアップロードします。
応募に必要な提案書類
| No. | 必須/任意 | 必要な提案書類 | 備考 |
|---|---|---|---|
| 1 | 必須 | (様式1)補助事業提案書※2 | PDFファイル/e-Radによる提出※1 |
| 2 | 必須 | (様式2)承諾書(代表機関)※3 | |
| 3 | 必須 | (様式3)医療機器開発マネジメントに関してのチェック項目記入表書 | |
| 4 | 任意 | (様式4)賃金引上げ計画の表明書※4 | |
| 5 | 必須 | (様式5)研究内容と開発対象物に関する概要※5 | |
| 6 | 該当する場合は必須 | (様式6)ヒト全ゲノムシークエンス解析プロトコール様式 |
応募先
スケジュール
| 提案書類の受付期間・選考スケジュール | |
|---|---|
| 提案書類受付期間 | 令和6年2月15日(木)~令和6年3月14日(木)【12:00:00(JST)】(厳守) |
| 書面審査 | 令和6年3月中旬~令和6年3月下旬(予定) |
| ヒアリング審査 | 令和6年4月10日(水)(予定) |
| 採択可否の通知 | 令和6年4月下旬(予定) |
| 補助事業開始(交付決定等) | 令和6年5月下旬(予定) |
資料
掲載日 令和6年2月15日
最終更新日 令和6年2月15日


