日本人に多い肺がん(肺腺がん)の新たな治療標的及び術後予後の予測マーカーを発見
プレスリリース
国立がん研究センター
順天堂大学
日本医療研究開発機構
発表のポイント
- これまで明らかでなかった日本人の軽喫煙者・非喫煙者の肺腺がんの遺伝子異常について996例を調べて、変異EGFRなどのドライバー遺伝子注1のない125例について網羅的ゲノム解析を行い、新たながん遺伝子を発見しました。
- ドライバー遺伝子陰性肺腺がんの約7割に、治療の標的となる遺伝子変異を同定しました。
- 術後再発のリスクを予測可能な、術後予後の予測マーカーを新たに同定しました。
概要
国立研究開発法人国立がん研究センター研究所細胞情報学の高阪 真路 主任研究員、間野 博行 分野長、順天堂大学人体病理病態学講座の林 大久生 准教授、同大呼吸器外科学講座の高持 一矢 准教授らの研究グループは、軽喫煙者・非喫煙者の肺腺がんの悪性化に関わるメカニズムを解明し、発がんの原因となる遺伝子変異を新たに明らかにしました。また、手術後再発のリスクの予測に重要な3種類の遺伝子を同定することに成功しました。
肺腺がんは、日本人の肺がんで多く、非喫煙者や女性でも発症しますが、非喫煙者は喫煙者に比べ一般的に遺伝子変異数が少なく、発症原因や治療標的が明らかでないため、研究開発が強く求められていました。
本研究成果は、米国科学雑誌「Journal of Thoracic Oncology」に、2月26日付で掲載されました。
背景
日本における成人の死因の第1位はがんであり、その中で肺がんはがん死亡原因のトップです。現在、日本で年間に約12万5千人が肺がんを発症し、7万人以上が肺がんで死亡しています。肺がんの約2/3の患者が手術不能の進行がんとして発見され、抗がん剤による薬物治療や放射線治療などを受けています。しかし、治療効果は十分でなく、より効果的な新たな治療法の開発が期待されています。
肺がんの組織型の中で最も多いのは肺腺がんであり、非喫煙者の女性も罹るがんです。肺腺がんは以前は原因の判らないがんと考えられていましたが、遺伝子解析技術の進歩により、vKRAS, EGFR, ALK, RET, ROS1, BRAFなどの遺伝子変異と関連があるがんとして注目され、分子標的治療薬注2による治療も著しく進歩してきています。
研究成果
本研究では非喫煙者・軽喫煙者の肺腺がん996例を調べ、従来の検査では明らかながん遺伝子 (KRAS, EGFR, ALK, RET, ROS1の遺伝子変異)が見つからない125症例(男性30症例、女性95症例)を対象に、次世代シークエンサー注3による全エクソーム解析注4・全トランスクリプトーム解析注5を行いました。その結果、解析した症例の約70%に従来の検査では同定できなかった標的となり得るがんの遺伝子変異を同定することができました(図1)。特に全く新たながん遺伝子として、NRG2融合遺伝子注6を発見しました。これまでに近縁のNRG1遺伝子については、その融合遺伝子が肺腺がんや膵がんなどで報告されており、がん細胞に異常な増殖シグナルを送り続けることにより、発がんに寄与することが知られていましたが、NRG2遺伝子については初めての発見になります(図1)。
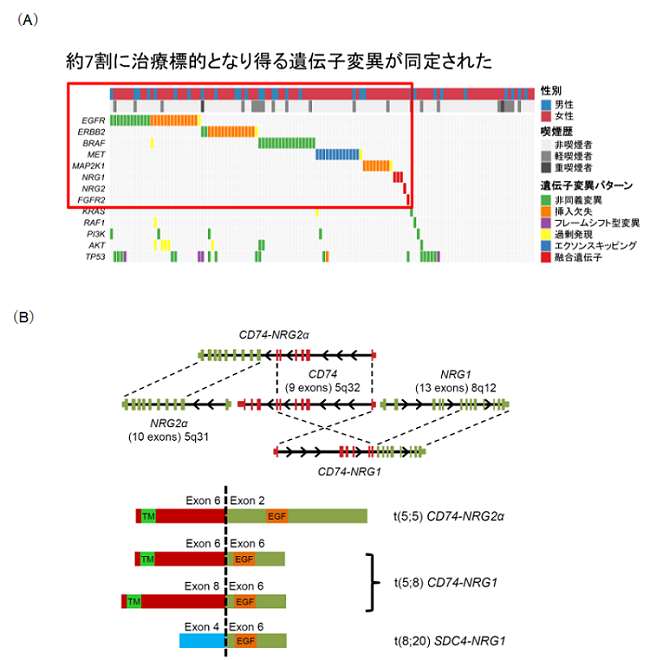
(B) 本研究で同定されたNRG融合遺伝子の転写産物の模式図。CD74遺伝子及びNRG2遺伝子はいずれも染色体5番長腕(5q)にコードされており、欠失等により融合遺伝子が形成されていると考えられます。NRG融合遺伝子はepidermal growth factor(EGF)ドメイン構造を有していることが特徴です。
全トランスクリプトーム解析においては術後再発のリスクを予測するマーカーを同定することができ、炎症反応に関連する遺伝子など3種類の遺伝子の発現量から算出したリスクスコアによって術後再発のリスクを層別化することが可能となりました(図2)。
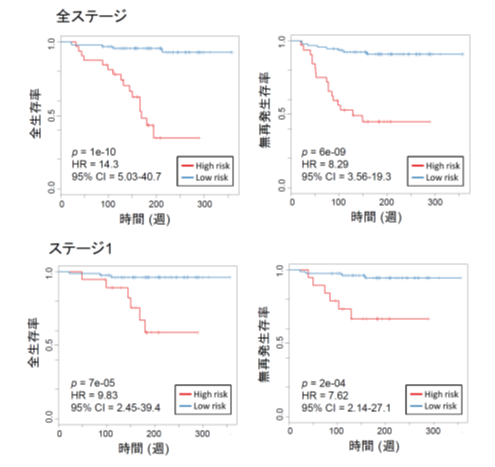
展望
本研究において、次世代シークエンサーを用いた網羅的なゲノム解析により、従来の検査法で同定できなかった標的となり得る分子を約7割の症例で同定できたことは、肺腺がんにおけるゲノム解析の有用性を示唆する結果でした。2019年6月からがん遺伝子パネル検査注7が保険診療開始されていますが、今後はより多くの患者に分子標的が同定され、最適な治療法の確立が促進されることが期待されます。
NRG1融合遺伝子の異常な増殖シグナルを抑える抗がん剤の開発が進んでおり、現在、国際臨床試験の開始が予定されています。NRG2融合遺伝子もNRG1と同様のメカニズムでがん化を誘導している可能性が高いため、NRG1融合遺伝子と同様に治療の標的となり得ることが期待されます。また、他のNRGファミリーメンバーであるNRG3, NRG4融合遺伝子の存在の可能性も、今回のNRG2融合遺伝子の発見により示唆されました。今後NRG融合遺伝子を有するがんに対する抗がん剤の効果が、臨床試験で証明されることが期待されます。
本研究で同定された術後予後の予測に関するマーカー遺伝子について、今後、がん遺伝子パネル検査等による検査が可能になれば、術後再発のリスクが高い患者に対する追加治療の有無(手術後に放射線治療や抗がん剤治療を追加するかどうかなど)の決定に有用になると考えられます。
発表論文
- 雑誌名:
- Journal of Thoracic Oncology
- タイトル:
- Identification of novel CD74-NRG2α fusion from comprehensive profiling of lung
- adenocarcinoma in Japanese never or light smokers
- 著者:
- Shinji Kohsaka, Takuo Hayashi, Masaaki Nagano, Toshihide Ueno, Shinya Kojima, Masahito Kawazu, Yuichi Shiraishi, Satsuki Kishikawa, Yoshiyuki Suehara, Fumiyuki Takahashi, Kazuhisa Takahashi, Kenji Suzuki, Kazuya Takamochi, and Hiroyuki Mano
- 国立がん研究センター
- 研究所 主任研究員 高阪 真路 (筆頭著者・責任著者)
- 研究所 研究員 上野 敏秀
- 研究所 外来研究員 小島 進也
- 研究所 任意研修生 長野 匡晃
- 研究所 ユニット長 河津 正人
- 研究所 ユニット長 白石 友一
- 研究所 分野長 間野 博行
- 順天堂大学 医学部
- 人体病理病態学講座 准教授 林 大久生
- 人体病理病態学講座 助手 岸川 さつき
- 呼吸器外科学講座 准教授 高持 一矢
- 呼吸器外科学講座 教授 鈴木 健司
- 整形外科学講座 准教授 末原 義之
- 呼吸器内科学講座 准教授 高橋 史行
- 呼吸器内科学講座 教授 髙橋 和久
研究費
本研究は下記事業の支援を受けて行われました。
- 日本医療研究開発機構 革新的がん医療実用化研究事業
- 日本医療研究開発機構 次世代がん医療創生研究事業(P-CREATE)
- 日本医療研究開発機構 臨床ゲノム情報統合データベース整備事業
- 日本医療研究開発機構 革新的先端研究開発支援事業インキュベートタイプ(LEAP)
用語解説
- 注1 ドライバー遺伝子
- がんの発生や増殖に直接かかわる遺伝子。
- 注2 分子標的治療薬
- がん細胞の増殖に関わるタンパク質や、栄養を運ぶ血管、がんを攻撃する免疫に関わるタンパク質などを標的にしてがんを攻撃する薬。
- 注3 次世代シークエンサー
- DNA全体の配列を、従来法と比べ桁違いに短時間で決定する技術。
- 注4 全エクソーム解析
- ヒトゲノムのうちタンパク質をコードするエクソン領域(エクソーム)を選択的に濃縮し、効率的に解析する手法。
- 注5 全トランスクリプトーム解析
- 細胞中に存在する全ての遺伝子転写産物(トランスクリプトーム)の配列・発現量を解析する手法。
- 注6 融合遺伝子
- がん細胞における染色体の転座、挿入、逆位などの組換えの結果、複数の遺伝子が連結されて生じる新たな遺伝子のこと。融合タンパク質がコードされ、細胞増殖のシグナルを活性化あるいは分化のシグナルを抑制する場合などは、がん化の原因となり得る。
- 注7 がん遺伝子パネル検査
- 高い精度で数百に及ぶがんの遺伝子を一括で調べることができる検査。
お問い合わせ先
研究に関する問い合わせ
国立研究開発法人国立がん研究センター
研究所 細胞情報学分野
高阪 真路(こうさか しんじ)
電話番号:03-3542-2511(代表)
Eメール:skohsaka"AT"ncc.go.jp
広報窓口
国立研究開発法人国立がん研究センター
企画戦略局 広報企画室
電話番号:03-3542-2511(代表) FAX:03-3542-2545
Eメール:ncc-admin"AT"ncc.go.jp
順天堂大学 総務局 総務部 文書・広報課
電話番号:03-5802-1006(直通) FAX:03-3814-9100
Eメール:pr"AT"juntendo.ac.jp
AMED事業に関するお問い合わせ先
国立研究開発法人日本医療研究開発機構(AMED)
戦略推進部 がん研究課
電話番号:03-6870-2221
Eメール:cancer"AT"amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
関連リンク
掲載日 令和2年2月26日
最終更新日 令和2年2月26日


