ダイレクトリプログラミング法を用いてヒト肝前駆細胞を作製することに成功―細胞移植による急性肝不全モデルマウスの救命効果を実証―
プレスリリース
九州大学
日本医療研究開発機構
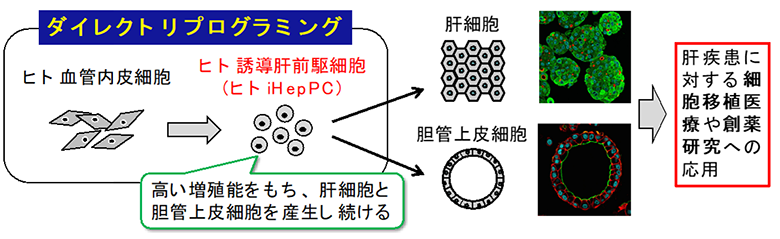
九州大学生体防御医学研究所の鈴木淳史教授らの研究グループは、同大学の大川恭行教授、須山幹太教授、前原喜彦教授(現九州中央病院)、小川佳宏教授、熊丸渉講師、京都大学の長﨑正朗教授、国立国際医療研究センターの植野和子研究員との共同研究により、ダイレクトリプログラミング※1の手法を用いてヒトの臍帯静脈や末梢血中の血管内皮細胞から高い増殖能と肝細胞・胆管上皮細胞への分化能を有する「誘導肝前駆細胞(iHepPC)」を作製することに成功しました。
鈴木教授らは、2011年にマウスの皮膚から抽出した線維芽細胞に2つの転写因子※2(Hnf4αとFoxa1、2、3のいずれか1つ)を導入することで、線維芽細胞を肝細胞の性質を有する「誘導肝細胞(iHepC)」へと変化させることに成功しました(Sekiya and Suzuki, Nature, 2011)。そこで次に、同様の手法を用いてヒトiHepCの作製を進めました。しかし、作製されたヒトiHepCは増殖能が低く、大量の細胞を必要とする細胞移植医療※3や創薬研究に応用することは難しいことが判明しました。この問題に対し、鈴木教授らは、増殖できない肝細胞ではなく、高い増殖能と分化能を有する肝前駆細胞をダイレクトリプログラミングの手法によって作り出せないかと考えました。この考えに基づき、本研究において転写因子の組み合わせを再検討した結果、最終的に3つの転写因子(FOXA3、HNF1A、HNF6)をヒトの臍帯静脈や末梢血由来の血管内皮細胞に導入することで、長期培養による安定的な増殖が可能なヒトiHepPCを作製することに成功しました。作製されたヒトiHepPCは、三次元培養下において肝・胆管組織様構造を形成し、それぞれ機能的な肝細胞と胆管上皮細胞へ分化・成熟する能力をもつことも判明しました。また、ヒトiHepPCから分化した肝細胞を致死率の高い急性肝不全※4モデルマウス(生存率2割)の肝臓へ移植したところ、マウス肝臓内でヒト肝実質組織を再構築して機能し、高い救命効果(生存率8割)を発揮することも判明しました。本研究によって開発された方法を用いることで、機能的に成熟した肝細胞や胆管上皮細胞をヒトiHepPCから大量に調達することが可能になると考えられます。将来、肝臓から採取される肝細胞や胆管上皮細胞の代わりにヒトiHepPC由来の肝細胞・胆管上皮細胞を用いることで、重篤な肝疾患患者に対する新しい移植医療の実現や、個人レベルで薬剤の効果や毒性を評価できるシステムの構築が期待されます。
本研究成果は、2020年10月21日(水)午後6時(日本時間)に英国科学雑誌『Nature Communications』に掲載される予定です。
用語の解説
- ※1 ダイレクトリプログラミング
- ある細胞Aの運命を決める遺伝子を別の細胞Bに発現させることで、細胞Bの分化状態を強制的に変更して細胞Aの性質を有する細胞へ変化させること。
- ※2 転写因子
- DNAに結合して遺伝子の発現を調節するタンパク質であり、標的遺伝子に応じて多様な種類、組み合わせがある。
- ※3 細胞移植医療
- 臓器を移植する代わりに細胞を移植することで、機能の低下した臓器の再生・機能回復を促す治療法を指す。ドナー臓器不足や拒絶反応の問題を解消する方法として、治療技術の確立が望まれている。
- ※4 急性肝不全
- 大量の肝細胞が急激に死滅することで肝臓の機能が著しく低下する疾病であり、劇症肝炎とも呼ばれる。本邦の患者数は年間400人ほどと推定されており、生体部分肝移植などの適切な治療を行わない場合は高頻度に死に至る難治性の疾病である。
論文情報
- 雑誌名
- Nature Communications, 2020
- 論文名
- Direct reprogramming of human umbilical vein- and peripheral blood-derived endothelial cells into hepatic progenitor cells
- 著者名
- *Inada H., *Udono M., Matsuda-Ito K., Horisawa K., Ohkawa Y., Miura S., Goya T., Yamamoto J., Nagasaki M., Ueno K., Saitou D., Suyama M., Maehara Y., Kumamaru W., Ogawa Y., Sekiya S., Suzuki A. (* Co-first author)
研究助成金情報
本研究は、日本医療研究開発機構(AMED)「再生医療実現拠点ネットワークプログラム(幹細胞・再生医学イノベーション創出プログラム)」(2019年度~2021年度)、同「革新的先端研究開発支援事業(AMED-CREST)(エピゲノム研究に基づく診断・治療へ向けた新技術の創出)」(2011年度~2016年度)、同「肝炎等克服実用化研究事業」(2015年度~2017年度)、日本学術振興会「科学研究費助成事業(JP16H01850、JP16K08592、JP18H05102、JP18K18369、JP19H01177、JP19H05267、JP20K12624、JP20H05040)」、九州大学生体防御医学研究所共同利用・共同研究拠点「多階層生体防御システム研究拠点」などの支援を受けました。
お問い合わせ先
研究内容に関すること
鈴木淳史(すずきあつし)
九州大学 生体防御医学研究所 器官発生再生学分野 教授
TEL:092-642-6449 FAX:092-642-6444
E-mail:suzukicks“AT”bioreg.kyushu-u.ac.jp
報道に関すること
九州大学 広報室
E-mail:koho“AT”jimu.kyushu-u.ac.jp
AMED事業に関すること
国立研究開発法人日本医療研究開発機構
再生・細胞医療・遺伝子治療事業部
再生医療研究開発課
TEL:03-6870-2220
E-mail:saisei“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
掲載日 令和2年10月21日
最終更新日 令和2年10月21日


