膵がんの血液バイオマーカー(アポリポプロテインA2 アイソフォームズ)が、公的医療保険で臨床使用可能になりました
プレスリリース
日本医科大学
国立がん研究センター
日本医療研究開発機構(AMED)
成果の概要
日本における膵がんの罹患者数は約44,000人(2019年)、死亡者数は年間約39,000人(2022年)に上ります。また、膵がんは早期に発見できれば生存率の向上が期待されますが、自覚症状が現れにくく進行が早いため、早期に発見することが難しいがんの一つです。
本研究は、➀膵がん前がん病変であるIPMNやリスク疾患である慢性膵炎・膵嚢胞、膵がん間接所見である主膵管拡張、膵脂肪浸潤などを診断する血液バイオマーカーの開発、②早期膵がんの発見の契機を増やし、膵がんの予後改善に貢献するべく、膵がんリスク疾患を診断する血液バイオマーカーの体外診断用医薬品の開発、ならびにその実用化を目標に進められてきました。
その成果として、膵がん患者の血液中での2種類のAPOA2アイソフォーム(APOA2-ATおよびAPOA2-ATQ)の量比が変化することに基づき、APOA2アイソフォームを測定する試薬の体外診断用医薬品としての開発を進め、臨床性能試験により膵がんの検出における有用性が確認されたため、2023年6月8日に膵がんの診断補助としての薬事承認を経て、このたび保険収載が決定し国内販売が開始され、公的医療保険での検査が可能になりました。
本邦で製造販売承認された本品による検査方法は、血液を用いるため、より多くの方々が受診しやすい検査です。既存の腫瘍マーカー 「CA19-9」とは異なる物質を測定することから、本品と「CA19-9」とは相補的な腫瘍マーカーとして機能し、適正使用指針に基づいて使用することで膵がんの早期診断に資すること、また既存の腫瘍マーカーでは検出できなかった膵がん患者を検出できることが期待されます。
本成果は、AMEDの「次世代がん医療加速化研究事業」と「革新的がん医療実用化研究事業」の事業間連携のもと、研究成果を臨床現場に届けるため研究支援をしたことが、大きな成果につながった好事例となります。
日本医科大学(学長:弦間 昭彦)、国立がん研究センター(理事長:中釜 斉)、東レ株式会社(社長:大矢 光雄)等が、産学共同研究で臨床開発をいたしました。
東レ(株)が上記成果を活用し、厚生労働省から「膵がんの診断を補助する体外診断用医薬品」の承認を取得し、国内販売が開始されました。
研究の内容
Apolipoprotein A2-isoforms(ApoA2-i)の説明とその臨床性能
1)はじめに
日本医科大学大学院医学研究科本田一文大学院教授らは、膵がんや膵がんリスク疾患、健常者の血液中を循環するタンパク質の質量分析プロファイルからapolipoprotein A2 2量体タンパク質のC末端アミノ酸が欠失したアイソフォーム(apolipoprotein A2-isoforms; apoA2-i)の量比が変化することを発見しました。特に、apoA2-iのうちC末端アミノ酸配列がATQ/AT型となるapoA2-ATQ/AT(アポA2中間鎖)が、膵がんや膵がん前がん病変であるIPMN患者では、健常者の血漿濃度に比べて有意に低下することを発見していました(図1)。
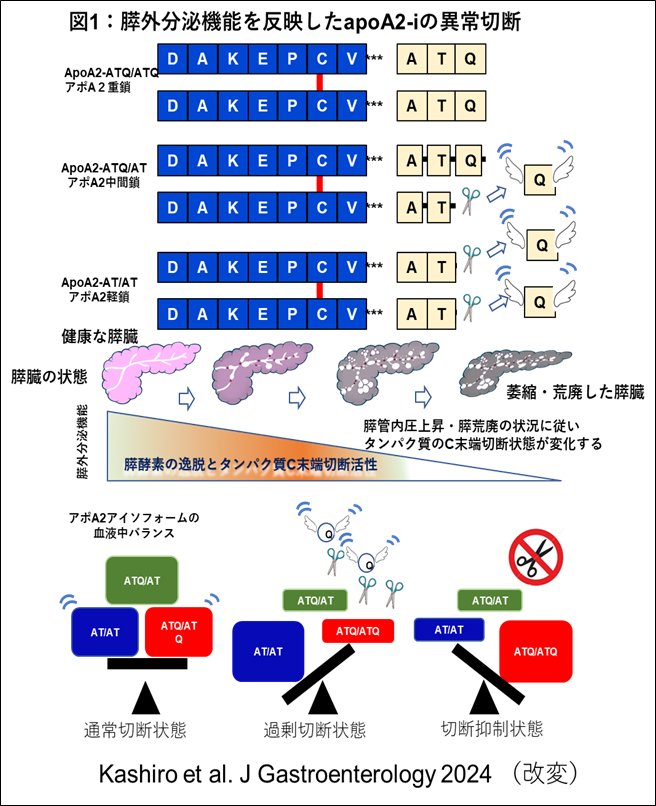
ApoA2-ATQ/ATQ型(アポA2重鎖)とapoA2-AT/AT(アポA2軽鎖)に反応する抗体を作製し、apoA2-ATQ/AT濃度(apoA2-I Index)を推定するELISA検査系(APOA2アイソフォーム)をAMEDの支援を受けて、日本医大、国立がん研究センター、東レ(株)との共同研究で確立しました(図2)。同APOA2アイソフォーム検査キットを用いて、体外診断用医薬品承認申請に必要な臨床性能試験を実施しました。
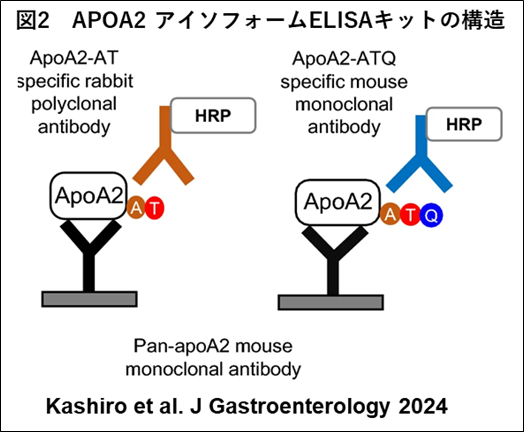
2)APOA2アイソフォームELISAキットの膵がんと健常者を判別する性能(国内試験)
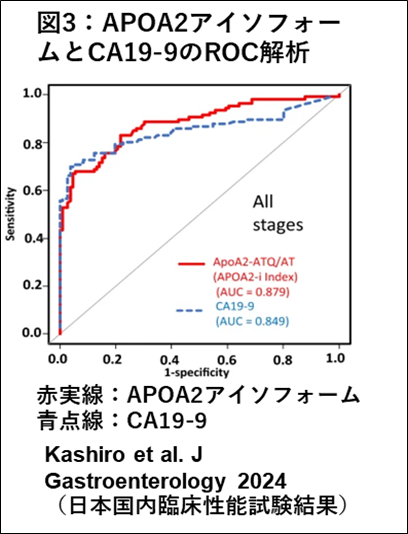
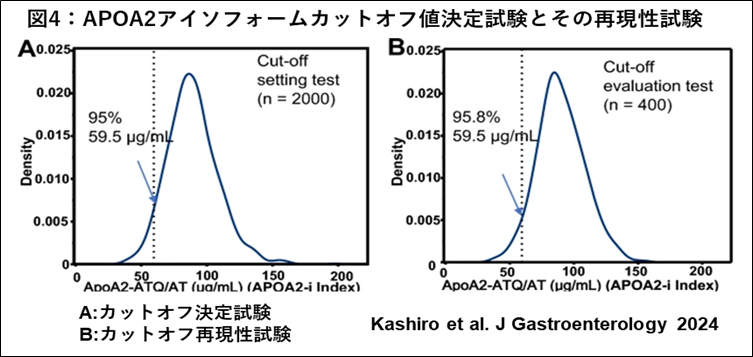
ROC解析による膵がん患者を健常者集団から判別するROC曲線下面積値(AUC)の点推定値は、APOA2アイソフォームが0.879と臨床で膵がん診断に利用されるCA19-9のAUC点推定値の0.849より高く、膵がんの既存腫瘍マーカーである「CA19-9」と同等以上の臨床性能が確認できました(図3)(日本国内臨床性能試験結果)。2000名の健常者血漿検体を用いて、その95%が陰性となる測定値を閾値(カットオフ値)としたときのAPOA2アイソフォームの血漿濃度は59.5μg/mLとなり、カットオフ値の決定には利用しなかった400名で、カットオフ値の再現性を確認しても、健常者の95.8%の集団が正確に判定されました(図4)。
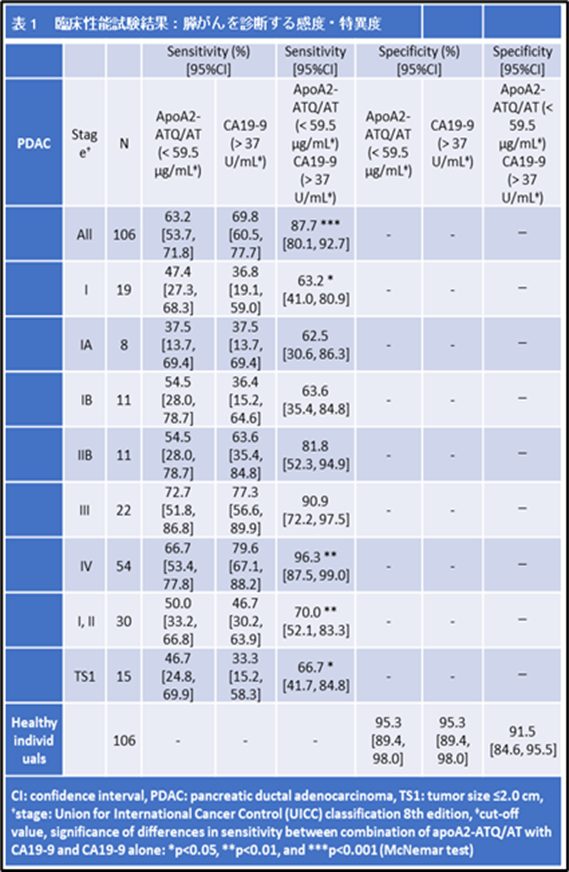
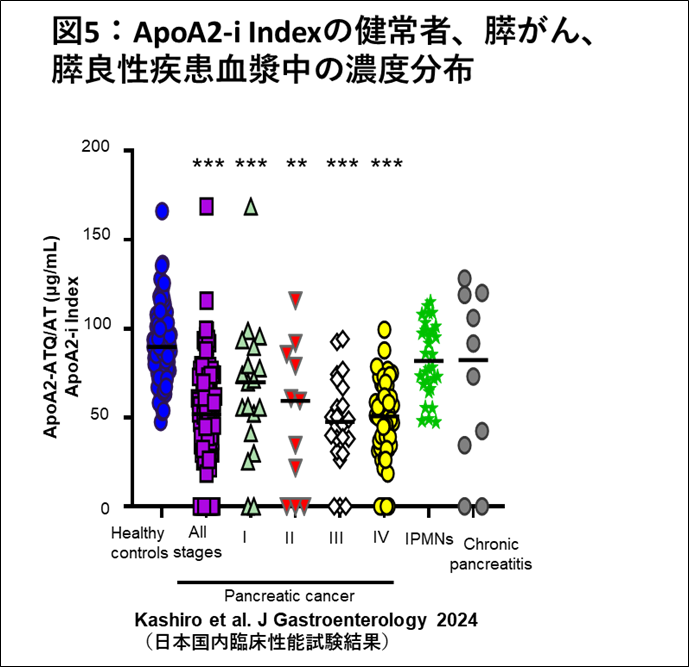
膵がんを発見するAPOA2アイソフォーム(カットオフ値 59.5μg/mL)とCA19-9(カットオフ値 37U/mL)の感度・特異度は、それぞれ表1の通りとなり、特にI期(n=19)におけるAPOA2アイソフォームとCA19-9の感度は、それぞれ47.4%、36.8%となりました。2㎝以下膵がん(TS1)(n=15)を発見する感度は、CA19-9単独では33.3%であったが、APOA2アイソフォームを加えるとその感度が66.7%に上昇しました。APOA2-iTQとCA19-9単独測定の特異度はいずれも95.3%でありました。ApoA2-i Indexは膵がんのいずれのステージでも健常者に比較して血漿濃度が減少しました(図5)。
3)米国国立がん研究所早期診断研究ネットワーク(NCI EDRN)による臨床病期I/II膵がんに対する臨床性能の検証研究
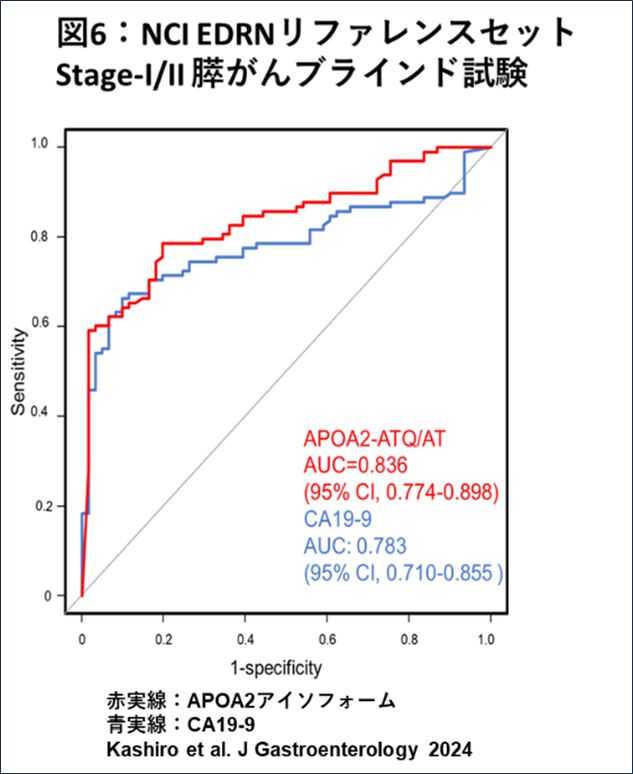
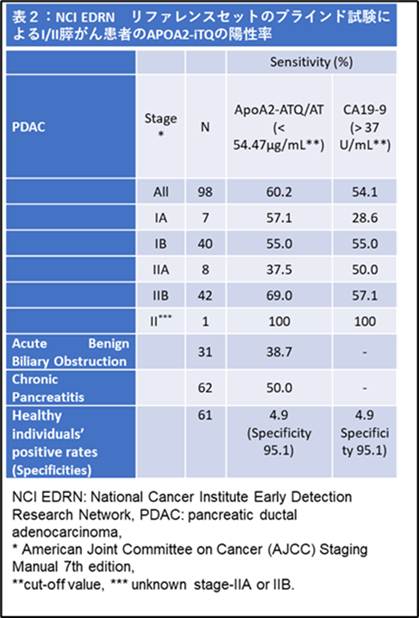
米国国立がん研究所早期診断研究ネットワーク(National Cancer Institute Early Detection Research Network: NCI EDRN) では、開発されたバイオマーカーの臨床性能を確認するための盲検試験を行い、そのバイオマーカーの性能評価を行います。NCIからI/II期などの切除手術可能期(ステージI/II)の膵がん血漿検体を入手し、米国の測定施設でAPOA2アイソフォームのブラインド測定を実施しました。I/II期膵がん(n=98)を健常者から判別するAUCは、APOA2アイソフォーム、CA19-9、それぞれ0.836、0.783となり、その点推定値は日本で実施された臨床性能試験結果と同様に、APOA2アイソフォームがCA19-9に比較して高く、再現性が確認されました。米国人健常者リファレンスサンプルの95%点をAPOA2アイソフォームのカットオフ値と定義し(54.47μg/mL)、膵がん患者の感度と特異度を確認したところ、表2のようになりました。
4)まとめ
最近、腫瘍細胞から微量に漏出するタンパク質、核酸、細胞小胞、代謝物、糖鎖などを総合的に分析して多種類のがん早期診断を可能にするリキッドバイオプシー(multi cancer early detection:MCED)が注目を集めています。一方で膵がんの診断を補助するバイオマーカーとして、臨床的に利用されている体外診断用医薬品は1970年代に臨床開発されたCA19-9をはじめとしたがん細胞が産出する糖鎖バイオマーカーだけです。今回の研究成果により、40年ぶりにCA19-9と同等以上の性能を持つ腫瘍マーカーが体外診断用医薬品として認可され、実際の臨床現場で健康保険により利用できるようになりました。既存の膵がん腫瘍マーカーであるCA19-9とは全く原理が異なるため、組み合わせることで、膵がんの診断に貢献できると考えられます。日本国内からこのようなバイオマーカーが探索から臨床開発され、世界に先駆けて体外診断用医薬品として社会実装されたことは大変喜ばしいことです。
5)今後の展望
このバイオマーカーの特徴は、先に説明した通り、腫瘍細胞が産出する特殊な物質ではなく、腫瘍発生母地になる膵臓の機能的変化をいち早くとらえて、早期膵がん患者やリスク患者を囲い込める可能性があることです。膵がんは、非常に予後不良な疾患ですが、わが国では10万人に34人程度しか罹患者がいない悪性腫瘍でもあります。米国疾病予防タスクフォース(The U.S. Preventive Services Task Force)は、このような頻度の低い膵がんには画像検査を用いたがん検診を推奨しておりません。血液検査という非侵襲的な方法を用いて早期膵がん患者や膵がん発症リスクを持つ集団を囲いこめれば、効率的な膵がん検診法を提案できるかもしれません。日本だけでなく海外研究機関とも連携しながら、さらなる研究を進めたいと思います。
発表論文
Kashiro A, Kobayashi M, Oh T, Miyamoto M, Atsumi J, Nagashima K, Takeuchi K, Nara S, Hijioka S, Morizane C, Kikuchi S, Kato S, Kato K, Ochiai H, Obata D, Shizume Y, Konishi H, Nomura Y, Matsuyama K, Xie C, Wong C, Huang Y, Jung G, Srivastava S, Kutsumi H, Honda K. Clinical development of a blood biomarker using apolipoprotein-A2 isoforms for early detection of pancreatic cancer.
J Gastroenterology. 2024. https://doi.org/10.1007/s00535-023-02072-w
先行研究
- (国立がん研究センター プレスリリース平成27年11月9日)検査キットの開発にも成功、膵がん検診への実用化を目指す膵がん早期診断の血液バイオマーカーを発見
- (AMEDプレスリリース 平成27年11月9日)検査キットの開発にも成功、膵がん検診への実用化を目指す膵がん早期診断の血液バイオマーカーを発見
膵がんの早期診断バイオマーカーの探索と診断薬としての実用化研究
- 次世代がん医療創生研究事業
「タンパク質・ペプチド修飾解析による早期がん・リスク疾患診断のための血液バイオマーカーの開発」 - 革新的がん医療実用化研究事業
「膵外分泌機能を評価する血液バイオマーカーを用いた膵がんリスク疾患・早期膵がんの診断法の臨床開発」
研究代表機関名:日本医科大学(国立がん研究センター)
研究代表者:本田一文大学院教授
問い合わせ先
研究に関すること
日本医科大学 先端医学研究所 事務室
電話番号:03-3822-2131(代表)
Eメール:sentankenjimushitsu.group”AT”nms.ac.jp
国立がん研究センター 企画戦略局 広報企画室
電話番号:03-3542-2511(代表)
Eメール:ncc-admin”AT”ncc.go.jp
AMED 事業に関すること
日本医療研究開発機構(AMED)
次世代がん医療加速化研究事業 E メール:jisedaigan”AT”amed.go.jp
革新的がん医療実用化研究事業 E メール:kakushingan”AT”amed.go.jp
※Eメールは上記アドレス“AT”の部分を@に変えてください。
関連リンク
掲載日 令和6年4月12日
最終更新日 令和6年4月12日


