iPS細胞を用いたパーキンソン病に対する細胞移植治療の医師主導治験がスタート
 世界初、iPS細胞を用いたパーキンソン病患者への再生医療
世界初、iPS細胞を用いたパーキンソン病患者への再生医療
京都大学の髙橋淳教授を中心とする研究グループは、iPS細胞から誘導したドパミン神経前駆細胞を直接脳内に移植することによって、パーキンソン病の症状を改善させる治療法を開発し、その安全性と有効性を検討するための医師主導治験を開始しました。これはiPS細胞を用いた世界初の治験となり、2018年10月に第1例目の手術が行われ、計7例をそれぞれ2年間の予定で観察します。
取り組み
パーキンソン病とは、ドパミンを産生・分泌する神経細胞(ドパミン神経細胞)が進行性に減少し、手足の震えやこわばりなどの運動機能障害が起こる神経難病です。病気の初期には薬剤の治療効果が見られますが、病気の進行とともにその効果は減弱し症状改善が難しくなります。これは、薬剤が脳内のドパミン神経細胞に作用していることを示しています。そこで研究グループは、iPS細胞からドパミン神経細胞を作りこれらを脳内に移植することで脳内のドパミン量を増やし症状を改善させる方法を開発してきました。
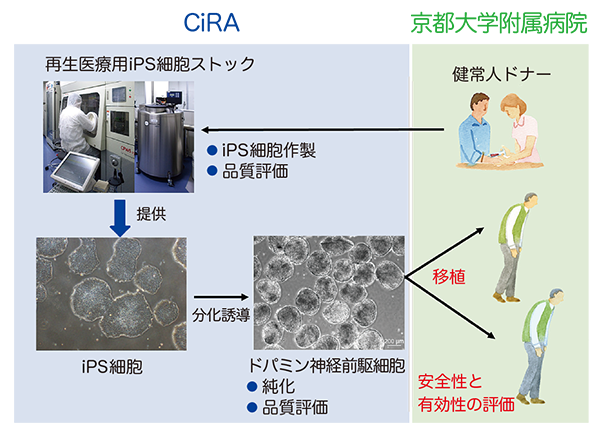
iPS細胞を利用する利点の一つは自家移植(自分の細胞を自分に移植する)ができることですが、現時点では多くの費用と時間がかかるために現実的ではありません。そこで今回の治験では、京都大学iPS細胞研究所(CiRA)で樹立された、健常人由来の細胞を用いて他家移植(他人の細胞を移植する)を行います。一度に多くの細胞を準備することができるので、一人当たりのコストと手間を大幅に削減できますが、免疫を抑制する必要があります。
成果
研究グループはこれまでにヒトES細胞やヒトiPS細胞を用いて、①ドパミン神経細胞が分化誘導できること、②誘導したドパミン神経細胞がパーキンソン病モデル動物の脳に生着して行動改善を来し得ること、③誘導したドパミン神経細胞を高度に濃縮できることを明らかにしてきました。本製法では、移植後に増殖する可能性のある細胞は濃縮過程で除去されるため、高い安全性と有効性が期待できます。
本製法で作製したドパミン神経前駆細胞を治験と同様のプロトコールでカニクイザルのパーキンソン病モデルに移植し2年間観察したところ、行動解析では症状の改善が確認され、脳の画像解析や組織学的解析ではドパミン神経細胞の生着と安全性が確認されました。
研究グループはこれらの結果に基づき、実際の臨床で用いるiPS細胞株を用いて安全性と有効性を検討する非臨床試験を行いました。がん関連遺伝子に異常がないことや免疫不全マウスへの移植で腫瘍形成が認められないことなど多くの結果が得られ、患者に移植する細胞の安全性と有効性を確認しました。
展望
治験の対象はパーキンソン病の患者、その中でも薬物治療による症状のコントロールが難しくなった症例です。ただし、細胞移植の目的はあくまでもドパミンの補充であり、ドパミンに対する反応が失われ重症化した患者は対象になりません。
治験は京都大学医学部附属病院で行われます(図1)。対象患者は7名であり、それぞれ移植後に定期的な行動評価と画像評価を行い、2年間にわたり経過観察します。安全性の評価が主目的であり、有害事象、特に移植片増大の有無について評価します。有効性については、世界的な症状評価の指標であるMDS-UPDRSやオン・オフ時間(身体を動かせる時間、動かない時間)などを評価します。
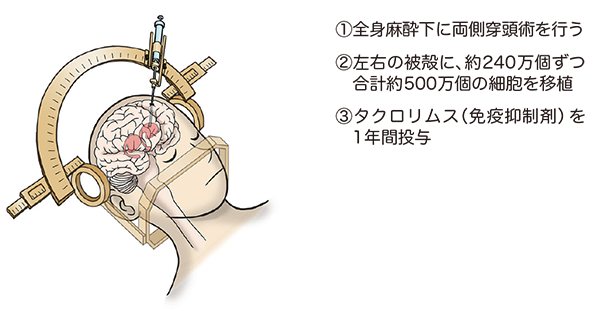
手術は定位脳手術の手法を用い、頭蓋骨に小さな穴を開け、そこから細い針を通してドパミン神経前駆細胞を正確に移植します(図2)。
この治験で細胞移植の安全性が確認され、かつ有効性を示唆する結果が得られれば、さらに多くの症例を重ねて、標準治療となることを目指します。パーキンソン病で寝たきりになる患者をゼロにすることが目標です。
関連リンク
最終更新日 令和2年6月23日


