iPS創薬で難聴治療薬を治験へ―Pendred症候群の難聴・めまいに対するシロリムス少量療法―
プレスリリース
慶應義塾大学医学部
慶應義塾大学病院
国立研究開発法人 日本医療研究開発機構
慶應義塾大学医学部耳鼻咽喉科学教室の小川郁教授、藤岡正人専任講師らは、生理学教室(岡野栄之教授)との共同研究で行ったiPS細胞を用いた研究の知見をもとに、Pendred症候群(注1)の難聴・めまいに対する低用量シロリムス療法の医師主導治験を行います。
Pendred症候群は進行性の難聴やめまい、甲状腺腫を引き起こす遺伝性の病気で、確立した治療法のない希少難治性疾患のひとつです。この症状を正確に再現できる遺伝子改変マウスは作成できないため、研究グループは非臨床試験において患者さん由来のiPS細胞を用いて、生体外で疾患病態を再現することによって創薬研究を行ってきました。そして、今回初めて、疾患動物モデルを用いることなくiPS創薬(注2)から得られた知見にもとづいた治験を行うことを予定しています。
治療薬は市販の既存薬の中からスクリーニングし、他疾患で安全性の確立したものを選んでいます。体内での内耳への作用は正常動物を用いて確認し、低用量での治療効果はiPS細胞モデルを用いて調べました。この創薬アプローチは、疾患を再現する動物モデルが確立していない他の疾患にも応用できる可能性があり、将来的な難病治療法の開発に役に立つものと期待されます。
今回の治験では患者さんに検査機器やタブレット端末を貸出し、難聴やめまいなどの症状や体調の変化を患者さんの自宅で毎日モニターします。検査結果を自宅からリモートアクセスで治験データセンターへ送ることで、膨大な治験データを管理・分析することができます。
iPS細胞技術とIoT(Internet of Things)を臨床現場に活かし、安全性を担保しながら効率のよい創薬を進めることで、今後も治療法のない難治性疾患の患者さんに一刻も早く新しい治療薬を届けることを目指します。
これまでの研究の背景と概要
老人性難聴や突発性難聴、メニエール病など、難聴の多くは内耳に原因があることが知られており、WHOによると65才以上の人口の30~40%が難聴によりハンディキャップを有しているといわれています。また、先天性疾患の中で難聴はもっとも罹患率が高く(新生児1000人に1人)、その約半数は遺伝子に変異が見つかる遺伝性難聴です(注3)。Pendred症候群は日本の遺伝性難聴の中で2番目に患者数の多い病気で、SLC26A4遺伝子の変異が原因として知られています。本疾患は進行性の難聴を引き起こしますが、遺伝子欠損マウスは重い奇形のために先天性の重度難聴をきたし、またヒト型遺伝子変異マウスは難聴になりません。このように動物モデルでは患者さんのような進行性難聴にならないため、本疾患の難聴メカニズムをうまく説明できず、治療薬の開発は難しい と考えられていました。
そこで研究グループでは、iPS技術を用いて患者さんの内耳細胞をつくり、難聴ではない健常者の内耳細胞と比較して、患者さんの細胞がより死にやすいこと(細胞脆弱性)を明らかにしました。さらに、細胞ストレスに対する細胞脆弱性を改善する薬剤として、免疫抑制やリンパ管脈管筋腫症という難病に用いられているシロリムス(注4)が、通常、用いる量のわずか1/10でこの脆弱性を改善できることを発見しました(Hosoya et al, Cell Report,2017 参考論文)。この結果から、Pendred症候群の患者さんに対してシロリムスを少量投与すること(シロリムス少量療法)で、内耳細胞の脆弱性が改善し、細胞死抑制により病勢の進行を遅らせられることで難聴・めまい発作が減弱する可能性が推定されました。
研究計画の概要
今回、Pendred症候群の患者さんを対象に、シロリムス製剤(ラパリムス®)を低用量で投与することの安全性の確認と、難聴・めまい発作(内耳障害の急性増悪症状)に対する有効性、および有効性評価法の探索を行う医師主導治験を行います。シロリムス製剤は臓器移植に対する免疫拒絶予防やリンパ脈管筋腫症に対して、長期投与での十分な忍容性と安全性をもって効果を発現することが確認されています。本治験ではさらに濃度を下げ、Pendred症候群の患者さんでの安全性を確認しながら、その治療効果についても詳細に検討していきます。
治験の内容
本治験では、遺伝子検査でPendred症候群/DFNB4(注5)の診断が確定した、難聴やめまい発作のある患者さんにラパリムス®錠かプラセボ(注6)のどちらかを少ない量で内服していただき、安全性を確認しながら、治療効果を追跡します。また、投薬期間中は、どちらを服用しているかは患者さんにも担当医にも知らされません。
投薬の治療効果は来院時の検査に加え、自宅でも患者さんに検査機器やタブレット端末を貸し出し、難聴やめまいの変化を毎日モニターすることで、症状や体調の日々の変化を調べます。体のゆれや平衡をモニターする眼鏡型重心動揺測定装置、聴力を測るポータブルオージオメータ、眼球の振動を診るワイヤレスフレンツェル眼鏡を用いて自宅で計測し、タブレット端末を介して治験データセンターへと送ります(図1)。Pendred症候群の症状は、体調の変化や日々の生活状態で変動すると言われています。このような日々の検査で膨大な量の検査データを収集し、シロリムス少量療法の効果を詳細に検討していきます。
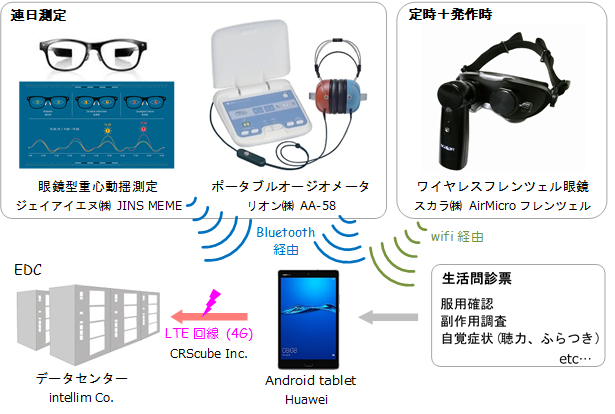
【図1】IoTを活用した治験データ登録システム
研究の意義
本疾患のような希少疾患に対する治療薬の開発では、医学的な発見と、患者さんへ治療薬を届ける製薬企業の間をつなぐ過程が重要になります。今回、研究グループでは、慶應義塾大学病院臨床研究推進センターの支援の下、AMED橋渡し研究加速ネットワークプログラムの協力を得て、シロリムスという候補薬(シーズ)をもとに臨床研究への基盤体制を整えました。その結果、iPS細胞研究から得られた知見をもとに、シロリムス少量療法のPendred症候群患者さんに対する安全性を確認しながら、治療効果を検討することとなりました。
疾患モデル動物が確立されていない場合、新しく発見した候補薬がその安全性と、どの程度の効果をもたらすかは予想困難です。iPS創薬研究によって、他の疾患に対してすでに30年以上使われているシロリムスという薬剤が、Pendred症候群の患者さん由来iPS細胞から作成した内耳細胞の細胞脆弱性を低減するだけではなく、低用量でも効果をもたらすことを見出しました。さらに、この低用量投与でもシロリムスが内耳細胞に届いて作用することを、正常動物で確認しています。この結果をもとに、独立行政法人医薬品医療機器総合機構(PMDA)からの助言を得て、臨床試験において、安全性を確認しながら、実際の臨床試験で効果を調査していきます。
特記事項
本研究は、JSPS科研費 JP24592560, JP15H04991, JP15K15624, JP26・5202、国立研究開発法人日本医療研究開発機構(AMED)の「再生医療実用化研究事業」、「再生医療実現拠点ネットワークプログラム」、「難治性疾患実用化研究事業」、「橋渡し研究加速ネットワークプログラム」、「橋渡し研究戦略的推進プログラム」、公益財団法人武田科学振興財団からの支援を受けて行われました。今後は、革新的医療技術創出拠点プロジェクト・橋渡し研究戦略的推進プログラム(慶應義塾大学拠点)シーズC(臨床でのPOC取得を目指す課題)の支援を受けて、治験に向けた準備を進めています。
参考論文
- タイトル:
- Cochlear cell modeling using disease-specific iPSCs unveils a degenerative phenotype and suggests treatments for congenital progressive hearing loss
- タイトル和訳:
- 疾患特異的iPS細胞を用いた蝸牛細胞モデルが明らかにした蝸牛変性疾患と先天性進行性難聴に対する治療法
- 著者:
- 細谷 誠、藤岡 正人、曽根 岳史、岡本 理志、赤松 和土、鵜飼 英樹、上田 泰巳、小川 郁、松永 達雄、岡野 栄之
- 掲載誌:
- Cell Reports 18, 1–14, January 3, 2017
用語解説
- (注1)Pendred症候群:
- 難聴・めまい・甲状腺腫を特徴とする常染色体劣性遺伝疾患で、1896年にPendred博士が初めて報告しました。聴力変動幅が大きく、発作のたびに周囲との音声コミュニケーションができなくなることがあります。
またPendred症候群のめまい症状は、数時間~数日続く回転性めまい発作を伴い、強い発作のときは寝たきりの生活を余儀なくされ、生活の質を極めて低下させます。 - (注2)iPS創薬:
- iPS細胞から目的の細胞を大量に分化誘導し、体外で多種類の薬剤を投与することによってそれぞれの薬剤の効果や毒性を検討する方法です。これまでに難しかったヒト由来の細胞を大量に用いて体外で検討することができ、薬剤開発の効率が上がることが考えられています。また、今回のように、マウスモデルが確立されていない疾患でも患者さん由来のヒト細胞を用い検討することができるため、新たな研究手法として注目されています。
- (注3)遺伝性難聴:
- 難聴のうち、遺伝子の変化が原因によって生じる難聴。
- (注4)シロリムス:
- 免疫抑制剤の一種で、国内でも使用されている薬剤です。ラパマイシンと呼ぶこともあります。
- (注5)DFNB4:
- Pendred症候群に似ているが甲状腺腫がなく、遺伝子検査ではSLC26A4に病的変異を認めるものがDFNB4に相当します。年齢が上がると甲状腺が腫れてくることも予想されています。
- (注6)プラセボ(偽薬):
- 患者さんによっては、「薬を使っている」という事実による心理的な効果(プラセボ効果)でも治療効果が出てしまうことがあります。そこで新しい薬の効果を調べるときには、本物の薬(実薬)と外見的に区別のつかない偽薬(プラセボ)を服用する患者さんも設けて、実薬との効果を比較することが必要になります。このような科学的な試験を行うことではじめて、本当に効果のある薬を世の中に送り出すことができるのです。
お問い合わせ先
本発表資料のお問い合わせ先
慶應義塾大学医学部耳鼻咽喉科学教室
専任講師 藤岡 正人(ふじおか まさと)
助教 細谷 誠(ほそや まこと)
TEL:03-5363-3827 FAX:03-3353-1261
E-mail:masato“AT”2002.jukuin.keio.ac.jp mhosoya“AT”keio.jp
URL:http://www.hosp.keio.ac.jp/annai/shinryo/otorhino/
AMED事業に関するお問い合わせ先
国立研究開発法人 日本医療研究開発機構
(AMED)戦略推進部 再生医療研究課
〒100-0004 東京都千代田区大手町一丁目7番1号
TEL:03-6870-2220 FAX:03-6870-2242
E-mail:saisei“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
掲載日 平成30年4月24日
最終更新日 平成30年4月24日


