生命活動の燃料「ATP」を観察する3色の蛍光センサーの開発に成功―がんや肥満の創薬開発への貢献に期待 日本、シンガポール、アメリカの国際共同研究―
プレスリリース
早稲田大学
東京工業大学
東京大学
日本医療研究開発機構
早稲田大学理工学術院の新井敏(あらいさとし)研究院講師と東京工業大学 科学技術創成研究院の北口哲也(きたぐちてつや)准教授(論文投稿当時、早稲田大学重点領域研究機構研究院准教授)らの研究チームは、東京大学大学院総合文化研究科、シンガポール国立大学、ハーバード大学と共同で、細胞の中のエネルギー代謝で中心的な役割を果たしているアデノシン三リン酸(ATP)を検出する、赤・緑・青(RGB)色の蛍光ATPセンサーの開発に成功しました。
地球上のあらゆる生物は、栄養素の分解を通して獲得したエネルギーを、ATPの形に変換・保存し、必要に応じて、ATPからエネルギーを取り出すことで、生命体を構成する細胞の中の様々な化学反応を滞りなく進行させたり、必要な場所に必要な物質を輸送するシステムを動かしたりしています。このATPの細胞内の分布を理解するためには、細胞内のATP濃度の変化の情報を蛍光シグナル(蛍光の明るさの強弱)に変換する蛍光ATPセンサーを細胞の中に導入し、蛍光顕微鏡を用いて生きた細胞を観察する蛍光イメージング技術が最も有力な手法の1つです。
本研究チームは、標的とするATPに特異的に結合するタンパク質(ATP合成酵素の一部)と、蛍光を発する色素を含む蛍光タンパク質をペプチドリンカー(※1)で繋ぎ、その長さやリンカーを構成するアミノ酸の種類を独自の手法で最適化することで、青・緑・赤色の蛍光ATPセンサー(MaLionB, G, R)を開発しました。今回開発した蛍光ATPセンサーを自在に組み合わせることで、従来の技術では原理的に極めて困難であった「同じ細胞内の異なる場所のATPの動態の同時観察」や、「ATP以外の他のシグナルやタンパク質の動態との同時観察」などが可能になりました。
今回の開発した一連の蛍光ATPセンサーは、汎用性の高い研究ツールとして、創薬・医療技術開発にATPに関わるシグナル伝達経路のビジュアルエビデンスという新しい視点を加え、開発研究を加速度的に進めることが期待されます。本研究は、文部科学省科学研究費補助金、及び、日本医療研究開発機構(AMED)革新的先端研究開発支援事業(PRIME)「メカノバイオロジー機構の解明による革新的医療機器及び医療技術の創出」研究開発領域における研究開発課題「人工オルガネラ熱源の作成細胞機能の温熱制御」(研究開発代表者:新井敏)の研究費によって行われました。研究成果は、ドイツ化学会誌『Angewandte Chemie International Edition』オンライン版に2018年6月27日に掲載され、近日中に紙面掲載される予定です。
ポイント
- 細胞の中のエネルギー代謝の中心であるATPをセンシングする、赤・緑・青(RGB)色の蛍光ATPセンサーの開発に成功
- 従来の技術では困難であった、同一細胞内の異なる場所のATP動態の同時観察が可能に
- 海外にある日本のラボ・早稲田バイオサイエンスシンガポール研究所(WABIOS)を中心とした、日本、シンガポール、アメリカの国際共同研究
(1)これまでの研究で分かっていたこと
地球上のあらゆる生物は、糖、脂質、アミノ酸などの栄養素の分解を通して獲得したエネルギーを、アデノシン三リン酸(ATP)の形に変換し、保存します。そして必要に応じて、ATPからエネルギーを取り出すことで、生命体を構成する細胞の中の様々な化学反応を滞りなく進行させたり、必要な場所に必要な物質を輸送するシステムを動かしたりしています。ATPは、言わば、生命活動の燃料であり、細胞の機能や恒常性を維持する上で極めて重要な分子であると言えます。
このため、生物学研究の幅広い領域において、細胞の中で、どのようにATPが分布しているのか、そして時間に伴ってどう変化していくのかを検出することは大きな課題の1つです。こうした課題を解決するために用いられるのが、蛍光イメージングの技術です。細胞の中で起きる現象の変化を、蛍光シグナル(主に、蛍光の明るさの強弱)に変換する極小の蛍光センサーで細胞内の注目分子の動態を蛍光顕微鏡で観察する手法です。現在までに、幾つかの蛍光ATPセンサーが報告されています(ATeam; Imamura et al., PNAS, 2009. B-Queen; Yaginuma et al., Sci. Rep., 2014)。しかしながら、従来の蛍光センサーでは、使用できる色に制限があるため、同じ細胞の中の異なる場所(細胞小器官など)のATPの動態を同時に解析することやATP以外の他のシグナル分子やタンパク質の動態を同時に観察することは原理的に困難でした。
(2)今回の研究で新たに開発した手法
本研究チームは、ATPの濃度変化に応答して、蛍光強度が変化する単色型の蛍光タンパク質を用いた新しい蛍光ATPセンサーを開発しました。今回の蛍光ATPセンサーは、標的とするATPに特異的に結合するタンパク質(ATP合成酵素の一部のεサブユニット)と、蛍光を発する色素を含む蛍光タンパク質がペプチドリンカーを介して繋がった構造をしています(図1左参照)。ATP濃度に応答して蛍光強度が大きく変わる蛍光ATPセンサーを得るには、このペプチドリンカーの長さや、構成するアミノ酸の種類が大きな鍵なります。最終的に、このリンカーを独自の手法で最適化し、青色(BFP)、緑色(Citrine)、赤色(mApple)のTurn-on型(※2)の蛍光ATPセンサーを開発、それぞれ、MaLionB, G, R(Monitoring aTP Level intensity based turn on indicators)と名づけました。MaLionB、MaLionG、MaLionRは、それぞれ、蛍光強度が90%、390%、350%増加します。また、センサーの作動するATPの濃度域も、0.1~8ミリモル濃度で、生理的条件のATP濃度域と一致しています。更に、この蛍光ATPセンサーは、細胞の中の狙った細胞小器官などに、自由自在に配置できることも特徴です。
(3)今回の研究で得られた結果及び知見
今回開発した一連の蛍光ATPセンサー(MaLions)によって、今までの技術では極めて困難であったことが可能になりましたので、その事例を2つ紹介します。
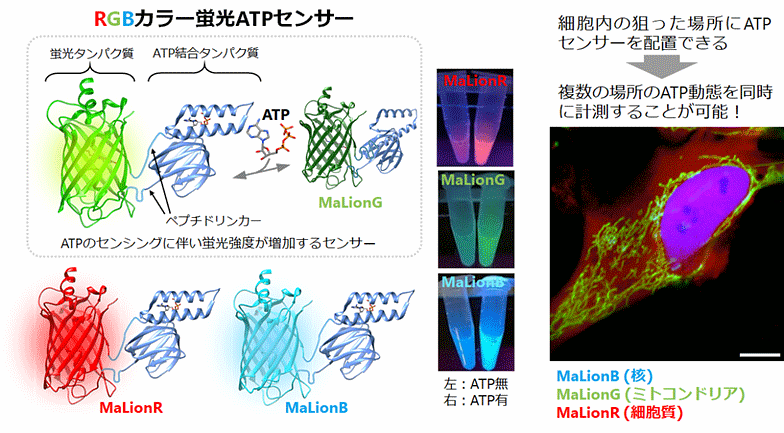
図1 ATPの濃度変化によって蛍光強度が変わるRGBカラーの蛍光ATPセンサー
[A] 同じ細胞の中の異なる場所のATPの動態を同時に観察する試み
通常、動物細胞の場合、ATPは、細胞質における解糖系と、ミトコンドリアでの酸化的リン酸化の両方の経路から合成されています。更に、分化した細胞は、ミトコンドリアでのATP産生系が主要経路であるのに対し、がん細胞をはじめとした増殖性の細胞では、解糖系が発達しているといった違いが知られています(ワーブルグ効果(※3))。がん細胞(HeLa細胞)と正常な細胞(褐色脂肪細胞)に、緑色の蛍光ATPセンサー(MaLionG)と赤色のセンサー(MaLionR)を、それぞれ、細胞質とミトコンドリアに導入し、顕微鏡観察しました。観察の途中に、ミトコンドリアのATP産生をオリゴマイシンで阻害したところ、HeLa細胞(※4)では、ミトコンドリアのATP濃度減少と同時に、細胞質のATP濃度上昇が観察されました。この現象は、活発な解糖系を持つがん細胞が、ミトコンドリアのATP産生の阻害による細胞全体でのATP濃度の低下に応答し、細胞質のATP濃度の一過的な上昇により補おうとしていると考察しています。一方、ミトコンドリアのATP産生が優位な細胞の例として、例えば褐色脂肪細胞では、細胞質のATP濃度上昇は見られませんでした。これらの結果は、がん細胞と正常な細胞の違いを、同一細胞内のATP動態という視点から検出した初めての例と言えます。また、上記の他に、光合成によって生じる植物(シロイヌナズナ)のATP産生の増加や(シンガポール国立大学との共同研究)、麻酔に伴って減少するATPの様子を線虫で捉えることにも成功しており(東京大学大学院総合文化研究科との共同研究)、開発したセンサーが、動物・植物の極めて広い範囲の生物種に適用できる可能性を示しました。
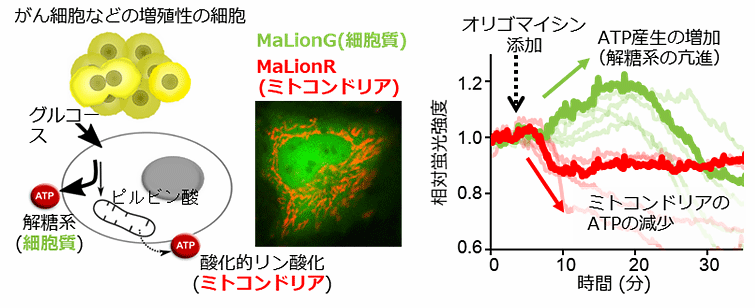
図2 がん細胞のダイナミックなATPの濃度変化を捉えた成功例
[B] ATPとそれ以外のシグナルの動態を同時に観察する試み
褐色脂肪細胞は、私達の体の中で、恒常性を保つために熱産生を行う重要な細胞の1つです。私達は褐色脂肪細胞をその前駆細胞より分化させ(シンガポール国立大学、ハーバード大学との共同研究)、細胞質に青色の蛍光カルシウムセンサー(B-GECO)と緑色の蛍光cAMPセンサー(Flamindo2)、そしてミトコンドリアに赤色の蛍光ATPセンサー(MaLionR)を導入しました。顕微鏡観察中に、βアドレナリン受容体をイソプロテノール(※5)で刺激したところ、cAMPが上昇(Flamindo2の蛍光強度が減少。Flamindo2はTurn-off型)、続いて、ミトコンドリアのATPが緩やかに減少、更に、反応の後半、カルシウムイオンの濃度が上昇する様子が見られました。褐色脂肪細胞は、受容体の刺激によって活性化された細胞膜上のアデニル酸シクラーゼ(AC)がcAMPを合成し、これがシグナル伝達となって、cAMP依存性のPKAを活性化します。その後、脂肪酸を遊離、ミトコンドリア膜上の脱共役タンパク質UCP1と作用して、ミトコンドリア膜上の膜電位の元となるプロトン濃度勾配を解消させATP合成を阻害し、最後に、ミトコンドリアからカルシウムイオンが流れ出てくることが知られています(褐色脂肪の熱産生)。生物学の教科書に記載されているこのような細胞内のシグナル伝達の模式図は、「時間」が止まっています。しかし、実際には、細胞の中は、時々刻々と様々な因子がダイナミックに変化しています。今回、R,G,Bというカラフルなセンサーを開発したことで、模式図として描かれているシグナル伝達の一部を本来の姿として見ることができるようになりました。
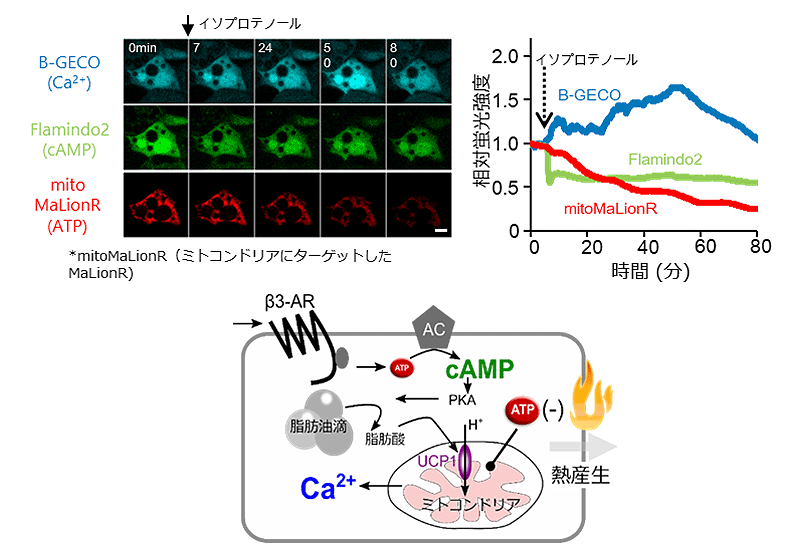
図3 褐色脂肪細胞の熱産生に関わるシグナル伝達系の可視化
(4)研究の波及効果と意義
今回、開発した一連の蛍光ATPセンサーは、エネルギー代謝系の変化について知りたいというニーズに対して、直感的に分かりやすいビジュアルのエビデンスを提供します。特に、薬剤の効果を迅速に解析することが要求される、がんや肥満などの生活習慣病のための創薬開発において威力を発揮します。また、力や熱などの物理的な刺激に伴う細胞の応答を知ることも、医療機器開発の分野においては重要です。従って、本研究成果は、創薬・医療機器開発の様々な分野の研究開発を加速させるものと期待されます。
本研究の実施においては、世界の研究ハブであるシンガポール・バイオポリスにある早稲田バイオサイエンスシンガポール研究所(WABIOS)が最大限に活用されました。現地のシンガポール国立大学(Raghunath博士やIto博士ら)から研究試料をスムーズに受け取り、迅速にWABIOSにて実験を遂行しつつ、日常的に議論できたことが、本研究を完遂するのに非常に重要でした。最終的に本共同研究は、東京大学大学院総合文化研究科、ハーバード大学へと広がり、世界中の研究者を巻き込んだ国際共著論文として達成されています。また、WABIOSは、効率良く国際的な共同研究を実施できる場所であることに加え、現地の大学・研究機関等から独立した研究所であるため、発生した知財に関しては、日本側の研究者が単独でその権利を主張できることも特徴です。こうした特殊性を活かし、蛍光ATPセンサー材料の関連で出願した特許は、本学が主導で、その知財を保護しながら、研究を進めることができました。こうした海外の研究拠点は本学の大きな強みであり、今後一層、新たな研究成果を発信していく独自のプラットフォームとして期待されます。
(5)今後の課題
本研究成果では、がん細胞の一部と褐色脂肪細胞に焦点が当てられているため、今後は、様々な細胞種のATP産生経路の特徴を体系的に理解していく必要があります。このため、今まで以上に、産学を問わず、多岐に渡る専門分野の研究者との共同研究が必須です。特に、複数の種類のがん細胞の特徴をATP産生系の視点から網羅的に理解することで、創薬研究に大きなインパクトを与えるものと期待しています。
(6)100字程度の概要
細胞の中のエネルギー代謝の中心であるATPをセンシングする、赤・緑・青(RGB)色の蛍光ATPセンサーの開発に成功。細胞内のATPのダイナミックな姿を高精度、且つ、簡便に捉える強力なツールとして期待できます。
(7)用語解説
- ※1 ペプチドリンカー:
- 本研究では数個~数十個のアミノ酸が連結した分子(ペプチド)が、2つの異なるタンパク質を繋げる役割(リンカー)を担っています。構成するアミノ酸の種類によって、ペプチドリンカーの柔軟性や剛直性が変わりますが、このバランスを最適化することが蛍光センサーの開発の重要な点の1つです。
- ※2 Turn-on型:
- 対象とする分子を検出して、蛍光強度を変化させる蛍光センサーの場合、蛍光強度が増加するタイプのセンサーを“Turn-on”型、逆に、減少するタイプを”Turn-off“型と呼びます。
- ※3 ワーブルグ効果:
- 細胞内でATPが合成される経路として、解糖系と酸化的リン酸化の2つが知られています。解糖系は細胞質で行われ、グルコース1分子からATPを2分子合成するのに対し、酸化的リン酸化はミトコンドリアで行われ、ATP36分子を合成します。したがって、ATP産生の効率の点では、解糖系よりも酸化的リン酸化の方が圧倒的に優れています。正常な細胞は、酸化的リン酸化に依存してATP産生を行っているのに対して、がん細胞は、効率の悪い解糖系に依存していることが古くから知られており、ワーブルグ効果と呼ばれています。
- ※4 HeLa細胞:
- ヒト子宮頸癌由来の細胞。さまざまな細胞生物学的研究で用いられるモデル細胞であり、蛍光センサーの開発研究においては、生細胞で作動するかを検討する目的で用いられます。
- ※5 イソプロテノール:
- アドレナリンβ受容体を選択的に刺激する分子であり、Gs経路を活性化することでcAMPを産生させます。
論文情報
- 掲載誌:
- Angewandte Chemie International Edition
- 論文名:
- RGB-color intensiometric indicators to visualize spatiotemporal dynamics of ATP in single cells
- 著者:
- Satoshi Arai(新井敏), Rókus Kriszt, Kazuki Harada(原田一貴), Liang-Sheng Looi, Shogo Matsuda(松田翔吾), Devina Wongso, Satoshi Suo(周防諭), Shoichi Ishiura(石浦章一), Yu-Hua Tseng, Michael Raghunath, Toshiro Ito(伊藤寿朗), Takashi Tsuboi(坪井貴司), Tetsuya Kitaguchi(北口哲也)
- 著者所属:
- 早稲田大学(当時WABIOS)、AMED、東京大学大学院総合文化研究科、シンガポール国立大学、ハーバード大学医学部
- 掲載URL:
- https://doi.org/10.1002/anie.201804304
お問い合わせ先
内容に関するお問い合わせ先
東京工業大学 科学技術創成研究院 化学生命科学研究所 北口 哲也 准教授
Tel:045-924-5270 E-mail:kitaguct-gfp"AT"umin.ac.jp
早稲田大学理工学術院 新井 敏 次席研究員(研究院講師)
Tel:+65-9026-2546 E-mail:satoshiarai"AT"aoni.waseda.jp
報道に関するお問い合わせ先
早稲田大学広報室広報課
Tel:03-3202-5454 E-mail:koho"AT"list.waseda.jp
東京工業大学 広報・社会連携本部 広報・地域連携部門
Tel:03-5734-2975 E-mail:media"AT"jim.titech.ac.jp
東京大学教養学部等総務課広報・情報企画係
Tel:03-5454-6560 E-mail:koho-jyoho"AT"adm.c.u-tokyo.ac.jp
AMED事業に関すること
国立研究開発法人日本医療研究開発機構(AMED)
基盤研究事業部 研究企画課
TEL:03-6870-2224 FAX:03-6870-2246 E-mail:kenkyuk-ask"AT"amed.go.jp
※E-mailは上記アドレス”AT”の部分を@に変えてください。
掲載日 平成30年7月24日
最終更新日 平成30年7月24日


