軟骨遺伝子疾患の原因遺伝子であるSox9の発現システムの解明―先天性骨軟骨形成異常症の病態解明へ向けた発見―
プレスリリース
国立大学法人 東京医科歯科大学
学校法人 日本医科大学
国立研究開発法人 産業技術総合研究所
国立研究開発法人 日本医療研究開発機構
ポイント
- SOX9は、性分化や軟骨細胞の分化に必須の役割を持つ転写因子であり、そのSOX9遺伝子もしくはそのエンハンサーの突然変異により、先天性骨軟骨形成異常症(キャンポメリックディスプラシア)が引き起こされることがわかっていました。
- 今回研究チームは、CRISPR/Cas9を用いたゲノム編集技術を複数の研究手法(クロマチン免疫沈降(ChIP)と次世代シークエンサーおよび質量分析、エピジェネティックスな編集制御、エンハンサーのノックアウトマウスの作成・解析)と組み合わせることによって、マウスの肋軟骨部位に特異的なエンハンサー(Rib Cage Specific Enhancer: RCSE)がSox9遺伝子から遠く離れた1Mb付近に存在し、これが転写因子Stat3によって制御されることをつきとめました。
- この発見は、キャンポメリックディスプラシアやアキャンポメリックディスプラシアといった先天性骨軟骨形成異常症の病態解明へとつながる可能性があります。
東京医科歯科大学大学院医歯学総合研究科システム発生再生医学分野の淺原弘嗣教授と日本医科大学医学部整形外科学大学院生ならびに東京医科歯科大学大学院医歯学総合研究科システム発生再生医学分野特別研究学生の望月祐輔大学院生は、日本医科大学医学部整形外科学、慶應義塾大学医学部整形外科学、産業技術総合研究所創薬分子プロファイリング研究センターらのグループとの共同研究で、Sox9遺伝子から遠く離れた1Mb付近に存在するエンハンサーとそこに結合するStat3という転写因子が、肋軟骨におけるSox9遺伝子の作動を制御する発現システムであることを見出しました。この研究成果は、先天性骨形成異常症キャンポメリックディスプラシアの原因の解明に寄与する可能性があります。この研究は、文部科学省科学研究費補助金(基盤研究)ならびに日本医療研究開発機構(AMED)革新的先端研究開発支援事業(AMED-CREST)「メカノバイオロジー機構の解明による革新的医療機器及び医療技術の創出」研究開発領域における研究開発課題「腱・靱帯をモデルとした細胞内・外メカノシグナルの解明とその応用によるバイオ靱帯の創出」(研究開発代表者:淺原弘嗣)、の支援のもとでおこなわれたもので、その研究成果は、国際科学誌Developmental Cell (デベロップメンタル・セル)に、2018年8月23日午前11時(米国東部時間)にオンライン版で発表されます。
研究の背景
軟骨細胞の分化や発生に必須の役割を持つ転写因子としてSOX9 (SRY-box9) が挙げられます。このSOX9遺伝子もしくはその周辺の突然変異により骨軟骨の異形成と性分化異常を主徴とする、重篤な先天性骨形成異常症 (キャンポメリックディスプラシア, アキャンポメリックディスプラシア)を引き起こすことが知られておりましたが、SOX9の遺伝子のスイッチ部分(エンハンサー)は、非常に長い距離(約2Mb)のどこかに存在するといった特殊なものであるため、現在まで解明されていませんでした。
研究成果の概要
近年、遺伝子改変を可能とするCRISPR(clustered regularly interspaced short palindromic repeats)/Cas systemを用いて、 エンハンサーの同定やエピジェネティックス制御の戦略が報告がされています。我々はこれらシステムを組み合わせることで、未だ明らかでないSox9の軟骨特異的なエンハンサーの同定を試みました。まず、Sox9の近傍に設計したCRISPR/Cas systemをレトロウイルスによりマウスの初代肋軟骨細胞に対し導入後、クロマチン免疫沈降とシークエンス(ChIP-seq)によってSox9から約1Mb離れたところに軟骨エンハンサー(RCSE)の候補を見出しました(図1)。
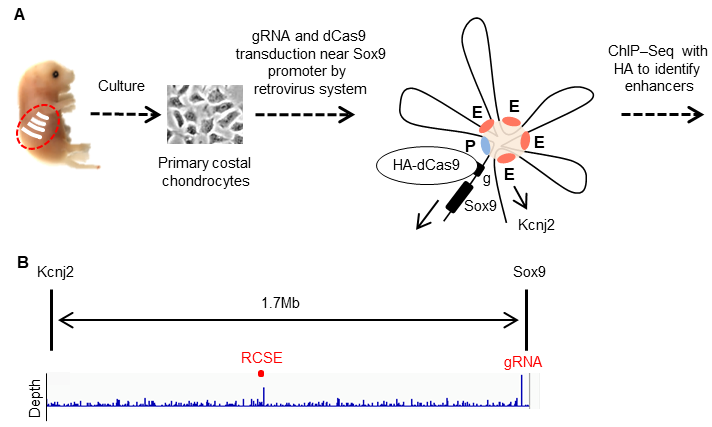
図1 Sox9上流1Mb付近に存在する肋軟骨特異的エンハンサー(RCSE)を同定するまでの模式図
肋軟骨細胞において、この軟骨エンハンサーの候補領域に遺伝子の作動をストップする機能のあるエピジェネティックシステムを誘導すると、Sox9の遺伝子の作動が弱まることが確認されたため、遺伝子スイッチとして機能することが示唆されました。
また、このRCSEが作動する部位で青く染まるLacZ-トランスジェニックマウスを作成したところ、肋骨の軟骨に青い染色が見られたため、RCSEは肋軟骨においてのみSox9を作動させるスイッチであることがわかりました(図2)。
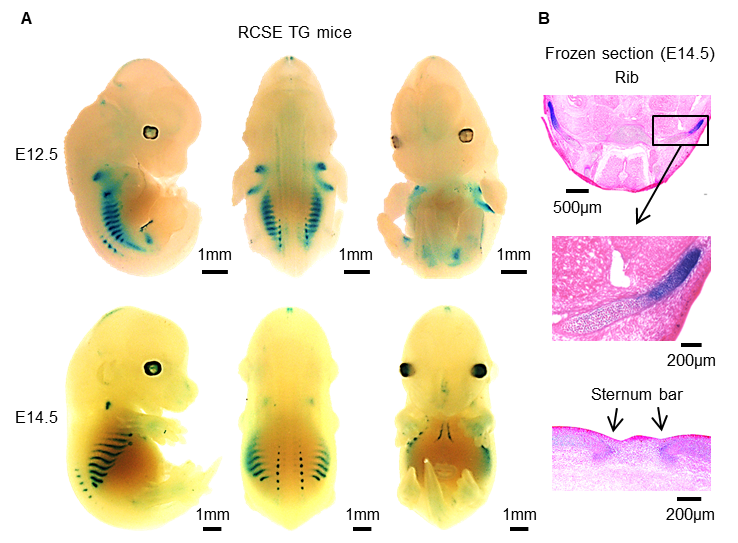
図2 RCSE領域をSox9プロモーターにつなぎLacZ配列を含んだベクターを用いたトランスジェニックマウスの作成
さらに、この軟骨スイッチRCSEをCRISPR/Cas9を用いて欠失させたノックアウトマウスを解析したところ、肋軟骨を含んだ胸郭のみの低形成・狭小化を認めました(図3)。また切片では肋軟骨のみで増殖軟骨細胞層の狭小化、および肥大軟骨細胞層の増大を認めました。これによって、このスイッチが肋軟骨におけるSox9遺伝子の作動に必要不可欠であることが証明されました。
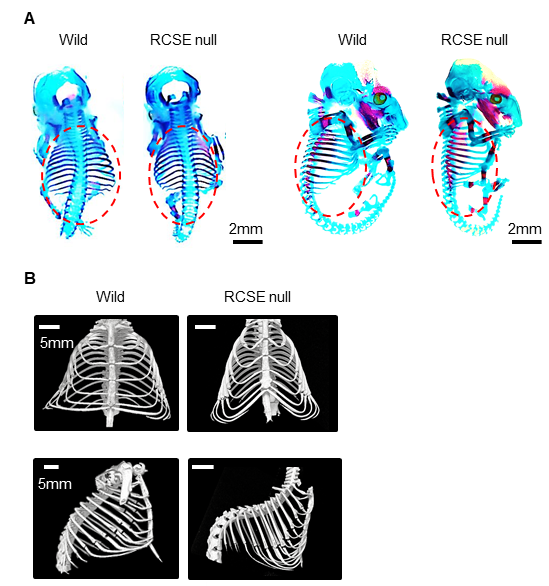
図3 RCSE領域を欠失させたノックアウトマウスの作成
最後に、このRCSEに結合するタンパクを質量分析装置をもちいて解析したところ、Sox9のスイッチを押す転写因子としてStat3(Signal transducer and activator of transcription 3)が同定されました。このStat3遺伝子を欠損させると、Sox9が作動しなくなり、軟骨発生が抑制されました。
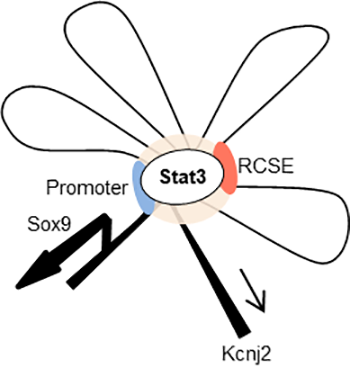
図4 転写因子Stat3が肋軟骨特異的エンハンサーであるRCSE領域を介してSox9の発現を制御している模式図
研究成果の意義
現在、ゲノムの機能を解析するための様々な手法が開発されていますが、それぞれ一長一短があり、まだまだ、未解明の先天性疾患や難病が多く残されています。
本研究では、最近までに報告されてきた複数のCRISPR/Cas9を用いた研究手法を組み合わせることによって、初めて肋軟骨におけるSox9遺伝子のスイッチ機構を明らかにすることができました。これらの結果は、先天性骨軟骨形成異常症(キャンポメリックディスプラシア)の疾患メカニズムの解明につながるものであり、本研究で用いられた手法は他の疾患の研究にも生かされることが期待されます。
論文情報
- 掲載誌:
- Developmental Cell
- 論文タイトル:
- Combinatorial CRISPR/Cas9 approach to elucidate a far-upstream enhancer complex for tissue-specific Sox9 expression
研究者プロフィール
- 淺原 弘嗣
- 東京医科歯科大学 システム発生再生医学分野 教授
- 研究領域
- 分子生物学(遺伝子発現)、発生・再生医学、整形外科学、リウマチ学
- 望月 祐輔
- 日本医科大学大学院 医学研究科整形外科学分野 大学院生
東京医科歯科大学大学院 医歯学総合研究科システム発生再生医学分野 特別研究学生 - 研究領域
- 発生・再生医学、整形外科学
問い合わせ先
研究に関すること
東京医科歯科大学大学院医歯学総合研究科
システム発生再生医学分野 氏名 淺原 弘嗣(アサハラ ヒロシ)
TEL:03-5803-5015 FAX:03-5803-5810
E-mail:asahara.syst"AT"tmd.ac.jp
報道に関すること
国立大学法人東京医科歯科大学 総務部総務秘書課広報係
〒113-8510 東京都文京区湯島1-5-45
TEL:03-5803-5833 FAX:03-5803-0272
E-mail:kouhou.adm"AT"tmd.ac.jp
学校法人日本医科大学 総務部広報課
〒113-8602 東京都文京区千駄木1-1−5
TEL:03-5814-6242 FAX:03-3824-2822
E-mail:kouhouka"AT"nms.ac.jp
国立研究開発法人産業技術総合研究所 企画本部報道室
〒305-8560 茨城県つくば市梅園1-1-1 中央第1
TEL:029-862-6216 FAX:029-862-6212
E-mail:press-ml"AT"aist.go.jp
AMED事業に関すること
国立研究開発法人日本医療研究開発機構(AMED)
基盤研究事業部 研究企画課
〒100-0002 東京都千代田区大手町1-7-1 読売新聞ビル
TEL:03-6870-2224 FAX:03-6870-2246
E-mail:kenkyuk-ask"AT"amed.go.jp
※上記の"AT"は@に置き換えてください。
掲載日 平成30年8月24日
最終更新日 平成30年8月24日


