動物体内で胚盤胞補完法によるマウス多能性幹細胞由来の血管内皮と血液細胞の作製に成功
プレスリリース
東京大学
日本医療研究開発機構
発表者
山口 智之(東京大学医科学研究所 幹細胞治療部門 特任准教授)
濱仲 早苗(東京大学医科学研究所 幹細胞治療部門 特任研究員)
発表のポイント
- 血管内皮・血液細胞が欠損したマウスは発生初期の胎生期に死亡するが、胚盤胞補完法(注1)を利用してこのマウスの受精卵にマウス多能性幹細胞(注2)を注入して作製したキメラ(注3)マウスでは、腫瘍形成などの異常もなく成体まで発育した。
- この胚盤胞補完法を利用して作製したキメラマウス体内で、マウス多能性幹細胞由来の血管内皮と血液細胞の作製に成功した。
- 本研究成果は、胚盤胞補完法を利用することによる拒絶反応を起こしにくい移植用臓器の作製法として、臓器再生および再生臓器の移植治療に大きく貢献するものと期待される。
発表概要
東京大学医科学研究所の中内啓光特任教授、山口智之特任准教授、濱仲早苗特任研究員らの研究グループは、多能性幹細胞のキメラ形成能を利用した「胚盤胞補完法」により、血管内皮・血液細胞欠損マウス体内にマウスESおよびiPS細胞(ドナー細胞)由来の血管内皮と血液細胞を作製することに成功した。通常は血管内皮・血液細胞が欠損したマウスは発生初期の胎生期に死亡するが、胚盤胞補完法を用いてこのマウス受精卵にマウスES細胞またはiPS細胞を注入して作製したキメラマウスでは、血管内皮・血液細胞がES細胞またはiPS細胞由来に置き換えられることにより、腫瘍形成などの異常もなく正常に成体まで発育した。
これまで本研究グループは動物体内で多能性幹細胞由来の臓器作製に取り組んできたが、今回の成果を組み合わせることで、目的の臓器だけでなく臓器内の血管内皮と血液細胞も同時に多能性幹細胞から作製可能であることが予想される。本研究成果は、動物体内での拒絶反応を起こしにくい移植用臓器の作製法として再生医療に大きく貢献するものと期待される。
本研究は、国立研究開発法人日本医療研究開発機構(AMED)の革新的先端研究開発支援事業インキュベートタイプ(LEAP)における研究開発課題「発生原理に基づく機能的立体臓器再生技術の開発」(研究開発代表者:中内啓光)の一環として行われた。なお、本研究成果に関わる基盤的な知見は国立研究開発法人科学技術振興機構(JST)の戦略的創造研究推進事業総括実施型研究(ERATO)「中内幹細胞制御プロジェクト」(研究総括:中内啓光、平成24年度終了)から得られたものである。
本研究成果は 2018年9月20日付の科学雑誌「Stem Cell Reports」のオンライン版に掲載される。
発表内容
東京大学医科学研究所の中内啓光特任教授らの研究グループは、これまでに多能性幹細胞のキメラ形成能を利用した「胚盤胞補完法」で膵臓欠損マウス/ラットの体内に異種であるラットあるいはマウス多能性幹細胞由来の膵臓を作製することに成功し、胚盤胞補完法を利用して動物体内に作製した臓器に含まれる血管や神経などの支持組織はキメラ状態(異種動物の細胞が混在している状態)であることを確認している。
臓器を移植する場合、ドナーである移植臓器内に存在するMHC不適合(注4)の血管内皮細胞は拒絶反応の標的となる。また、移植するドナー臓器に残存する血液細胞がレシピエント(注5)の臓器を攻撃(GVHD)(注6)することがある。そのため、拒絶反応そしてGVHDを起こしにくい移植臓器の作製には、臓器のみならず臓器内の血管内皮細胞および血液細胞も同時に多能性幹細胞から作製する必要がある。
本研究では、多能性幹細胞由来の血管内皮細胞および血液細胞を作製するために、血管内皮・血液細胞欠損(Flk-1遺伝子(注7)欠損)マウス受精卵を用いて胚盤胞補完を行った(図1)。
その結果、血管内皮・血液細胞が欠損したマウスは発生初期の胎生期に死亡するが、胚盤胞補完法を用いてこのマウス受精卵に多能性幹細胞を注入して作製したキメラマウスでは、腫瘍形成などの異常もなく成体まで発育し、マウス多能性幹細胞由来の血管内皮および血液細胞を作製することに成功した(図2)。
本研究グループは、異種動物体内にヒトの臓器を作製し移植治療に用いることを目指しているが、今回の成果と組み合わせることで、臓器のみならず臓器内の血管内皮および血液細胞も同時に多能性幹細胞から作製することにより、胚盤胞補完法による拒絶反応を起こしにくい移植用臓器の作製法として臓器再生および再生臓器の移植治療に大きく貢献するものと期待される。
発表雑誌
- 雑誌名:
- Stem Cell Reports 9月20日付(日本時間9月21日)オンライン版
- 論文タイトル:
- Generation of vascular endothelial cells and hematopoietic cells by blastocyst complementation
- 著者:
- Sanae Hamanaka, Ayumi Umino, Hideyuki Sato, Tomonari Hayama, Ayaka Yanagida, Naoaki Mizuno, Toshihiro Kobayashi, Mariko Kasai, Fabian Patrik Suchy, Satoshi Yamazaki, Hideki Masaki, Tomoyuki Yamaguchi, and Hiromitsu Nakauchi
- DOI番号:
- 10.1016/j.stemcr.2018.08.015
- URL:
- https://doi.org/10.1016/j.stemcr.2018.08.015
用語解説
- (注1)胚盤胞補完法:
- 遺伝的に臓器が欠損する動物の受精卵(胚盤胞)に正常な多能性幹細胞を注入しキメラ動物を形成することで、欠損していた臓器を注入した多能性幹細胞が補完し、臓器欠損動物の体内に完全に多能性幹細胞由来の臓器を再生させる方法。
- (注2)多能性幹細胞:
- 胎盤などの組織(胚体外組織)を除く体中のさまざまな組織に分化する能力を持つ細胞。多能性幹細胞には2種類あり、受精卵に含まれる細胞を培養した細胞は「胚性幹細胞(ES細胞)」、体細胞に遺伝子を導入して人工的に樹立した細胞を「人工多能性幹細胞(iPS細胞)」という。
- (注3)キメラ:
- キメラ動物とは2つ以上の遺伝的背景の異なる細胞によって構成された1つの生物であり、受精卵同士の集合、受精卵への多能性幹細胞の注入によって作製する。1つの受精卵から異なる遺伝形質を持った細胞が出現するモザイクや、異種の動物同士の交配でできるハイブリッド、細胞の核を別の細胞に移植することでできるクローンとは異なる。
- (注4)MHC不適合:
- 細胞膜上に発現する主要組織適合遺伝子複合体(major histocompatibility complex:MHC)、ヒトの場合はヒト白血球型抗原(Human Leukocyte Antigen:HLA)と呼ばれる分子で、自己非自己を見分けて組織適合性を司る主要な遺伝子のことである。MHCが不適合な臓器移植の際は非自己として認識され、拒絶反応などが引き起こされる。
- (注5)レシピエント:
- 臓器移植手術や骨髄移植手術で臓器の移植を受ける患者。ドナー(臓器提供者)から臓器を提供される人。
- (注6)GVHD(移植片対宿主病):
- ドナーの臓器中あるいは輸血した血液中のリンパ球が免疫応答によってレシピエントの臓器を攻撃することによって臓器障害を引き起こしたりする症状の総称で、臓器移植に伴う合併症の1つである。これに対して<拒絶反応>はレシピエントの免疫応答によってドナーの移植片が攻撃されることによる合併症の総称であり、GVHDとは、攻撃する側と攻撃される側が反対である。
- (注7)Flk-1遺伝子:
- 血管内皮細胞増殖因子受容体(VEGFR-2・KDR/Flk-1)は血管内皮細胞膜上に発現し血管内皮増殖因子(VEGF)の結合により血管内皮細胞の増殖・遊走の促進などが起こる。Flk-1遺伝子が欠損すると血管内皮細胞膜上の血管内皮細胞増殖因子受容体が欠損するため、血管内皮細胞の欠如、血液細胞の著しい減少によりマウスでは発生初期の胎生期に子宮内で死亡する。
- (注8)EGFP:
- オワンクラゲが持つ緑色蛍光タンパク質‐GFP (green fluorescent protein)の改良型がEGFPである。各種細胞に導入することでレポーターとして利用されている。
添付資料
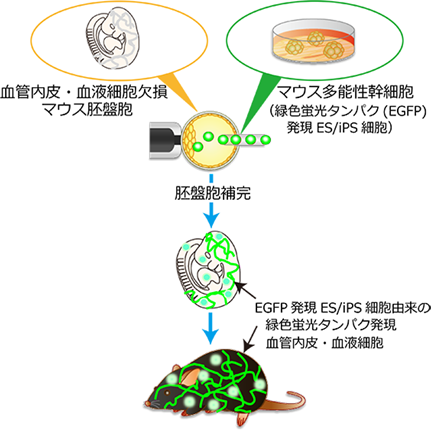
発生初期の胎生期で死亡する血管内皮・血液細胞欠損マウス胚盤胞に緑色蛍光タンパクであるEGFP(注8)を発現するマウス多能性幹細胞(ES細胞またはiPS細胞)を注入し、血管内皮・血液細胞欠損キメラマウス体内にマウス多能性幹細胞由来のEGFPを発現する血管内皮・血液細胞を作製する(胚盤胞補完)。マウスに示した緑色の線はEGFPを発現するマウス多能性幹細胞由来の血管内皮と血液細胞を表す。
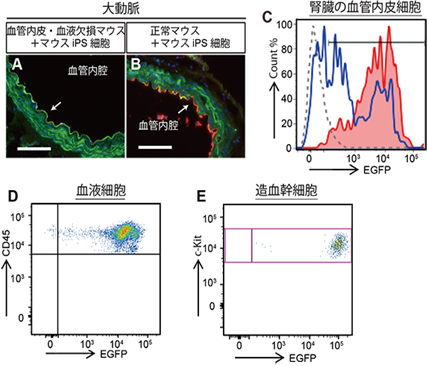
(A、B)は、大動脈の組織切片像で血管内腔側が血管内皮(矢印)である。血管内皮は赤色蛍光、マウス多能性幹細胞に由来する細胞は緑色蛍光を呈する。(A)血管内皮・血液細胞欠損マウスに作製された血管内皮はマウスiPS細胞由来であったが、(B)正常マウス胚盤胞にiPS細胞を注入して作製されたキメラマウスでは、マウスiPS細胞由来の血管内皮は一部だけであった(A、B)において、白線は長さ100mを示す。(C)は腎臓の血管内皮のキメリズムを示した。血管内皮・血液細胞欠損マウス胚盤胞にiPS細胞を注入して作製されたキメラマウスの血管内皮はEGFPを発現するマウスのiPS細胞由来であった(赤線)。正常マウス胚盤胞にiPS細胞を注入して作製されたキメラマウスではEGFPを発現するマウスiPS細胞由来の血管内皮は一部であった(青線)。破線はiPS細胞を注入していない正常マウスを示す。血管内皮・血液細胞欠損マウス体内に作製された(D)血液中の血液細胞(CD45陽性細胞)と(E)骨髄中の造血幹細胞(c-Kit陽性/Sca-1陽性/Lineage陰性細胞)はEGFP陽性のマウス多能性幹細胞由来であった。
問い合わせ先
研究に関する問い合わせ先
東京大学医科学研究所 幹細胞治療部門
特任准教授 山口 智之 (ヤマグチ トモユキ)
特任研究員 濱仲 早苗 (ハマナカ サナエ)
東京都港区白金台4-6-1
Tel:03-5449-5129
Email:tomoyama"AT"ims.u-tokyo.ac.jp(山口)
sanahmnk"AT"ims.u-tokyo.ac.jp(濱仲)
JST事業に関する問い合わせ先
国立研究開発法人科学技術振興機構(JST) 研究プロジェクト推進部
内田 信裕(ウチダ ノブヒロ)
東京都千代田区五番町7 K’s五番町
Tel:03-3512-3528
Email:eratowww"AT"jst.go.jp
AMED事業に関する問い合わせ先
国立研究開発法人日本医療研究開発機構(AMED) 基盤研究事業部 研究企画課
東京都千代田区大手町1-7-1読売新聞ビル
Tel:03-6870-2224
Email:kenkyuk-ask"AT"amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
掲載日 平成30年9月21日
最終更新日 平成30年9月21日


