筋萎縮性側索硬化症(ALS)に対する高用量メチルコバラミン筋注の第3相臨床試験
 ALSの平均余命の延長が期待される製剤の医師主導治験開始
ALSの平均余命の延長が期待される製剤の医師主導治験開始
国立大学法人徳島大学大学院医歯薬学研究部の梶龍兒特命教授らの研究グループは、高用量メチルコバラミン筋注が筋萎縮性側索硬化症(ALS)発症後1年未満の生存期間を非投与群に比べて延長することを明らかにしました。本研究成果によりALSの新しい治療法として導出先企業による製造販売承認申請が予定されています。
取り組み
ALSは難治性神経疾患の一つで、上位・下位運動ニューロンの障害による筋萎縮と筋力の低下を特徴とする進行性の疾患です。歩行困難、言語障害、嚥下障害および呼吸障害などの症状があり、本人の意識や知覚が正常であるにも関わらず、生活やコミュニケーションの自由が阻害されるため、生活の質(QOL)は著しく低下します。また、経過には個人差があるものの、発症から死亡ないしは呼吸器装着までの期間(イベント発生)は20~48か月であると報告されています。(日本神経学会:筋萎縮性側索硬化症診療ガイドライン2013)
ALSの治療には現在、内服薬のリルテック®錠(リルゾール)と点滴静注薬のラジカット®(エダラボン)のみが保険適用薬として承認されていますが効果は限定的で、生存期間と機能障害の進行抑制の両方を達成する薬剤はまだ確立されていません。
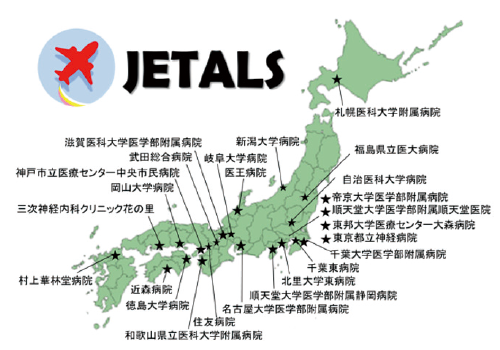
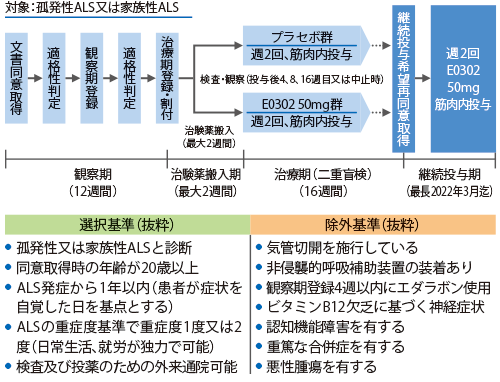
高用量メコバラミン(E0302)は、ALSを対象とした第Ⅱ/Ⅲ相試験(E0302-J081-761)にて、発症1年未満の部分集団でイベント発生率(非侵襲的呼吸補助装置の終日装着、侵襲的呼吸補助装置の装着又は死亡)までの期間の延長及びALSの機能評価スケールであるALSFRS-R合計点の低下の抑制に用量反応性が示唆されていました(図1)。この結果を踏まえ、梶龍兒特命教授らは発症1年以内のALS患者を対象に「高用量E0302の筋委縮性側索硬化症に対する第Ⅲ相試験‐医師主導治験‐」(JETALS)(E0302-TOK-763)を計画し、全国25施設による多施設共同(図2)、ランダム化、プラセボ対照二重盲検並行群間試験として2017年11月~2019年10月までの症例登録期間に観察期203例、治療期130例を組み入れ、目標の治療期128例を達成しています(図3)。
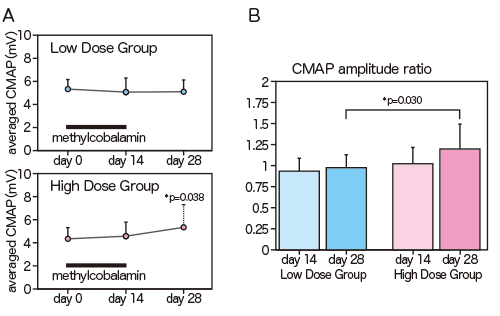
・高用量群で有意にCMAPが増大。
成果
プロトコル遵守のうえ計画通りに医師主導治験を実施し(図3)、目標例数の128例を超える130例の組み入れに成功しました。
この組み入れ症例についてデータ固定の上、契約期間内に有効性、安全性に関する解析を実施しています。
展望
現在、導出先企業において本治験結果を用いた製造販売承認申請の準備が進められています。
E0302によるALS患者への治療が承認されることで、早期に治療をされたALS患者における生存期間や呼吸器装着までの期間の延長につながるとともに、症状の進行を抑制が期待できる新しい治療選択肢となります。
最終更新日 令和3年8月13日


