光で意のままにゲノムを編集する技術を開発―CRISPR-Cas9システムの光制御を実現―
プレスリリース
東京大学
日本医療研究開発機構
発表者
二本垣 裕太(東京大学大学院総合文化研究科広域科学専攻 大学院生)
佐藤 守俊(東京大学大学院総合文化研究科広域科学専攻 准教授)
発表のポイント
- ゲノム編集(注1)を自由自在に光で制御する世界で初めての技術
- 光によるCRISPR-Cas9システム(注2)の活性制御(スイッチオン・スイッチオフ)を実現
- ゲノム編集の応用可能性が大きく広がる期待
発表概要
東京大学大学院総合文化研究科の二本垣裕太大学院生と佐藤守俊准教授らの研究グループは、「ゲノム編集」と呼ばれる遺伝子の改変操作を、自由自在に光で制御する技術を開発しました。
ゲノム編集を行うためには、ゲノム上の狙った塩基配列をDNA切断酵素で切断する必要があります。しかし、従来の技術ではDNA切断酵素の活性を全く制御できないため、たとえば、狙ったタイミングや狙った時間のみでゲノム編集を行うことが不可能であるなど、さまざまな制約が課せられていました。
本研究グループは原核生物で発見されたCRISPR-Cas9システムのDNA切断酵素(Cas9タンパク質)の活性を青色の光で制御し、ゲノムを意のままに編集できる技術を世界で初めて実現しました。
この新しい技術により、ゲノム編集の応用可能性が大きく広がることが期待されます。
本成果は、米国科学誌「Nature Biotechnology」(電子版:英国時間 6月15日(月))に掲載されます。
本成果は文部科学省 生命動態システム科学推進拠点事業の一環として得られました。平成27年度より、国立研究開発法人 日本医療研究開発機構が本事業の研究支援担当機関の役割を果たしています。
発表内容
研究の背景
2012年に原核生物のCRISPR-Cas9システムに基づくゲノム編集技術が発表されて以来、この技術は爆発的な勢いで利用され、世界中の研究室の研究スタイルを変えつつあります。この技術を利用すれば、ゲノム上の狙った遺伝子の機能を非常に簡単に破壊したり(ノックアウト)、別の塩基配列で置き換えること(ノックイン)ができます。このためゲノム編集技術は、基礎生命科学研究のみならず、医療や創薬、育種・品種改良等へ応用が期待されています。
ゲノム編集を行うためには、ゲノム上の狙った塩基配列をDNA切断酵素(Cas9タンパク質)で切断する必要があります。しかし、従来の技術ではCas9タンパク質のDNA切断活性を全く制御できないため、ゲノム編集にさまざまな制約が課せられていました。このため、Cas9の活性を制御できる技術の開発が強く求められていました。
研究内容(技術の説明)
本研究グループはCas9の制御を実現するために、まずCas9タンパク質を二分割してそのDNA切断活性を不活性化しました(図1)。さらに、二分割により活性を失ったCas9のN末端側断片(N-Cas9)とC末端側断片(C-Cas9)に同研究グループが最近開発した小さな光スイッチタンパク質(pMag,nMag、注3)を連結しました。pMagとnMagは青色の光に応答して互いに結合するタンパク質です。青色の光を照射すると、pMagとnMag の結合に伴って、N-Cas9とC-Cas9も互いに近接し結合します。これにより、N-Cas9とC-Cas9は本来のCas9タンパク質のようにDNA切断活性を回復し、標的の塩基配列を切断できるようになります(スイッチオン)。なお、光照射を止めるとpMagとnMagは結合力を失うため、N-Cas9とC-Cas9も離れ離れになり、DNA切断活性は消失します(スイッチオフ)。
本研究グループは、上述のように開発したツール(以後、光活性化型Cas9(paCas9)と呼ぶ)を用いて、狙ったゲノム遺伝子の塩基配列を改変し、その機能を破壊(ノックアウト、図2)できることを示しました。また、狙ったゲノム遺伝子の塩基配列を別の塩基配列に置換(ノックイン、図2)できることも示しました。さらに、光照射のパターンを制御することにより、ゲノム編集を空間的に制御できることも実証しました(図3)。
さらに本研究グループは、paCas9に変異を加えてDNA切断活性を欠失させることにより、ゲノム上の狙った遺伝子に結合して当該遺伝子の発現を光で可逆的に抑制する技術も開発しました(図4)。
上述のように本研究グループは、CRISPR-Cas9システムを光照射のオン・オフで制御する技術を開発し、光によるゲノム編集の制御を世界で初めて実現しました。既存の技術では、狙ったタイミングや狙った時間でのみゲノム編集を実行することは不可能でした。paCas9を用いればDNA切断活性の持続時間を非常に短く制御できるため、既存の技術が抱える、目的としない塩基配列のDNA切断というオフターゲットの問題(注4)を低減できると期待されます。また、既存の技術ではゲノム編集を空間的に制御することは不可能でしたが、paCas9を用いれば、例えば脳における神経細胞のように、組織の中で狙った細胞単位でのゲノム編集が実現すると期待されます。以上のように、本研究グループが開発した技術は、ゲノム編集の応用可能性を大きく広げ、医療や創薬、育種・品種改良等に貢献することが期待されます。
発表雑誌
- 雑誌名:
- 「Nature Biotechnology」(6月15日(英国時間)オンライン)
- 論文タイトル:
- Photoactivatable CRISPR-Cas9 for optogenetic genome editing
- 著者:
- Yuta Nihongaki, Fuun Kawano, Takahiro Nakajima, Moritoshi Sato*
- DOI番号:
- 10.1038/nbt.3245
用語解説
- (注1)ゲノム編集技術
- ゲノム上の遺伝子の塩基配列を改変してその機能を破壊したり(ノックアウト)、別の塩基配列で置き換える(ノックイン)技術のこと。
- (注2)CRISPR-Cas9システム
- ゲノムの切断を人為的に行うための技術。Cas9と呼ばれるDNA切断酵素がガイドRNAと共にDNAに結合し、そのDNA配列を部位特異的に切断します。このCRISPR-Cas9システムは、バクテリオファージに対する原核生物の免疫システムとして発見されましたが、2012年以降、ゲノム編集に利用されています。ガイドRNAの5’末端の塩基配列(20塩基程度)を適切に設計するだけで、ゲノムの切断部位を決定できる簡便性が大きな特徴です。
- (注3)光スイッチタンパク質(pMag,nMag)
- アカパンカビ(Neurospora crassa)が有する小さな光受容体のヴィヴィッド(Vivid)に対して多角的にプロテインエンジニアリングを施して開発されたタンパク質の対。本研究グループにより開発(Nat. Commun. 6, 6256 (2015). doi: 10.1038/ncomms7256)。pMagとnMagは暗所では単量体として存在し、青い光を受容するとヘテロ二量体を形成します。このような光による単量体と二量体の変換を利用して、さまざまな光活性化型のツールを設計・開発できます。
- (注4)オフターゲットの問題
- 標的部位以外でもDNAの切断と塩基配列の改変が起こってしまう問題を指します。従来のDNA切断酵素(Cas9)は全く活性制御ができないため、細胞内にCas9タンパク質を導入すると、そのDNA切断活性は長時間持続します。そのため、生じる既存技術の大きな問題として認識されていました。paCas9はDNA切断活性の持続時間を非常に短く制御できるため、このオフターゲットの問題を低減できると期待されます。
添付資料
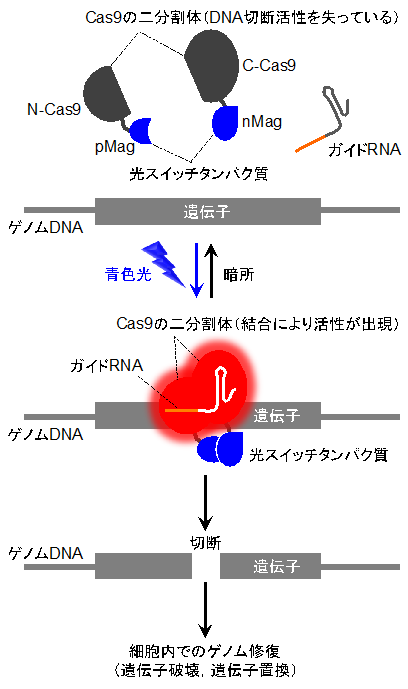
図1 本技術の原理
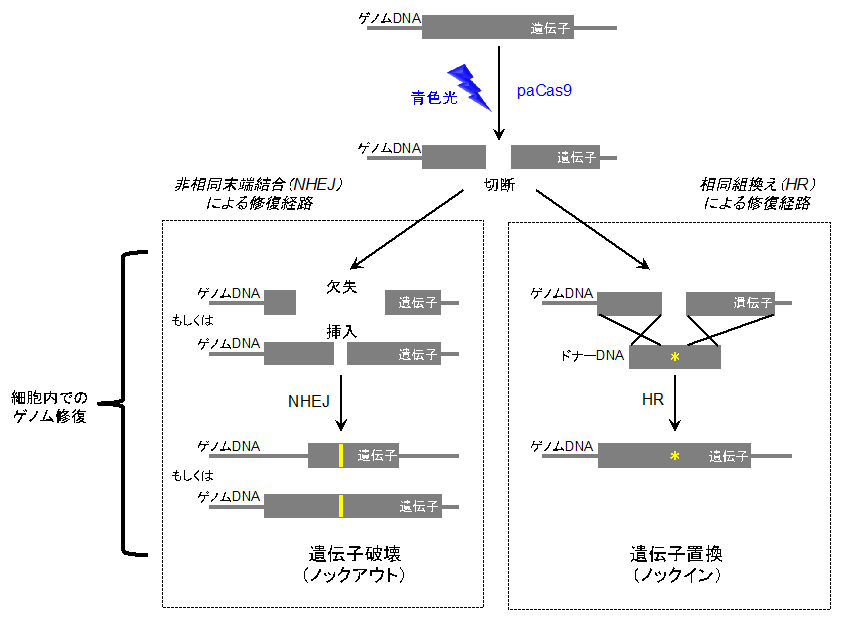
図2 ゲノム上の塩基配列の切断とそれに引き続くゲノムの修復
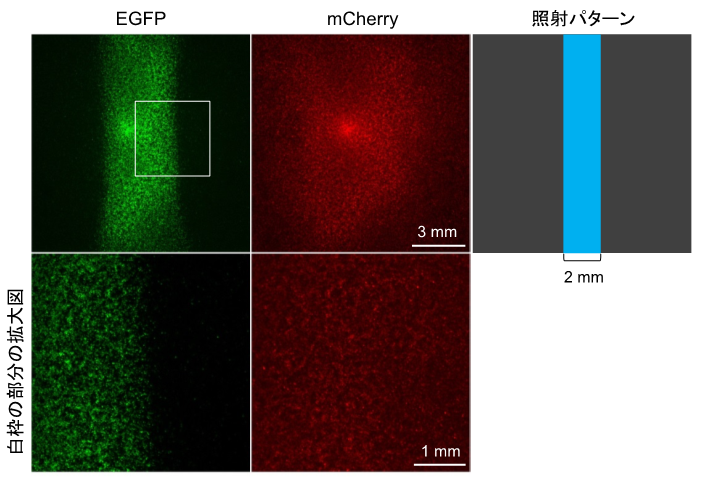
図3 ゲノム編集を空間的に制御
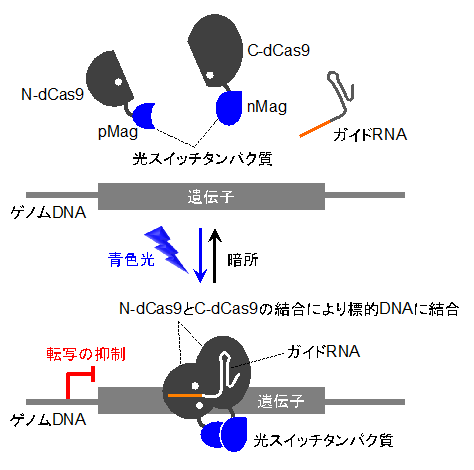
図4 狙ったゲノム遺伝子の発現を光照射で抑制する技術
問い合わせ先
東京大学大学院総合文化研究科
准教授 佐藤 守俊(さとう もりとし)
〒153-8902 東京都目黒区駒場3-8-1
Tel:03-5454-6579
E-mail:cmsato”AT”mail.ecc.u-tokyo.ac.jp
AMED事業に関するお問い合わせ先
国立研究開発法人日本医療研究開発機構(AMED)
〒100-0004 東京都千代田区大手町一丁目7番1号
創薬戦略部 医薬品研究課
TEL:03-6870-2219
E-mail:souyakukiban"AT"amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください
関連リンク
掲載日 平成27年6月16日
最終更新日 平成27年6月16日


