ヒトES細胞から機能的な下垂体ホルモン産生細胞の分化に世界で初めて成功
プレスリリース
国立大学法人名古屋大学
国立研究開発法人理化学研究所
国立研究開発法人科学技術振興機構
国立研究開発法人日本医療研究開発機構
名古屋大学大学院医学系研究科(研究科長・髙橋雅英)糖尿病・内分泌内科(教授・有馬寛)の須賀英隆(すがひでたか)助教(責任著者)および、理化学研究所多細胞システム形成研究センター(センター長・濱田博司)器官誘導研究チームの辻孝(つじたかし)チームリーダー、大曽根親文(おおぞねちかふみ)リサーチアソシエイト(筆頭著者)、同センター立体組織形成研究チームの永樂元次(えいらくもとつぐ)チームリーダーらのグループは、ヒト胚性幹細胞(ES細胞)[1]を用い、下垂体[2]前葉のホルモン産生細胞[3]を分化誘導させる方法を確立しました。
本研究成果は、英国科学誌『Nature Communications』誌(2016年1月14日5時(米国東部時間))に掲載されます。
下垂体は様々なホルモンを分泌する内分泌器官で、成人で1センチ程度の小さな器官ですが、全身の恒常性を保つために大きな働きをしています。そのため、下垂体が機能しなくなると、血圧低下や電解質異常、基礎代謝の低下、成長障害、不妊など、欠乏したホルモンに応じた様々な重い症状を引き起こします。
本研究グループは、2011年にマウスのES細胞から下垂体組織を作ることに成功しており、このたび、この培養技術をさらに改良・発展させ、ヒトES細胞から立体的な下垂体のもと(下垂体原基[4];ラトケ嚢とも呼ばれる)を試験管内で作り出すことにも世界で初めて成功しました。さらに、数週間に渡る長期培養方法を開発した結果、成熟した下垂体ホルモン産生細胞を誘導することにも成功しました。こうしてできたホルモン産生細胞は、生体内の下垂体細胞と同様にホルモンを分泌し、さらに下垂体の機能を失ったマウスに移植すると生存率が著しく向上するなど、治療効果も認められました。
本研究の成果は、下垂体の機能が低下した患者さんに対する再生医療の可能性を示しただけでなく、下垂体疾患の発症メカニズムの解明や新規薬剤の開発にも役立つと考えられます。
本成果は、国立研究開発法人科学技術振興機構(JST)再生医療実現拠点ネットワークプログラム(平成27年度より、国立研究開発法人日本医療研究開発機構(AMED)へ移管)の一環として得られました。
ポイント
- ヒトES細胞から下垂体ホルモン産生細胞への分化誘導方法を確立。
- 誘導した下垂体細胞は実際にホルモンを分泌し、生体と同じ機能を明示。
- 下垂体機能不全マウスへの移植による、治療効果を実証
背景
下垂体は、様々なホルモンを制御する司令塔とも言うべき中心的な働きをしており、成長・思春期・代謝・ストレス反応・妊娠・出産など、多岐にわたる生命現象をコントロールするのに重要な役割を担っています。
そのため、下垂体ホルモン産生細胞の機能が低下すると、血圧低下や電解質異常、意識障害、成長障害、不妊など、様々な重い症状を引き起こします。現在、根治療法は存在せず、不足しているホルモンを投与する補充療法が行われています。しかしながら生涯に渡ってホルモンを投与し続けなくてはならない問題点や、時々刻々と変動するホルモン必要量に対して現行の補充治療では十分には対応できない問題点があります。したがって、もし生体内の下垂体と同様の機能をもったホルモン産生細胞が再生できれば、根治療法の第一歩となる可能性があります。
研究成果
下垂体は、生体内において口腔外胚葉[5]と視床下部[6]という2つの異なる組織が相互作用することによって形成されます。研究グループは、ヘッジホッグ[7]シグナルを強める化合物(SAG)と骨形成タンパク質(BMP)[7]をヒトES細胞に対して作用させることで、口腔外胚葉と視床下部を同時に試験管内で誘導することに成功し、そこから下垂体原基が自己形成されることを示しました(図1)。さらに、線維芽細胞増殖因子(FGF)[7]を加えることで、下垂体原基の形成効率が向上することも明らかにしました。
この長期培養技術の向上を行った結果、ヒトES細胞由来の下垂体原基を成熟させ、ホルモン産生細胞に分化させることに成功しました(図2)。下垂体前葉には、代表的な6種類のホルモン産生細胞がありますが、その全てが分化誘導されることも確認しました。それらは生体内では分化の途中でいくつかの細胞系譜に分かれて生じることが分かっていますが、本研究でもそれに即した誘導方法を確立しました。誘導されたホルモン産生細胞を電子顕微鏡で観察すると、内分泌細胞に特徴的な分泌顆粒が存在し、高い成熟度を得ていることが明らかになりました。特に、副腎皮質刺激ホルモン(ACTH)細胞と成長ホルモン(GH)細胞については、試験管内でホルモン分泌刺激シグナルおよび抑制シグナル[8]双方に正しく反応し(図3)、内分泌細胞としての機能を備えていることを示しました。
最後に、ヒトES細胞由来のACTH細胞を下垂体機能不全[9]モデルマウスに移植し、血中ACTHやその下流で働く糖質コルチコイド[10]が上昇すること、その結果、活動性や生存率が向上することを示しました(図4)。
今後の展開
生体と同じ機能を備えた下垂体を作り出すことに成功していることから、今後、下垂体機能不全に対する再生医療に応用できることが期待されます。また、ヒトの下垂体発生のモデルとしての利用や、疾患特異的iPS細胞[1]を用いた下垂体疾患モデルとしての応用も見込め、新規薬剤の開発にも役立つと考えられます。
用語説明
- [1] 胚性幹細胞(ES細胞)/人工多能性幹細胞(iPS細胞)
- 胚性幹細胞(ES細胞)とは発生初期の動物胚に存在する内部細胞塊から作られる細胞で、あらゆる種類の体細胞へ分化する能力と、ほぼ無限に増殖する能力を合わせ持つ多能性幹細胞の1つである。人工多能性幹細胞(iPS細胞)は皮膚などの体細胞に遺伝子を導入することによって得られる多能性幹細胞である。
- [2] 下垂体
- 下垂体は、全身に向かって各種ホルモンを放出する内分泌の中枢器官。頭部の正中に位置し、視床下部の腹側に接する場所にある。ヒトでは直径1センチ程度の大きさ。下垂体のもとになる組織をラトケ嚢と呼ぶ。
- [3] 下垂体ホルモン産生細胞
- 下垂体から分泌される主要なホルモンとして、
- 生命維持に必須の副腎皮質ホルモンの産生を促す副腎皮質刺激ホルモン(ACTH)
- 身体の成長を促す成長ホルモン(GH)
- 授乳時に乳汁分泌を促す乳汁分泌ホルモン(PRL)
- 甲状腺の機能を調整する甲状腺刺激ホルモン(TSH)
- 精巣や卵巣機能を調整する性腺刺激ホルモン(LH/FSH)
- [4] 下垂体原基(ラトケ嚢)
- 胚の中の器官のもととなる組織を原基とよぶ。下垂体の場合、マウスでは胎生10~11日に口腔外胚葉の一部から形成される袋状の構造であるラトケ嚢がそれに当たる。ラトケ嚢はさらに成熟して、下垂体を形成する。
- [5] 口腔外胚葉
- 胚の発生過程で、口腔粘膜の表皮を形成する1層の細胞を口腔外胚葉という。口腔外胚葉は初期胚において視床下部に隣接する外胚葉から発生し、その一部は下垂体のもとになるラトケ嚢を形成する。
- [6] 視床下部
- 視床下部は、脳の一部であり、大脳の腹側に存在する。体の恒常性、血圧、水分調節、摂食など生命維持に必須の役割を果たす脳の中枢。視床下部は隣接する下垂体に各種の「放出ホルモン」を送ることにより、下垂体から特定のホルモンを全身に向かって放出させる。
- [7] ヘッジホッグ・骨形成タンパク質(BMP)・線維芽細胞増殖因子(FGF)
- 生体内において、細胞の増殖を刺激するような活性を有する物質。増殖刺激以外にも多様な生理活性を持つものが多く、ES細胞などの幹細胞の分化制御を含め多彩な機能を発揮することが知られている。
- [8] ホルモン分泌刺激シグナルおよび抑制シグナル
- 一般に、ホルモンはわずかな血中濃度で大きな生体の反応を引き起こすため、多すぎても少なすぎても障害を引き起こす。それを防ぐため、生体ではフィードバックと呼ばれる制御により、そのバランスが維持されている。副腎皮質ホルモンを例に挙げると、視床下部の副腎皮質刺激ホルモン放出ホルモンが、下垂体から副腎皮質刺激ホルモンを分泌させ、それが副腎皮質から副腎皮質ホルモンを分泌させる。これは正の制御連鎖だが、最後にできた副腎皮質ホルモンが過剰に産生されると身体のバランスを崩すことになる。そのため、副腎皮質ホルモンが過剰になると、視床下部や下垂体に働き、副腎皮質刺激ホルモン放出ホルモンや副腎皮質刺激ホルモンの分泌を抑制する。このように下流の産生物が、上流の制御系に対して負の制御をすることで一定の量的バランスを維持している。
- [9] 下垂体機能不全
- 下垂体のホルモン分泌機能が低下した状態。副腎皮質刺激ホルモン、成長ホルモン、甲状腺刺激ホルモン、性腺刺激ホルモン、乳汁分泌ホルモンなどが不足することで様々な身体の不調を起こす。治療法としては、不足したホルモンを投与する補充療法があるが、生涯ホルモンを投与し続ける必要がある、刻々と変化するホルモンの必要量に対応できないなどの課題がある。
- [10] 糖質コルチコイド
- 糖質コルチコイドは副腎皮質ホルモンの一種で、副腎の表面にある副腎皮質から分泌される。副腎皮質ホルモンは、体のさまざまな恒常性の維持(血糖、血圧、ミネラルバランスなど)に必須だが、特に身体がストレスを受けた時に、それに耐える反応を起こすのに重要。そのため、副腎皮質ホルモンの完全欠損は致命的となり、部分的な欠乏でも身体に異常を引き起こす。糖質コルチコイドの分泌は、下垂体から血中に分泌される副腎皮質刺激ホルモン(ACTH)により促進され、ACTHの低下は糖質コルチコイドの欠乏を引き起こす。
発表雑誌
Chikafumi Ozone, Hidetaka Suga, Mototsugu Eiraku, Taisuke Kadoshima, Shigenobu Yonemura, Nozomu Takata, Yutaka Oiso, Takashi Tsuji & Yoshiki Sasai. Functional anterior pituitary generated in selforganizing culture of human embryonic stem cells. Nature Communications (2016).
DOI: 10.1038/ncomms10351
添付資料
-
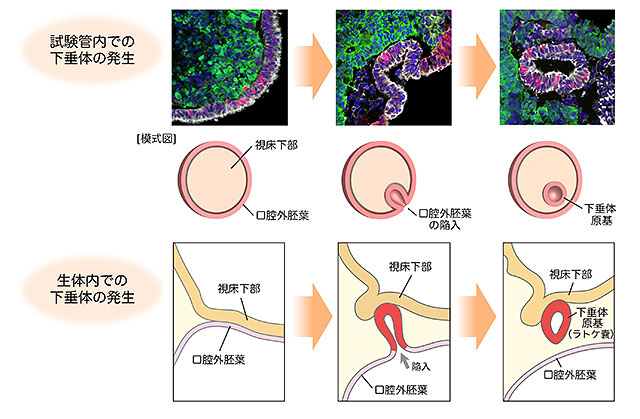 図1 ヒトES細胞から下垂体原基の試験管内3次元誘導
図1 ヒトES細胞から下垂体原基の試験管内3次元誘導
-
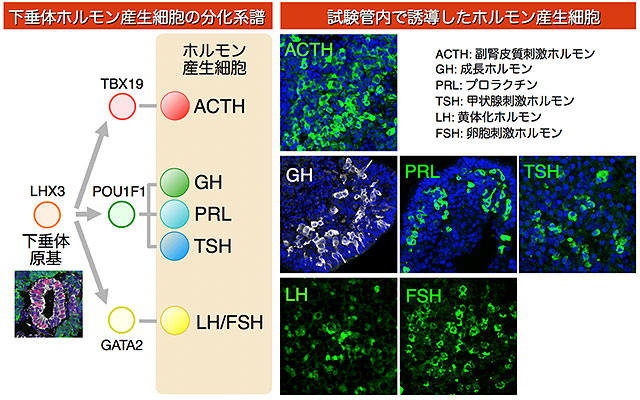 図2 下垂体前葉ホルモン産生細胞の分化
図2 下垂体前葉ホルモン産生細胞の分化
-
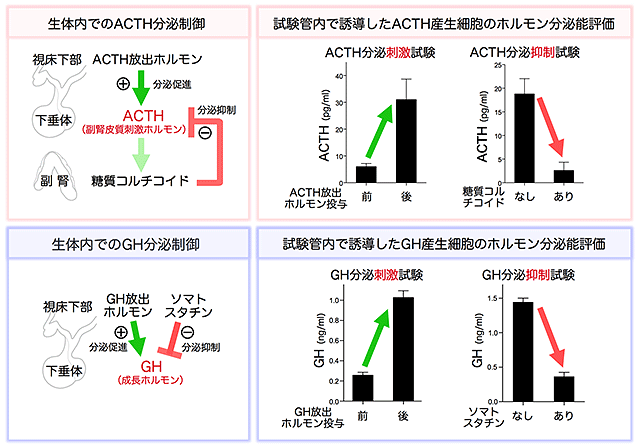 図3 ヒトES細胞から誘導された下垂体組織のホルモン分泌機能評価
図3 ヒトES細胞から誘導された下垂体組織のホルモン分泌機能評価
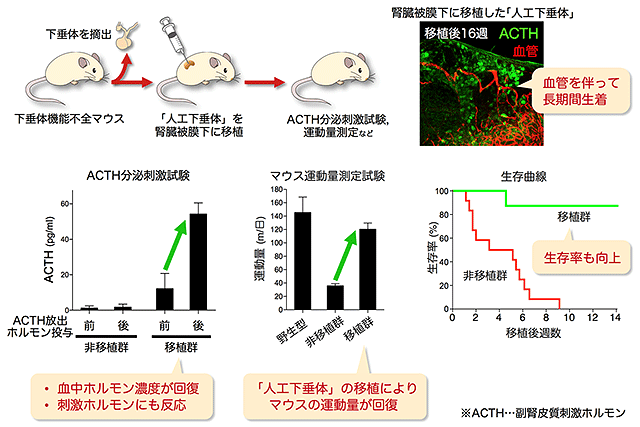 図4 試験管内で誘導したACTH産生細胞(人工下垂体)の移植による治療効果
図4 試験管内で誘導したACTH産生細胞(人工下垂体)の移植による治療効果
お問い合わせ先
内容に関するお問い合わせ
所属:糖尿病・内分泌内科 助教
氏名:須賀 英隆
TEL:052-744-2140
FAX:052-744-1352
E-mail:sugahide“AT”med.nagoya-u.ac.jp
報道に関するお問い合わせ
名古屋大学医学部・医学系研究科総務課総務係
広報担当
TEL:052-744-2228
FAX:052-744-2785
E-mail:iga-sous“AT”adm.nagoya-u.ac.jp
理化学研究所 広報室 報道担当
TEL:048-467-9272
FAX:048-462-4715
E-mail:ex-press“AT”riken.jp
科学技術振興機構 広報課
TEL:03-5214-8404
FAX:03-5214-8432
E-mail:jstkoho“AT”jst.go.jp
事業に関する問い合わせ
国立研究開発法人 日本医療研究開発機構(AMED)戦略推進部 再生医療研究課
〒100-0004東京都千代田区大手町一丁目7番1号
TEL:03-6870-2220
E-mail:saisei“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
最終更新日 平成28年1月14日


