ヒトiPS細胞におけるグルタミン代謝の特徴を利用し安全性を高めた心筋細胞の作製に成功―心臓の再生医療の実現化を大きく加速―
プレスリリース
慶應義塾大学医学部
国立研究開発法人日本医療研究開発機構(AMED)
慶應義塾大学医学部循環器内科学教室の遠山周吾助教、藤田淳特任講師、福田恵一教授らの研究グループと、慶應義塾大学医学部医化学教室の末松誠教授(当時。現AMED理事長)らの研究グループは、ヒトiPS細胞由来の分化細胞集団から、臨床応用の課題であった腫瘍化の原因となる細胞を高水準で除去し、より安全性を高めた心筋細胞を作製することに成功しました。
心筋梗塞、拡張型心筋症(注1)などが重症化すると数億個もの心筋細胞が失われてしまいますが、ヒトを含む哺乳類は失われた心筋細胞を元に戻す自己再生能力を持っていません。胚性幹細胞(ES細胞)(注2)や人工多能性幹細胞(iPS細胞)(注3)は、理論的に体を構成するすべての細胞種へと分化できる多能性を持つことから、このような疾患に対し、体外で作製した治療細胞を体内に移入することによる「再生医療」の実現が期待されています。しかし、すべての未分化幹細胞(注4)を目的とする細胞へ分化誘導することは困難であり、分化できなかった細胞の中に腫瘍形成の原因となる細胞が混入してしまうことが実現化の大きなハードルになっていました。
今回、共同研究グループは、ヒトES・iPS細胞におけるグルコースおよびグルタミン代謝の役割を明らかにし、培養液から全ての細胞の生存に必須とされるグルコースおよびグルタミンを除去し、この代替物として心筋細胞だけが効率よく利用することのできる乳酸を添加する工夫をしました。その結果、腫瘍形成の原因となる未分化幹細胞を完全に死滅させ、心筋細胞だけを生きたまま選別する方法を確立することに成功しました。これによって、特殊な培養液に交換するという極めて単純な工程によって、臨床応用を視野に入れた高純度の心筋細胞を作製することが可能となりました。この研究成果は、安全性の高い心筋細胞を比較的安価かつ簡便に入手するという大きな課題を解決し、心臓の再生医療の実現化を大きく加速するものと考えます。
本研究は、国立研究開発法人日本医療研究開発機構(AMED)「再生医療の実現化ハイウェイ」、国立研究開発法人科学技術振興機構(JST)「健康研究の実用化加速のための研究・開発システム関連の挨路解消を支援するプログラム」等の助成によって行われました。本研究成果は2016年3月31日正午(米国東部時間)に、米科学誌「Cell Metabolism」に掲載されます。
1.研究の背景
ヒトES細胞やiPS細胞のような多能性幹細胞は、多種類の体細胞に分化出来る能力を有している反面、分化させた細胞集団の中に未分化幹細胞が残存する性質があることがわかっています。仮にこうした未分化幹細胞が生体内に移植されると、腫瘍を形成する危険性があるため、目的とする細胞を純化精製すると同時に、未分化幹細胞を除去する方法の開発が望まれてきました。この課題に対する先行研究として、遺伝子改変などによって心筋細胞を蛍光蛋白でラベル化し、特殊な機械を用いて、1細胞ずつ心筋細胞を分取する方法が報告されていました。
細胞の培養は培養液という細胞の生存にとって重要な栄養素を含む液体中で行いますが、その必要成分は細胞の種類によって異なっているとされます。2013年に我々のグループは、未分化幹細胞においてグルコース代謝が活発であること、心筋細胞は乳酸をエネルギー源とすることを明らかにし、培養液に含まれているグルコースを除去し乳酸を添加することで未分化幹細胞を除去する方法を報告しました(Tohyama, Cell Stem Cell 2013)。しかし、ヒトES・iPS細胞はグルコースを除去するだけでは完全に死滅するのに時間を要するという問題がありました。
そこで、培養液に含まれる成分のうち細胞の生存にとって重要なアミノ酸に着目しました。ヒトES・iPS細胞等の未分化幹細胞にとっては非常に重要で、心筋細胞によっては重要ではないアミノ酸を同定することにより、さらに効率よく未分化幹細胞を除去できるのではないかと考え、今回の研究を行い、前述の問題の原因としてヒトES・iPS細胞におけるグルタミン代謝が関与していることを見出しました。
2.研究成果
未分化幹細胞におけるアミノ酸代謝について
除去したい未分化幹細胞にとって重要なアミノ酸を探索するため、各アミノ酸における消費量を解析しました。その結果、ヒトES・iPS細胞(未分化幹細胞)ではグルコースと同等に消費が活発なアミノ酸が複数存在することが明らかになりました。そこで、消費が活発な4つのアミノ酸(グルタミン、アルギニン、セリン、グリシン)を除去した条件に加えて、グルコースも除去した培養液を用いてヒトES・iPS細胞を培養したところ、アミノ酸を除去しなかった場合と比較してヒトES・iPS細胞が劇的に死滅することがわかりました。さらに、その4つのアミノ酸のうち最も重要なアミノ酸がグルタミンであることを見出しました。次に、ヒトES・iPS細胞におけるグルタミン代謝の役割をトランスクリプトーム解析(注5)およびメタボローム解析(注6)を行ったところ、ヒトES・iPS細胞はグルタミンを活発に取り込んでミトコンドリアにおける酸化的リン酸化により(注7)エネルギーを得ていることを明らかにしました(図1)。一方で、ヒトES・iPS細胞はピルビン酸を効率代謝出来ない仕組みを有していることを見出しました。
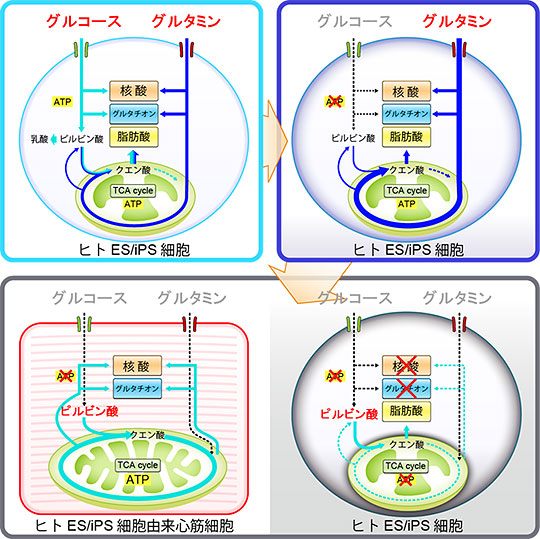 図1 ヒトES・iPS細胞と心筋細胞におけるグルコースおよびグルタミン代謝
図1 ヒトES・iPS細胞と心筋細胞におけるグルコースおよびグルタミン代謝
グルコースだけを除去する従来の方法に加え、グルタミンを除去すると完全にエネルギー源を絶たれるため、ヒトES・iPS細胞は速やかに死滅することを見出しました。
心筋細胞は乳酸を効率よく代謝し、エネルギーを産生することで生存することができます。
未分化幹細胞と心筋細胞の代謝の違いを利用した心筋純化精製法について
未分化幹細胞と心筋細胞の代謝の違いに着目し、“未分化幹細胞やその他の増殖細胞が生存不可能で、心筋細胞のみが生存可能な代謝環境”を作り出すために、通常は培養液に必要不可欠とされるグルコースおよびグルタミンを除去し、心筋細胞にとってエネルギー源となる乳酸を添加することにより、心筋細胞のみを選別できるのではないかと考え、“無グルコース無グルタミン乳酸添加培養液”を作製しました。実際に、ヒトES・iPS細胞由来の様々な細胞集団をこの培養液で培養すると、短期間で未分化幹細胞が完全に死滅し、心筋細胞のみが選別されることが確認されました(図2)。グルコースおよびグルタミン非存在下における心筋細胞の乳酸代謝の役割を解明するためにメタボローム解析を行ったところ、心筋細胞では乳酸を利用してエネルギーを得ているのみならず、乳酸を利用してグルタミン酸を産生していることが明らかになりました(図1)。さらに、選別されたヒトES細胞由来の心筋細胞には腫瘍を形成する原因となる未分化幹細胞が残存しておらず、その残存率は0.001%未満であることが確認されました。また、純化精製後の心筋細胞はそのほとんどが心室筋細胞であることも明らかとなりました。
以上のことから、1細胞ずつ選別することなく、特殊な培養液に交換するという極めて単純な工程によって、腫瘍化の原因となる細胞を効率よく除去し、臨床応用を視野に入れた高水準の心筋細胞を作製することが可能となりました(図2)。
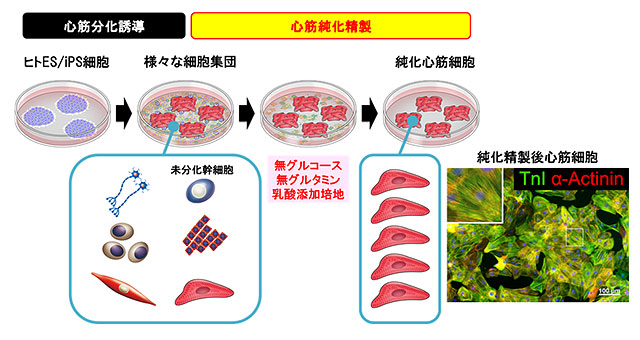 図2 無グルコース無グルタミン乳酸添加培地を用いた心筋純化精製法
図2 無グルコース無グルタミン乳酸添加培地を用いた心筋純化精製法
3.今後の展開
本技術の確立により、特殊な機械を用いて細胞を1つずつ選別することなく、特殊な培養液に曝露させるという比較的安価かつ簡便な方法で残存する未分化幹細胞を除去し、臨床応用を視野に入れた高水準の心筋細胞を作製することが可能となりました。今回の発見は、ヒトiPS細胞から分化させた心筋細胞を用いて心臓再生医療を行う際に、安全性が担保された心筋細胞を大量に得る上で極めて重要な技術であると期待されます(図3)。
今回の成果を元に、研究グループでは心臓再生医療の実現化に向けて、PMDAとの相談を開始し、医師主導の臨床研究、臨床治験の準備を実施する予定です。
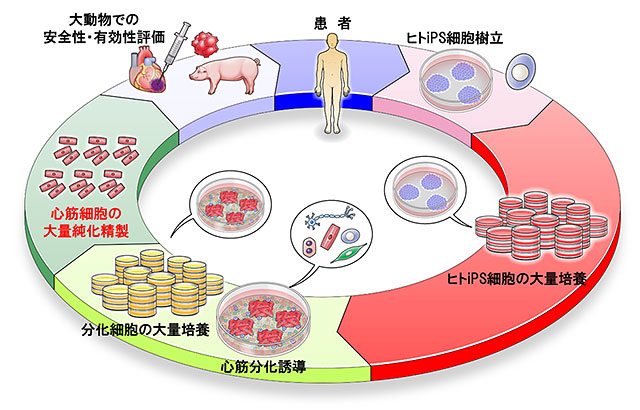 図3 我々の目指す心臓再生医療
図3 我々の目指す心臓再生医療
4.論文名
“Glutamine Oxidation Is Indispensable for Cell Survival of Human Pluripotent Stem Cells”
「ヒトES細胞・iPS細胞におけるグルタミン代謝の役割を解明」
遠山周吾、藤田淳、菱木貴子、松浦友美、服部文幸、大野麗、金澤英明、関倫久、中嶋一晶、岸野喜一、岡田麻里奈、平野暁教、黒田拓也、安田智、佐藤陽治、湯浅慎介、佐野元昭、末松誠、福田恵一
Cell Metabolism, 2016 (e-pub online)
5.本研究への支援
本共同研究は、下記機関より資金的支援を受け実施されました。
国立研究開発法人日本医療研究開発機構(AMED)「再生医療の実現化ハイウェイ」
文部科学省 先導的創造科学技術開発費補助金「健康研究の実用化加速のための研究・開発システム関連の挨路解消を支援するプログラム」
用語解説
- 注1:拡張型心筋症
- 心筋細胞の異常により心筋細胞が失われ、心室における筋肉の収縮能が著しく低下し、心室が拡張する疾患。心臓移植の適応疾患の一つ。
- 注2:胚性幹細胞(ES細胞:embryonic stem cell)
- ES細胞は受精後6、7日目の胚盤胞から細胞を取り出し、それを培養することによって作製される多能性幹細胞の一つで、あらゆる組織の細胞に分化することができる。
- 注3:人工多能性幹細胞(iPS 細胞:induced pluripotent stem cell)
- 体細胞に特定因子を導入することにより樹立される、ES細胞に類似した多能性幹細胞。2006年に山中教授の研究グループにより世界で初めてマウス体細胞を用いて樹立された。受精卵を破壊する必要がなく、患者自身の細胞から作製することが可能なため、免疫拒絶の問題が理論上ない。
- 注4:未分化幹細胞
- ES細胞やiPS細胞を含む、腫瘍形成の原因となる細胞。ES細胞やiPS細胞は様々な体細胞に分化することができるが、この未分化幹細胞が残存することにより、細胞移植後に腫瘍を形成する可能性があることが知られており、ES細胞やiPS細胞を扱う上での大きな問題となっている。
- 注5:トランスクリプトーム解析
- 細胞に存在する全遺伝子を網羅的に解析することにより、細胞の特徴を解明することができる。
- 注6:メタボローム解析
- 細胞や組織内に存在する全代謝産物を網羅的に解析すること。メタボローム解析は、細胞における代謝を包括的に理解する目的以外にも、病気におけるバイオマーカー探索や創薬開発への応用が期待されている。
- 注7:酸化的リン酸化
- ミトコンドリアの電子伝達系を用いたエネルギー合成反応。酸素を利用し、効率よくエネルギーを合成することができる。
お問い合わせ先
本発表資料について
慶應義塾大学医学部循環器内科学教室 教授
福田恵一(ふくだ けいいち)
TEL:03-5363-3874 FAX:03-5356-3875
E-mail:kfukuda“AT”a2.keio.jp
慶應義塾大学医学部循環器内科学教室 助教
遠山周吾(とおやま しゅうご)
TEL:03-5363-3446 FAX:03-5356-3875
E-mail:shugotohyama“AT”gmail.com
本リリースの発信元
慶應義塾大学 信濃町キャンパス総務課
谷口・吉岡
〒160-8582 東京都新宿区信濃町35
TEL:03-5363-3611 FAX:03-5363-3612
E-mail:med-koho“AT”adst.keio.ac.jp
事業について
国立研究開発法人日本医療研究開発機構
戦略推進部 再生医療研究課
TEL:03-6870-2220
E-mail:saisei“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
掲載日 平成28年4月1日
最終更新日 平成28年4月1日


