ドラッグリプロファイリングによる中東呼吸器症候群(MERS)コロナウイルス感染を阻害する薬物の同定
プレスリリース
国立研究開発法人日本医療研究開発機構
1.発表者:
井上純一郎(東京大学医科学研究所 分子発癌分野 教授、アジア感染症研究拠点 北京拠点長)
松田善衛(東京大学医科学研究所 アジア感染症研究拠点 特任教授)
2.発表のポイント:
- 中東呼吸器症候群(MERS)の原因ウイルス(MERSコロナウイルス)の感染の最初の過程であるウイルス外膜と細胞膜との融合を簡便かつ定量的に評価できるハイスループット測定系を開発し、MERSコロナウイルスの感染を効果的に阻害する薬剤を同定した。
- 感染性の生ウイルスを用いずにハイスループットでウイルス外膜と細胞膜との融合を阻害する化合物を探索できる測定系を開発し、従来発表されている阻害剤に比べて約100分の1の低濃度で効果を有する阻害剤nafamostatを見いだした。
- 今回見いだされた阻害剤nafamostatは既に他疾患で臨床使用されている薬剤であることから、中東呼吸器症候群に対する治療への速やかな応用、またその派生化合物の解析により新規薬剤開発も期待できる。
3.発表概要:
東京大学医科学研究所アジア感染症研究拠点の井上純一郎教授と山本瑞生特任研究員は同拠点松田善衛特任教授らの研究グループによって開発されたデュアルスプリットプロテイン(DSP、注1)と呼ばれるレポーター蛋白質を応用し、中東呼吸器症候群(MERS)の原因ウイルスであるMERSコロナウイルスが細胞に侵入する最初の過程であるウイルス外膜と細胞膜との融合を感染性の生ウイルスを使用せずに安全、簡便かつ定量的に評価できる膜融合ハイスループット測定系を開発した。この測定系を用いてドラッグリプロファイリング(注2)を目的に既に臨床適用されている薬剤を対象にスクリーニングを実施した結果、セリンプロテアーゼ阻害剤であるnafamostatが従来発表されている融合阻害剤に比べて約100分の1の低濃度で膜融合を阻害する事を見いだした。また、国立感染症研究所ウイルス第3部竹田誠部長、松山州徳室長らとの共同研究により実際にnafamostatがMERSコロナウイルスの細胞への感染を低濃度で阻害する事も確認した。
中東呼吸器症候群は2012年に発見された新興ウイルス感染症で、基礎疾患を持つ個人においては40%に上る致死率を持つと考えられている。現在まで有効なワクチンや薬剤は実用化されていない。今回発見されたnafamostatは他疾患での臨床使用が認められている薬剤であることから、その派生化合物の解析などを含めて本成果は中東呼吸器症候群の治療法開発に大きく貢献すると期待される。本研究は国立研究開発法人日本医療研究開発機構(AMED)による感染症研究国際展開戦略プログラム(J-GRID)の支援を受けた。
4.発表内容:
中東呼吸器症候群(MERS)は2012年に報告された重症呼吸器感染症であり、特異的な症状を欠くため初期の確定診断が容易ではなく、基礎疾患を持つ個人おいて40%に上る致死率を持つとされている。2015年の韓国での流行に見られるように、日本でもその流行の可能性があり対応が求められている新興ウイルス感染症である。原因はMERSコロナウイルスの感染であるが、現在このウイルスに対する有効なワクチンや薬剤は開発されていない。 MERSコロナウイルスは脂質二重膜とS蛋白質で構成される外膜を持つウイルスであり、S蛋白質を介した外膜と細胞膜との膜融合によって宿主細胞に侵入し感染を開始する。
このウイルスの取り扱いにはBSL3レベル(注3)の施設が要求され、感染性を持つ生ウイルスを用いた有効薬剤のスクリーニングは容易ではない。今回、本研究グループは生ウイルスを用いることなく安全、簡便かつ定量的にS蛋白質による膜融合を評価出来るハイスループット測定系を開発した。使用した測定系は医科研アジア感染症研究拠点北京拠点で開発されたデュアルスプリットプロテイン(DSP)と呼ばれる分割レポーター蛋白質を用いたもので、S蛋白質または宿主受容体を発現する293FT(注4)由来の細胞株を各々樹立し、それらを共培養してS蛋白質による細胞間膜融合を惹起し、その程度をDSPに由来するルシフェラーゼ活性で評価するものである(図1)。この測定系を384 wellプレート(注5)を用いたハイスループットスクリーニング測定系として至適化し、多数の候補薬剤のスクリーニングを可能とした。
ドラッグリプロファイリングを目的に現在臨床適用されている約1000種類の薬剤を対象にスクリーニングを実施した結果、S蛋白質による膜融合を低濃度で効果的に阻害する薬剤としてnafamostatを見いだした。nafamostatはセリンプロテアーゼ阻害剤であり、その作用点はS蛋白質が膜融合能を獲得するのに必須である宿主セリンプロテアーゼ(TMPRSS2、注6)の阻害であると考えられる。先行研究で同様のセリンプロテアーゼ阻害剤であるcamostatがMERSコロナウイルスの阻害剤として報告されているが、今回の結果ではnafamostatは camostatに比べて約100分の1の濃度で膜融合を阻害した。さらにnafamostatの実際のウイルス感染に対する効果を検証するために、国立感染症研究所との共同研究を行った。その結果、ウイルス感染に対してもnafamostatは顕著な阻害効果を示し、その有効阻害濃度は融合阻害の結果と同様camostatの約100分の1であり非常に強力なMERSコロナウイルスの感染阻害剤であることが確認された。
中東呼吸器症候群はMERSコロナウイルスによって引き起こされる感染症で、ラクダやコウモリを介した感染の可能性が示唆されている。高齢者や基礎疾患(糖尿病、高血圧、心疾患など)を有する患者においては致死率が高いことが報告されており高齢化社会を迎えている日本での流行は社会的・経済的損失の懸念があり、公衆衛生的対応が切望される。しかし、現在に至るまで対症療法しかなく、有効なワクチンや抗ウイルス剤は開発されていない。今回見いだされたnafamostatは既に他疾患での臨床適用を受けている薬剤であるだけでなく、以前にMERSコロナウイルスに対する効果が報告されているcamostatよりも効果が高い事が示され、 今後さらなる研究が必要ではあるがMERSコロナウイルス感染への迅速な応用が期待される。さらに、nafamostatの作用対象と考えられるセリンプロテアーゼTMPRSS2はMERSコロナウイルス以外のウイルス感染にも重要な役割を果たしていることが示されており、nafamostatあるいはその派生化合物の、より広範なウイルス感染症への適用も期待される。(本研究は国立研究開発法人日本医療研究開発機構(AMED)による感染症研究国際展開戦略プログラム(J-GRID)の支援を受けた。)
5.発表雑誌:
論文タイトル:Identification of nafamostat as a potent inhibitor of Middle East respiratory syndrome (MERS) corona virus S-mediated membrane fusion using the split protein-based cell-cell fusion assay
著者:Mizuki Yamamoto, Shutoku Matsuyama, Xiao Li, Makoto Takeda, Yasushi Kawaguchi, Jun-ichiro Inoue*, and Zene Matsuda*
DOI番号:10.1128/AAC.01043-16:
アブストラクトURL:http://aac.asm.org/content/early/2016/08/09/AAC.01043-16.abstract
6.お問い合わせ先:
内容に関すること
東京大学医科学研究所 分子発癌分野 教授
E-mail:jun-i“AT”ims.u-tokyo.ac.jp
Tel:03-5449-5275 Fax:03-5449-5421
AMED事業に関すること
国立研究開発法人日本医療研究開発機構 戦略推進部感染症研究課
E-mail:kansen“AT”amed.go.jp
Tel:03-6870-2225
※E-mailは上記アドレス“AT”の部分を@に変えてください。
7.用語解説:
- (注1)DSP:
- デュアルスプリットプロテインは分割レニラルシフェラーゼと分割GFPのキメラ蛋白質でそれぞれ単独では活性を持たないが、分割GFPドメインを介して自己会合しGFP活性並びにルシフェラーゼ活性を回復する。この特性を用いて、それぞれを別々の細胞に発現させておくと、GFP活性並びにルシフェラーゼ活性をもとにそれらの細胞間の融合を定量できる。
- (注2)ドラックリプロファイリング:
- ヒトでの安全性や体内動態が臨床で充分に確認されている既存薬から、新たな薬効を見つけ出し実用化へつなげていこうとする試み。
- (注3)BSL3レベル:
- バイオセーフティーレベル(BSL)とは世界保健機関(WHO)の指針に基づいて定められた、細菌・ウイルスなどの微生物・病原体等を取り扱う実験施設に必要な設備や管理体制の基準。MERSコロナウイルス等のヒトあるいは動物に対して重篤な病気を起こす病原体を扱うためにはBSL3レベルの厳格な管理体制が必要であるが、封じ込め実験室における安全キャビネット内での実験実施など、多数の薬剤の効果を試験することが困難な設備での実験が求められる。
- (注4)293FT:
- ヒト胎児腎臓由来の不死化細胞株で細胞増殖が速く遺伝子導入が簡便などの優れた性質を持つ。
- (注5)384 wellプレート:
- 多数の化合物を一定の条件下で検査するためには独立した空間に区切られた細胞培養のための容器が必要である。384 wellプレートは1枚のプレートが384個の約5ミリ四方の空間に区切られており、多数の化合物を同時に検査するのに適した容器である。
- (注6)TMPRSS2:
- Transmembrane protease, serine 2。細胞膜に存在するセリンプロテアーゼでMERSコロナウイルスS蛋白質は宿主受容体に結合後、TMPRSS2による蛋白質分解を受けるとされており、この蛋白質によるプロセシングを受けないと膜融合能を獲得できない。NafamostatはTMPRSS2活性を阻害することでS蛋白質による膜融合を阻害していると考えられる。
8.添付資料:
図1.DSP:デュアルスプリットプロテインを用いた細胞融合の定量化
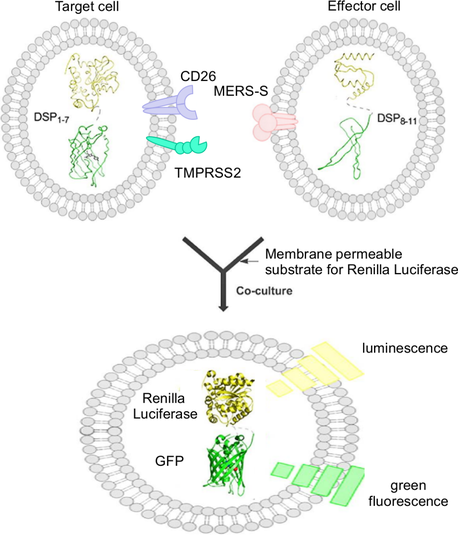
DSP:デュアルスプリットプロテインは分割レニラルシフェラーゼと分割GFPのキメラ蛋白質でそれぞれ単独では活性を持たないが、分割GFPドメインを介して自己会合しGFP活性並びにルシフェラーゼ活性を回復する。この特性を用いて、それぞれを別々の細胞に発現させておくと、GFP活性並びにルシフェラーゼ活性をもとにそれらの細胞間の融合を定量できる。(図はJ. Biol. Chem. 2010 May 7;285(19):14681-8.を改変)
掲載日 平成28年8月23日
最終更新日 平成28年8月23日


