エクソソームの高純度精製法の開発に成功―癌等の早期診断や治療効果判定の革新に期待―
プレスリリース
国立大学法人大阪大学
国立研究開発法人日本医療研究開発機構
研究成果のポイント
- 細胞から放出される小胞、エクソソームを高純度で抽出する新しい方法を開発
- エクソソームは癌細胞など病的細胞のバイオマーカー(注1)として有用であるが、これまでの精製法で得られるエクソソームは純度が低く、バイオマーカーとしての信頼性が懸念されていた
- 本研究成果を用いた高純度のエクソソーム抽出のためのキットは、国産試薬として既に製品化されている
概要
その結果、これまで同定することができなかったエクソソーム上の蛋白質やRNAの同定が可能となり、癌をはじめとした様々な疾患の早期診断や治療効果の判定に革新をもたらすことが期待されます。
本研究成果は、英国の科学雑誌『Scientific Reports』(日本時間 9月23日18時)にオンライン掲載されます。
研究の背景
エクソソームは様々な細胞が放出する直径30~100nmの細胞外小胞です。近年、エクソソームに含まれる蛋白質やRNAが癌細胞など病的細胞のバイオマーカー(注1)として有用であることが報告されており、疾患の早期診断や治療効果の判定などとの相関性が活発に研究されています。
しかし、これまでの精製法で得られたエクソソームには多くの不純物が含まれている為、バイオマーカーとしての信頼性が懸念されていました。
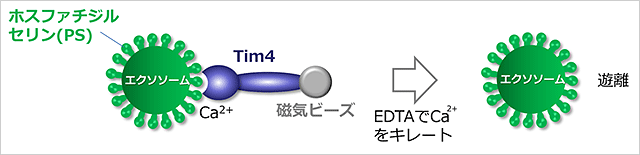 図.Tim4磁気ビーズを用いたエクソソームの新たな精製法
図.Tim4磁気ビーズを用いたエクソソームの新たな精製法
本研究の内容
本研究成果が社会に与える影響(本研究成果の意義)
今後、本技術によって精製されたエクソソームは、癌のみならず、免疫系や循環器系、脳神経系、内分泌系など様々な疾患のバイオマーカーの同定と解析に有用となりえます。
また、本技術では超遠心機(注2)などの高額な機器が不要であり、その簡便性から広く臨床検査の現場で使用可能です。今後、様々な疾患の早期診断や治療効果の判定、予後の予測などに用いることが期待されます。
なお、本技術は和光純薬工業株式会社よりMagCapture™ Exosome Isolation Kit PSとして製品化され、国産試薬として世界販売が開始されています。
特記事項
著者名:Wataru Nakai, Takeshi Yoshida, Diego Diez, Yuji Miyatake, Takahiro Nishibu, Naoko Imawaka, Ken Naruse, Yoshifusa Sadamura and Rikinari Hanayama.
タイトル:A novel affinity-based method for the isolation of highly purified extracellular vesicles.
本研究は、国立研究開発法人日本医療研究開発機構(AMED)の事業「革新的がん医療実用化研究事業」における研究開発課題「高純度エクソソーム精製法による新規腫瘍マーカーの同定」(研究開発代表者:華山力成)の一環で行われました。また、大阪大学免疫学フロンティア研究センター(IFReC)は、日本が科学技術の力で世界をリードしていくため「目に見える世界的研究拠点」の形成を目指す文部科学省の「世界トップレベル研究拠点プログラム(WPI)」に採択されています。
詳しい研究の解説
研究の背景
エクソソームは様々な細胞が放出する直径30~100nmの細胞外小胞で、分泌細胞と標的細胞の間で脂質や蛋白質、RNAなどを交換する新たな媒体として注目されています。近年、エクソソームの構成分子(特に蛋白質やRNA)が癌細胞など病的細胞のバイオマーカー(注1)として有用であることが報告されており、疾患の早期診断や治療効果の判定、予後の予測などとの相関性が活発に研究されています。例えば、悪性黒色腫細胞が放出するエクソソームにはTYRP2、VLA-4、METなどの蛋白質が高濃度に含まれており、転移能や進行を予期できるマーカーとしての可能性が報告されています(Nat Med. 18:881-891(2012))。またエクソソームには分泌細胞由来のmRNAやnon-coding RNAが多く含まれており、これらが微量なサンプルでもPCR法で増幅可能であることから、画期的なバイオマーカーとして疾患との相関性と特異性が広く研究されています(Biochim Biophys Acta. 1806(2):200-207(2010))。
現在、エクソソームの精製には超遠心法(注2)やPEG沈殿法(注3)などが主に用いられていますが、これらの精製法で得られたエクソソームには多くの不純物が含まれている為、バイオマーカーとしての信頼性が懸念されております。また超遠心法は操作が煩雑である為、回収量が不安定で定量的な解析が行えない上に、高額な超遠心機が必要である為、多検体の解析が行えないなどの問題点が存在します。このような状況では、エクソソームをバイオマーカーとして用いるのは困難であり、エクソソームを簡易に高純度で精製する技術の開発が期待されています。
本研究成果の内容
我々は、Tim4という膜蛋白質が標的細胞におけるエクソソームの特異的な受容体であることを見出しました。Tim4を発現した細胞はTim4の細胞外領域にあるIgVドメインを介して、エクソソーム膜表面に存在するリン脂質ホスファチジルセリン(PS)とカルシウムイオン依存的に強く結合し、エクソソームを細胞内へと取り込みます。そこで我々は、Tim4の細胞外領域と磁気ビーズとを結合させた「Tim4磁気ビーズ」を作製しました。Tim4はエクソソーム膜表面のPSとカルシウムイオン依存的に結合することから、キレート剤(注4)であるEDTAを含む溶出バッファー(注5)を用いることで遊離させ、高純度なエクソソームを効率よく精製することが可能です(図1)。
実際、Tim4磁気ビーズ法を用いて、ヒト白血病細胞から放出されたエクソソームを精製し、その純度を超遠心法やPEG沈殿法により精製したエクソソームと比較したところ、Tim4磁気ビーズ法は他の方法に比べ10~100倍以上に高純度なエクソソームを再現性よく回収できることが明らかとなりました(図2)。その結果、これまで同定することができなかったエクソソーム上の蛋白質やRNAを数多く同定することが可能となりました。以上の結果から、Tim4磁気ビーズ法の有用性が示され、エクソソームを簡易かつ高純度に精製する方法の開発に成功しました。
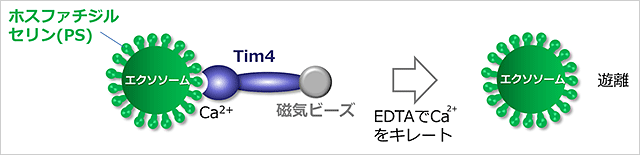 図1.Tim4磁気ビーズを用いたエクソソームの精製法
図1.Tim4磁気ビーズを用いたエクソソームの精製法
Tim4磁気ビーズはカルシウムイオン依存的にエクソソーム膜表面のリン脂質ホスファチジルセリンと結合する。Tim4磁気ビーズに結合したエクソソームはEDTAでカルシウムイオンをキレートすることにより遊離することができる。
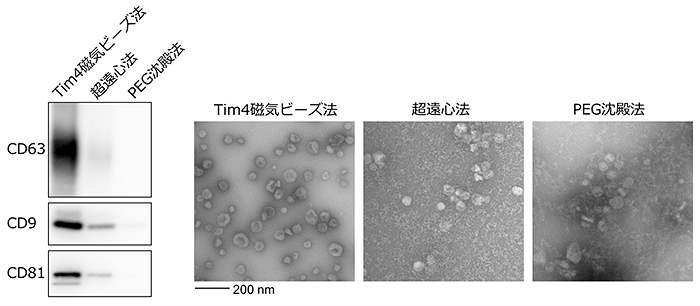
図2.各種精製法によるエクソソームの純度比較
Tim4磁気ビーズ法では超遠心法やPEG沈殿法に比べ、エクソソームに特異的な蛋白質がより強く検出される(左)とともに、エクソソーム以外の夾雑物がほとんど混入していない(右)。
本研究成果が社会に与える影響(本研究成果の意義)
近年、エクソソーム研究が加速的に進展していますが、これらの研究では超遠心法やPEG沈殿法などで精製された純度の低いエクソソームが使用されており、エクソソーム本来の機能を反映しているのかは実際のところ不明であります。今回我々が開発したエクソソームの高純度精製技術は、エクソソーム研究そのものの方法論を大きく変える革新的な解析技術になると期待されます。今後、本技術によって精製されたエクソソームは、癌のみならず、免疫系や循環器系、脳神経系、内分泌系など様々な疾患のバイオマーカーの同定と解析に有用となりえます。また、本技術では超遠心機などの高額な機器が不要であり、その簡便性から広く臨床検査の現場で使用可能です。今後、疫学研究と相関させることによって、様々な疾患の早期診断や治療効果の判定、予後の予測などに用いることが可能となります。なお、本技術は和光純薬工業株式会社よりMagCapture™ Exosome Isolation Kit PSとして製品化され、国産試薬として世界販売が開始されています。
用語解説
- (注1):バイオマーカー
- 血液や尿、髄液などの体液中に含まれる蛋白質やRNAなどの物質で、その濃度が特定の疾病の存在や進行度と相関する指標となる。
- (注2):超遠心法
- 超遠心分離機を用いて、試料に強大な遠心力をかけることにより、その試料の成分を分離する方法。
- (注3):PEG沈殿法
- ポリエチレングリコール(PEG)を用いて、試料から高分子などを沈殿させる方法。
- (注4):キレート剤
- 金属イオンに結合し、その金属の作用を不活化する物質。
- (注5):溶出バッファー
- 特定の物質間の結合を解離させる溶液。
お問い合わせ先
取材等に係る連絡先
金沢大学医学系免疫学教授(兼:大阪大学免疫学フロンティア研究センター招へい教授)
華山 力成(はなやま りきなり)
〒920-8640 石川県金沢市宝町13番1号
TEL:076-265-2727 FAX:076-265-2734
E-mail:hanayama“AT”med.kanazawa-u.ac.jp
機関窓口
国立研究開発法人日本医療研究開発機構(AMED) 戦略推進部がん研究課
〒100-0004 東京都千代田区大手町一丁目7番1号
TEL:03-6870-2221
E-mail:cancer“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
関連リンク
掲載日 平成28年9月23日
最終更新日 平成28年9月23日


