細胞外マトリックスを用いてヒト多能性幹細胞から高効率に血管内皮細胞の誘導に成功
プレスリリース
京都大学iPS細胞研究所
大阪大学蛋白質研究所
国立研究開発法人日本医療研究開発機構
ポイント
- 細胞外マトリックス(注1)のひとつラミニン411(LM411)(注2)の組換えタンパク質断片(LM411-E8)を用い、ヒトiPS細胞から血管内皮細胞への高効率な分化誘導法を開発した。
- iPS細胞が中胚葉前駆細胞を経て血管内皮へと分化する際、LM411-E8との接着を介したシグナルが細胞の運命決定と増殖に重要な役割を果たすことを明らかにした。
- LM411-E8と低分子化合物を組み合わせることにより、フィーダー細胞フリーで動物由来成分を含まない条件で、iPS細胞から血管内皮細胞を高効率に分化誘導する方法を確立した。
- この方法で分化誘導した血管内皮細胞は、試験管内のみならず生体内でも血管様構造の形成が可能であり、マウス由来の血液が環流していた。
1.要旨
京都大学iPS細胞研究所(CiRA)の齋藤潤准教授グループ(太田諒大学院生、丹羽明特定拠点助教、中畑龍俊教授ら)と、大阪大学蛋白質研究所の関口清俊寄附研究部門教授グループらの共同研究チームは、細胞外マトリックスのひとつラミニン411(LM411)の組換えタンパク質断片(LM411-E8)を用いることにより、ヒト多能性幹細胞(注3)から正常機能を有する血管内皮細胞を高効率に分化誘導する手法の開発に成功しました。
この研究は、京都大学CiRAと大阪大学蛋白質研究所の共同研究として、国立研究開発法人日本医療研究開発機構(AMED)の再生医療実現拠点ネットワークプログラムによる支援を受け行われました。成果は10月31日午前10時(英国時間)に英国科学誌Scientific Reportsに掲載されます。
2.研究成果
コラーゲンを始めとする一部の細胞外マトリックスは、細胞培養において細胞の生存率や増殖率を上げる細胞の足場として利用され、細胞の種類により適した細胞外マトリックスの種類があることが知られていました。しかし、細胞外マトリックスを単なる足場としてだけでなく、細胞分化における運命決定の制御因子として着目した研究はほとんどありませんでした。
血管の内側は血管内皮細胞の層で覆われており、血液の凝固を防いだり、血中のコレステロールを取り込んだりして、血液がスムーズに流れるための役割を担っています。血管内皮細胞は常に新陳代謝されており、その管腔構造を保つため、細胞外マトリックスが重要な役割を果たすと考えられています。研究チームによる基礎検討で、細胞外マトリックスのひとつLM411が血管に沿って管腔状に存在する知見を得ていました。そこで、ヒト多能性幹細胞から血管内皮細胞への分化過程において、LM411が与える影響を詳細に解析しました。
3.研究結果
1. LM411、およびLM411-E8断片はiPS細胞から血管内皮細胞への分化を支持する
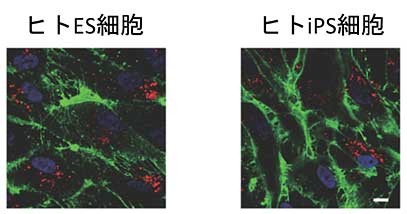 図1:ヒト多能性幹細胞から誘導した血管内皮細胞。
図1:ヒト多能性幹細胞から誘導した血管内皮細胞。赤色は内皮細胞に取り込まれたコレステロール。
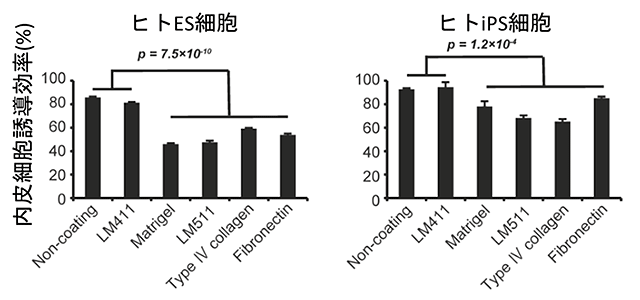 図2:様々なマトリックスによる、内皮細胞誘導効率の比較。
図2:様々なマトリックスによる、内皮細胞誘導効率の比較。
-
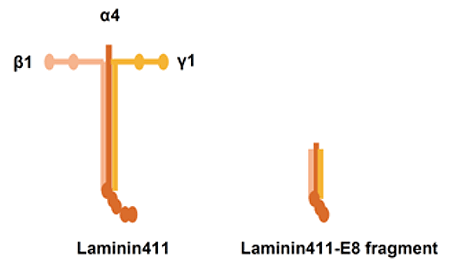 図3:LM411とLM411-E8断片の模式図
図3:LM411とLM411-E8断片の模式図
-
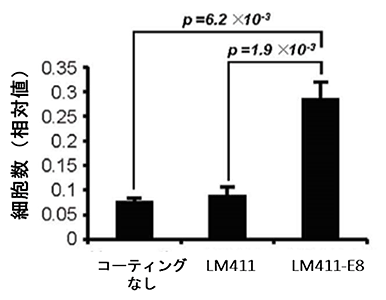 図4:LM411-E8断片は血管内皮細胞への分化を促進する
図4:LM411-E8断片は血管内皮細胞への分化を促進する
2. LM411-E8は、血管内皮細胞への分化増殖を修飾・賦活する因子としての作用を持つ
3. 正常な血管機能のある血管内皮前駆細胞への高効率な無血清分化誘導
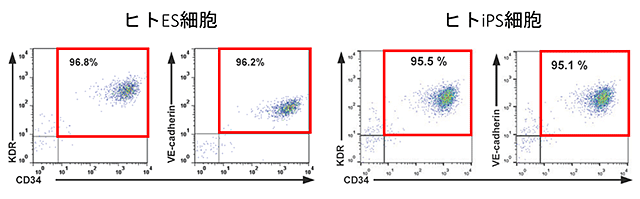
図5:改良された分化方法による内皮細胞の誘導効率。
赤枠内が内皮細胞
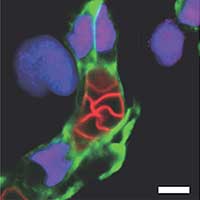
図6:マウス皮下に移植した血管内皮細胞由来の血管様構造。
緑:内皮細胞、赤:マウス赤血球、紫:ヒト由来細胞核。ヒト由来内皮細胞でできた構造の中にマウス赤血球が確認される。
4.研究の意義
ヒト多能性幹細胞の応用という実用的観点から、本研究成果による高純度で簡便な血管内皮誘導は今後の再生医療や様々な疾患解析研究への展開に直結するものと考えます。
同時に、ともすればこれまで「細胞の足場」としての側面に偏って捉えられがちであった細胞外マトリックスの機能について、「作用因子」としての役割の一端を明らかにした点にも本研究の意味があります。細胞外マトリックスは発生初期から生涯にわたり体内に豊富に存在し、様々な組織で細胞運命決定に少なからず影響を与えています。本研究が血管内皮細胞分化をモデルに示したように、今後あらゆる組織における細胞外マトリックスの新たな作用機序解明にiPS細胞は役立つと考えられます。さらに、そうした研究の成果が再びiPS細胞を用いた再生医療の開発に還元できると期待されます。
5.論文名と著者
- 論文名
- “Laminin-guided highly efficient endothelial commitment from human pluripotent stem cells.”
- ジャーナル名
- Scientific Reports
- 著者
- Ryo Ohta1*, Akira Niwa1*, Yukimasa Taniguchi2, Naoya M. Suzuki1, Junko Toga2, Emiko Yagi2, Norikazu Saiki1, Yoko Nishinaka-Arai1, Chihiro Okada3,4, Akira Watanabe3, Tatsutoshi Nakahata1, Kiyotoshi Sekiguchi2** and Megumu K. Saito1**
*筆頭著者、**責任著者 - 著者の所属機関
-
- 京都大学iPS細胞研究所(CiRA)
- 大阪大学 蛋白質研究所
- 京都大学 iPS細胞研究所 未来生命科学開拓部門
- 三菱スペース・ソフトウエア
6.本研究への支援
本研究は、下記機関より資金的支援を受けて実施されました。
- 日本学術振興会・文部科学省 科学研究費補助金
- 内閣府 最先端研究開発支援プログラム
- AMED 再生医療実現拠点ネットワークプログラム「iPS細胞研究中核拠点」
- AMED 再生医療実現拠点ネットワークプログラム「疾患特異的iPS細胞を活用した難病研究」
- AMED 再生医療実現拠点ネットワークプログラム「技術開発個別課題」
7.用語説明
- (注1)細胞外マトリックス
- 細胞間の隙間を埋める生体高分子(コラーゲンやプロテオグリカンなど)の集合体。骨・軟骨、歯、皮膚などに多く含まれ、組織を支えてメカニカル(クッション・伸び縮みなど)な機能を果たしている。
- (注2)ラミニン
- 細胞を接着させるために重要なタンパク質。上皮細胞や筋細胞、血管内皮細胞など様々な細胞で分泌合成されている。様々なタイプのラミニンがあり、細胞の種類によって作られているラミニンは異なる。
- (注3)ヒト多能性幹細胞
- 自分を増やす能力(自己増殖能)と様々な細胞に変化する能力(多分化能)を持つ特殊な細胞。胚性幹細胞(ES細胞)や人工多能性幹細胞(iPS細胞)が含まれる。
- (注4)マトリゲル
- マウスの肉腫細胞から抽出したマトリックス。動物由来の様々な成分を含む。
- (注5)免疫不全マウス
- ヒトの細胞が生着しやすいように免疫能を低下させたマウスのこと。
お問い合わせ先
本件担当
京都大学iPS細胞研究所(CiRA)
研究支援部門 国際広報室
和田濵
TEL:075-366-7005 FAX:075-366-7152
E-mail:media“AT”cira.kyoto-u.ac.jp
大阪大学蛋白質研究所
庶務係
吉村 則子
TEL:06-6879-4317 FAX:06-6879-8590
E-mail: tanpakuken-syomu“AT”office.osaka-u.ac.jp
AMED事業に関するお問い合わせ先
国立研究開発法人日本医療研究開発機構(AMED)
戦略推進部 再生医療研究課
〒100-0004 東京都千代田区大手町一丁目7番1号
TEL:03-6870-2220 FAX:03-6870-2242
E-mail:saisei“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
掲載日 平成28年11月2日
最終更新日 平成28年11月2日


