治療抵抗型統合失調症の治療薬の作用機序の一端を発見―治療反応性を予測するバイオマーカーの開発に期待―
プレスリリース
国立大学法人大阪大学
慶應義塾大学
国立研究開発法人日本医療研究開発機構
本研究成果のポイント
- 治療抵抗性統合失調症※1のクロザピン反応性が異なる※2一卵性双生児患者のiPS神経細胞由来分化神経細胞において、細胞接着※3系分子群の患者間における発現量の相違を発見。
- 治療抵抗性統合失調症に唯一有効な抗精神病薬であるクロザピンは、同症患者の約6割に有効であるが、これまでそのメカニズムは不明で、動物モデルでの研究では本疾患に対する研究が進展していなかった。
- 今後、クロザピンの治療反応性を予測するバイオマーカー※4の開発や、将来的に治療抵抗性統合失調症に対する有効な新規治療薬の開発に資することに期待。
研究成果の概要
治療抵抗性統合失調症に唯一有効な抗精神病薬であるクロザピンの有効性のメカニズムが不明であるとともに、副作用の問題もあり、クロザピンが十分に普及していない現状において、最先端の技術を用いてiPS細胞由来の治療抵抗性統合失調症患者神経細胞を作製し、クロザピン反応性の分子メカニズムの一端を見いだしたことは、精神医学領域や基礎医学/薬学領域において注目される成果です。
今後、今回発見した細胞接着系遺伝子群の発現量の相違が、クロザピン治療反応性の分子メカニズムの包括的解明の糸口となる可能性のみならず、クロザピンに対する反応性を予測するマーカーとなる可能性が考えられます。また、治療抵抗性統合失調症に対する有効かつ副作用の少ない新たな治療薬の開発が期待されるだけでなく、あらかじめ患者由来の神経細胞により治療反応性を予測でき、客観的診断法としても役立つことが期待されます。
なお、本研究成果は、国際的な学術専門雑誌「Schizophrenia Research」の電子版に11月3日(木)午前4時(米国東部標準時)に掲載予定です。
研究の背景
統合失調症は幻覚・妄想、意欲低下、および認知機能障害等が認められる精神障害で、約100人に1人が発症する非常に頻度が高い疾患です。現存する治療薬を用いても充分に治療されない患者も多く、また主要な治療薬の副作用も大きな問題となっています。複数の抗精神病薬を、十分量、十分期間投与しても改善が認められない治療抵抗性統合失調症患者の存在も大きな問題です。
治療抵抗性統合失調症に唯一有効な抗精神病薬であるクロザピン治療は、治療抵抗性統合失調症患者の約6割程度に有効であることが知られておりますが、クロザピンには無顆粒球症※5という致死的な副作用が、0.5~1.0%程度に認められており、クロザピンが十分に普及しない大きな原因の1つとなっています。また、クロザピンは複雑な薬理学的特性をもっているため、クロザピンの有効性のメカニズムは未だ不明です。
クロザピンの有効性のメカニズムを明らかにするためには、治療抵抗性統合失調症患者の神経細胞を用いた研究が重要でありますが、患者脳サンプルを研究に用いることはできないことから、現在までは、主に動物モデルや齧歯類の神経細胞を用いた研究が主流でした。しかし、治療抵抗性統合失調症に対する確立した動物モデルがなく、研究は進んでおりませんでした。
研究の内容
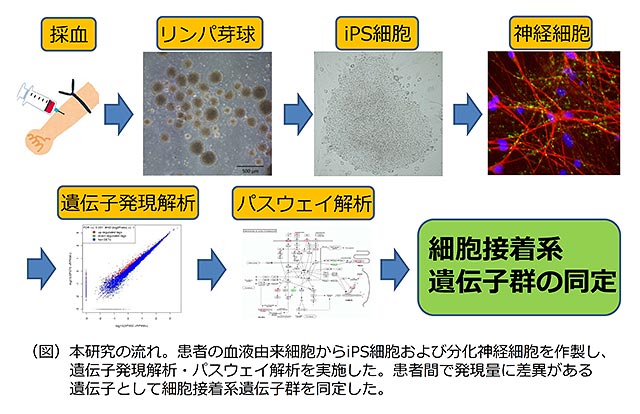
今回の一卵性双生児患者では、片方の患者は治療抵抗性統合失調症治療薬のクロザピンの投与で改善し、他方の患者においてはクロザピンの効果がありませんでした。一卵性双生児にも関わらず、明確に抗精神病薬に対する治療反応性に相違がある分子メカニズムを明らかにすることを目的として、両者の不死化リンパ芽球※6からiPS細胞を作製し、神経細胞へと分化させました。得られたiPS細胞由来分化神経細胞から全RNAを調製し、遺伝子発現解析を実施しました。
その結果、クロザピンの効果が見られた患者では、効果がみられなかった患者と比較して、167遺伝子で高い発現が見られ、95遺伝子で低い発現が見られました。それらのトータル262遺伝子に関して、パスウェイ解析※7を実施したところ、細胞接着関連の機能が推定されるグループに有意に濃縮されていることがわかりました。iPS細胞および分化神経細胞の作製に使用した患者の不死化リンパ芽球についても同じ解析を行いましたがその発現に同様な差異がありませんでした。
従って、本研究で明らかにした両患者間における遺伝子発現の差異は、iPS細胞由来分化神経細胞にのみ見られることがわかりました。
本研究成果が社会に与える影響
すなわち、本研究により得られた成果は、治療抵抗性統合失調症に対する有効かつ副作用の少ない新たな治療薬の開発に貢献することが期待されるのみならず、あらかじめ患者由来の神経細胞により治療反応性を予測することが可能となり、客観的診断法としても役立つことが期待されます。また、(治療抵抗性)統合失調症の細分類化が可能となる、新たな系の開発に資することが期待されます。
用語解説
- ※1 治療抵抗性統合失調症患者:
- 複数の抗精神病薬を、十分量、十分期間投与しても改善が認められない統合失調症患者。
- ※2 クロザピン反応性が異なる
- 今回の一卵性双生児患者では、片方の患者は治療抵抗性統合失調症治療薬のクロザピンの投与で寛解し、他方の患者においてはクロザピンの効果がなかった。
- ※3 細胞接着:
- 細胞同士が接着すること。神経細胞では、神経細胞の移動といった神経発達、神経細胞からの軸索誘導、あるいはシナプス形成等にとって必須。
- ※4 バイオマーカー:
- 特定の疾患等において、生体の変化を定量化することを可能にする指標。
- ※5 無顆粒球症:
- 顆粒球(好中球)が、ほとんど認められない症状。生命が危機にさらされる。
- ※6 不死化リンパ芽球:
- ヒト(患者)のリンパ球の一つであるB細胞をウイルス感染により不死化させたもの。活発な増殖能を持つので、研究によく使われる。
- ※7 パスウェイ解析:
- 発現変動遺伝子がどの機能、代謝経路に関与しているのかを網羅的に調べる解析方法。
研究支援
特記事項

本件に関する問い合わせ先
研究内容に関わる件
大阪大学大学院医学系研究科情報統合医学講座精神医学教室
准教授 橋本亮太
電話:06-6879-3074; E-mail: hashimor“AT”psy.med.osaka-u.ac.jp
大阪大学大学院歯学研究科薬理学教室
准教授 中澤敬信
電話:06-6879-2913; E-mail: nakazawa“AT”phs.osaka-u.ac.jp
事業に関わる件
日本医療研究開発機構 脳と心の研究課
電話:03-6870-2222; E-mail:brain-pm“AT”amed.go.jp
※Eメールは上記アドレス“AT”の部分を@に変えてください。
関連リンク
掲載日 平成28年11月4日
最終更新日 平成28年11月4日


