腸で鉄の吸収を調節するメカニズムの一端を解明―貧血時に鉄吸収を促進するフィードバック機構を発見―
プレスリリース
国立大学法人京都大学
国立研究開発法人日本医療研究開発機構
概要
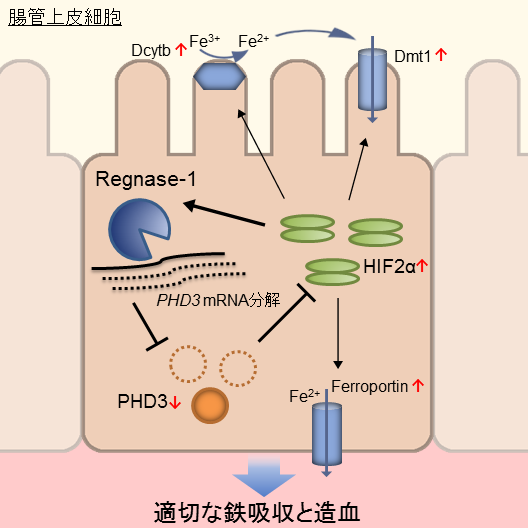 図1:Regnase-1による腸管の鉄吸収調節モデル
図1:Regnase-1による腸管の鉄吸収調節モデル
鉄は生体にとって非常に重要な元素のひとつです。体内の鉄の量が不足すると貧血を生じ、逆に過剰になると臓器が機能不全を起こすヘモクロマトーシスといった疾患の原因になります。したがって生物の体内での鉄の量は、さまざまな仕組みにより厳密に調節されています。鉄代謝を制御する機構の一つとして、関連する遺伝子のmRNAの安定性を調節する機構の重要性が知られています。既に鉄代謝にかかわるmRNAを安定化する因子は判明しており、研究が進められています。しかし、鉄代謝にかかわるmRNAの分解を促進する機構はほぼ明らかになっていませんでした。
本研究では、鉄代謝にかかわるタンパク質のなかでトランスフェリン受容体(※ⅱ)とPHD3(※ⅲ)のmRNAをRegnase-1が分解することを解明しました。また、Regnase-1はPHD3のmRNAを分解することで、腸での鉄吸収において重要な転写因子であるHIF2αを安定化させ、腸管での鉄吸収を促進する役割があることを明らかにしました。さらに、Regnase-1自身がHIF2αの標的遺伝子であり、Regnase-1、PHD3、HIF2αの三者からなる正のフィードバック機構が腸管での鉄吸収を調節していることを発見しました。本研究は、慢性炎症における鉄代謝制御機構、貧血などの鉄代謝異常による疾患の病態解明や、新たな治療法の開発に繋がることが期待されます。
本研究は、大阪大学、東京大学、兵庫医科大学と共同で行ったものです。本研究成果は、2017年5月24日(日本時間)発行の米国科学誌Cell Reportsに掲載されます。
1.背景
鉄は生体において非常に重要な元素のひとつです。食事から得られた鉄は、ヘモグロビンとして酸素の運搬を担い、また貯蔵鉄として体内に蓄積されます。体内の鉄の量の異常によって引き起こされる疾患もあるため、体内の鉄の量はさまざまな仕組みにより厳密に調節されています。
そのような仕組みの一つに、mRNAの安定性を調節する機構が知られています。鉄代謝にかかわる遺伝子はDNAからmRNAが転写され、mRNAからタンパク質が翻訳されることで機能を発揮しますが、mRNAを分解、または安定化することでも最終的なタンパク質の産生量が調節されています。鉄代謝においては、以前からmRNAを安定化する因子としてIRP(※ⅳ)の存在が知られていました。また、鉄代謝にかかわる遺伝子のひとつであるトランスフェリン受容体のmRNAは、RNA分解酵素により分解されると提唱されていましたが、このプロセスにどのRNA分解酵素が関与するかは不明なままでした。
本研究グループはこれまでにRNA分解酵素であるRegnase-1を発見し、この分子が炎症関連遺伝子のmRNAを分解することで免疫機能を抑制していることを報告してきました。この研究の過程でRegnase-1を欠損したマウスが、炎症性疾患に加え、重度の貧血を発症することを見出しました。これまで、慢性炎症により貧血になることはよく知られており、Regnase-1が慢性炎症時の貧血発症にかかわる可能性が示唆されました。しかしながら、Regnase-1欠損マウスにおいて貧血がどのようにして起こるのかは明らかになっていませんでした。そこで本研究では、Regnase-1が鉄代謝において果たす役割の解明を目指しました。
2.研究手法・成果
次にRegnase-1の生体での鉄代謝における役割を調べるため、Regnase-1を欠損したマウスを用いて解析を行ったところ、このマウスは重度の貧血に加えて極度の鉄欠乏状態であることが明らかになりました。さらに解析を進めたところ、Regnase-1欠損マウスでは腸管での鉄吸収が低下しているため鉄欠乏性貧血が起こることが明らかとなり、Regnase-1は腸管での鉄吸収にとって重要な因子であることが分かりました。
では、どのようにしてRegnase-1は腸管での鉄吸収を調節しているのでしょうか。網羅的な解析の結果、腸管での鉄吸収に関与するRegnase-1の標的遺伝子がPHD3であることを発見しました。PHD3は腸管での鉄吸収に重要な転写因子であるHIF2αを分解することが知られています。実際Regnase-1欠損マウスではHIF2αの活性が抑制されており、PHD3の発現が活発になるため鉄吸収機構を活性化できないことが、Regnase-1欠損マウスでの鉄吸収異常の原因と考えられました。次にPHD3とRegnase-1の二重欠損マウスを作成したところ、このマウスでは鉄欠乏性貧血が改善することがわかりました。これらの結果から、PHD3がRegnase-1の鉄吸収における重要な標的であることが示されました。
更に、Regnase-1は鉄欠乏において発現が増加する遺伝子であることを見出しました。また、鉄欠乏で活性化される因子であるHIF2αによって、Regnase-1の転写が促進されることも明らかになりました。これらの結果から、鉄欠乏時にはRegnase-1、PHD3、HIF2αの三者からなる正のフィードバックループが活性化し、腸管での適切な鉄吸収を行っていることが分かりました(図1)。
3.波及効果・今後の予定
本研究では、Regnase-1が腸管での鉄吸収にとって重要な因子であることを解明しました。今後ヒトの貧血や鉄代謝異常におけるRegnase-1の役割を検討することで、これら疾患のさらなる病態解明に発展することが期待されます。また、Regnase-1の活性を調節することで、これらの疾患の治療につながることが期待されます。
本研究では,鉄代謝に焦点を当ててRegnase-1の作用を検討しました。Regnase-1は炎症の制御においても重要な因子であり、鉄代謝は慢性炎症とも関わりが深いことからRegnase-1が慢性炎症と鉄代謝の2つの経路を結ぶ因子として働いていると考えています。今後そのメカニズムのさらなる解明に取り組んでいく予定です。
4.研究プロジェクトについて
5.論文タイトルと著者
- タイトル:
- Regnase-1 maintains iron homeostasis via the degradation of transferrin receptor 1 and prolyl hydroxylase domain-containing protein 3 mRNAs
- 著者:
- Masanori Yoshinaga, Yoshinari Nakatsuka, Alexis Vandenbon, Daisuke Ori, Takuya Uehata, Tohru Tsujimura, Yutaka Suzuki, Takashi Mino, Osamu Takeuchi
- 掲載誌:
- Cell Reports
注釈
- (※ⅰ)Regnase-1:
- 免疫の活性化を担うタンパク質であるサイトカインのmRNA を分解することで過剰な免疫応答や炎症を抑制するRNA分解酵素。
- (※ⅱ)トランスフェリン受容体:
- 体内で鉄イオンの輸送を担うトランスフェリンに結合した血中の鉄を細胞内に取り込むための受容体。
- (※ⅲ)PHD3:
- 腸での鉄吸収にかかわる遺伝子の転写を活性化することが知られている転写因子HIF2αの分解を誘導する酵素。
- (※ⅳ)IRP:
- トランスフェリン受容体などの鉄代謝にかかわる遺伝子のmRNAを安定化するRNA結合タンパク質。
お問い合わせ先
報道に関すること
竹内 理(タケウチ オサム)
京都大学ウイルス・再生医科学研究所 感染防御分野 教授
Tel:075-751-4024 Fax:075-761-5766
E-mail:otake“AT”infront.kyoto-u.ac.jp
事業に関すること
国立研究開発法人日本医療研究開発機構(AMED)
革新的先端研究開発支援事業
基盤研究事業部 研究企画課
Tel:03-6870-2224 Fax:03-6870-2243
E-mail:kenkyuk-ask“AT”amed.go.jp
※E-mailは上記アドレス“AT”の部分を@に変えてください。
掲載日 平成29年5月24日
最終更新日 平成29年5月24日


